Casirivimab i Imdevimab u pacjentów przyjmowanych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe
Mar 26, 2022
Po więcej informacji:ali.ma@wecistanche.com
Streszczenie
Tło
Casirivimab i imdevimab to niekonkurujące przeciwciała monoklonalne, które wiążą się z dwoma różnymi miejscami w domenie wiążącej receptorSARS-CoV-2glikoproteina kolczasta, blokująca wejście wirusa do komórek gospodarza. Celem naszej pracy była ocena skuteczności i bezpieczeństwa casirivimabu i imdevimabu podawanych w skojarzeniu u pacjentów przyjętych do szpitala zCOVID-19.
Metody
RECOVERY to randomizowane, kontrolowane, otwarte badanie platformowe porównujące kilka możliwych metod leczenia ze standardową opieką u pacjentów przyjętych do szpitala zCOVID-19. W ocenie casirivimabu i imdevimabu wzięło udział 127 szpitali w Wielkiej Brytanii. Uprawnionymi uczestnikami byli wszyscy pacjenci w wieku co najmniej 12 lat przyjęci do szpitala z klinicznym podejrzeniem lub potwierdzonym laboratoryjnie zakażeniem SARS-CoV-2. Uczestnicy zostali losowo przydzieleni (1:1) albo do standardowego leczenia samodzielnie, albo do standardowej opieki plus casirivimab 4 g i imdevimab 4 g podawane razem w pojedynczej infuzji dożylnej. Badacze i oceniający dane zostali zamaskowani do analizy danych wynikowych podczas badania. Pierwszorzędowym punktem końcowym była 28-dniowa śmiertelność z jakiejkolwiek przyczyny oceniona na podstawie zamiaru leczenia, najpierw tylko u pacjentów bez wykrywalnych przeciwciał przeciwko zakażeniu SARS-CoV-2 przy randomizacji (tj. u tych, którzy byli seronegatywni), a następnie w całej populacji. Bezpieczeństwo oceniano u wszystkich uczestników, którzy otrzymali casirivimab i imdevimab. Badanie jest zarejestrowane w ISRCTN (50189673) i ClinicalTrials.gov (NCT04381936).
Wyniki
Między 18 września, 2020 a 22 maja, 2{{3{0}}21, 9785 pacjentów zapisanych do programu RECOVERY kwalifikowało się do casirivimabu i imdevimabu, z czego 4839 było losowo przydzielone do casirivimabu i imdevimabu plus standardowa opieka, a 4946 do zwykłej opieki. 3153 (32%) z 9785 pacjentów było seronegatywnych, 5272 (54%) było seropozytywnych, a 1360 (14%) miało nieznany wyjściowy stan przeciwciał. Wiadomo, że 812 (8 procent) pacjentów otrzymało co najmniej jedną dawkę szczepionki SARS-CoV-2. W pierwotnej populacji pacjentów seronegatywnych oceniających skuteczność, 396 (24%) z 1633 pacjentów przydzielonych do casirivimabu i imdevimabu w porównaniu z 452 (30 procent) z 1520 pacjentów przydzielonych do zwykłej opieki zmarło w ciągu 28 dni (współczynnik częstości [RR] 0,79, 95 procent CI 0,69–0,91; p=0·0009). W analizie wszystkich losowo przydzielonych pacjentów (niezależnie od wyjściowego statusu przeciwciał), 943 (19 procent) z 4839 pacjentów przydzielonych do casirivimabu i imdevimabu w porównaniu do 1029 (21%) z 4946 pacjentów przydzielonych do zwykłej opieki zmarło w ciągu 28 dni (RR 0·. 94, 95% CI 0·86–1,02; p=0·14). Proporcjonalny wpływ casirivimabu i imdevimabu na śmiertelność różnił się istotnie między pacjentami seropozytywnymi i seronegatywnymi (wartość p dla heterogeniczności=0·002). Nie było zgonów przypisywanych leczeniu ani znaczących różnic między grupami we wcześniej określonych wynikach bezpieczeństwa dotyczących zgonu z przyczyn przyczynowo-skutkowych, zaburzeń rytmu serca, zakrzepicy lub poważnych krwawień. Poważne działania niepożądane zgłoszone w siedmiu (<1%) participants="" were="" believed="" by="" the="" local="" investigator="" to="" be="" related="" to="" treatment="" with="" casirivimab="" and="">
Interpretacja
U pacjentów przyjętych do szpitala z COVID-19 połączenie przeciwciała monoklonalnego casirivimabu i imdevimabu zmniejszyło 28-dniową śmiertelność u pacjentów seronegatywnych (a zatem nie uzyskano własnego stężenia humoralnegoodpornyodpowiedź) na początku badania, ale nie u osób seropozytywnych na początku badania.
Finansowanie
UK Research and Innovation (Medical Research Council) i National Institute of Health Research
RECOVERY Collaborative Group
Wstęp
Przeciwciała monoklonalne to zestaw identycznych przeciwciał, które mają wysoką specyficzność i powinowactwo do pojedynczego epitopu. Wykazano, że są one bezpieczne i skuteczne w wybranych chorobach wirusowych, gdy są stosowane w profilaktyce (wirus syncytialny układu oddechowego) lub w leczeniu (choroba wirusowa Ebola).1–3 Uważa się, że skuteczność kliniczna przeciwciał monoklonalnych w zakażeniach wirusowych zależy od bezpośredniego wiązania do uwolnienia cząstek wirusa i neutralizacji ich zdolności do infekowania komórek gospodarza. Przeciwciała monoklonalne mogą również wiązać się z antygenami wirusowymi wyrażanymi na powierzchni zakażonych komórek i stymulować zależną od przeciwciał fagocytozę i cytotoksyczność poprzez krystalizujący fragment fragmentu przeciwciała.4
Kliknij na Cistanches i Cistanche produkty na odporność
Zakażenie SARS-CoV-2 jest inicjowane przez związanie wirusowej transbłonowej glikoproteiny wypustek z enzymem konwertującym angiotensynę 2 na powierzchni komórek gospodarza.5 Domena wiążąca receptor glikoproteiny wypustek jest w konsekwencji głównym celem neutralizacji przeciwciała.6 Po pojawieniu się SARS-CoV-2, przeciwciała monoklonalne skierowane na domenę wiążącą receptor wypustek zostały szybko wyizolowane z humanizowanych myszy i obwodowych komórek B odzyskanych pacjentów.7,8 Anty-SARS-CoV{{ 14}} przeciwciała monoklonalne neutralizujące białka kolców wykazały skuteczność in-vivo zarówno w warunkach terapeutycznych, jak i profilaktycznych w modelach mysich i modelach naczelnych innych niż ludzie, przy zmniejszeniu miana wirusa i patologii płuc.9-12
Casirivimab i imdevimab to dwa niekonkurujące ze sobą ludzkie przeciwciała monoklonalne IgG1 anty-SARS-CoV-2 o wysokim powinowactwie, które wiążą się swoiście z domeną wiążącą receptor glikoproteiny wypustkowej SARS-CoV-2, blokowanie wnikania wirusa do komórek gospodarza.13 Kombinacja przeciwciał, które wiążą się z nienakładającymi się epitopami, a nie z pojedynczym przeciwciałem, ma na celu zminimalizowanie prawdopodobieństwa utraty aktywności przeciwwirusowej z powodu naturalnie krążących wariantów wirusa lub rozwoju mutantów wymykających się pod wpływem leku 14 W badaniu klinicznym z udziałem dorosłych pacjentów ambulatoryjnych z zakażeniem SARS-CoV-2 i czynnikami ryzyka ciężkiego COVID-19, skojarzenie casirivimabu i imdevimabu było dobrze tolerowane i w porównaniu z placebo zmniejszało miano wirusa w górnych drogach oddechowych, skrócił czas do ustąpienia objawów i zmniejszył złożony wynik hospitalizacji w związku z COVID-19-lub śmiertelność z jakiejkolwiek przyczyny.15,16 Wykazano również, że połączenie casirivimabu i imdevimabu zapobiega SARS -CoV{ Zakażenie {20}} u niezakażonych wcześniej osób z kontaktu w gospodarstwie domowym zakażonych osób.17 Inne produkty zawierające przeciwciała monoklonalne przeciwko kolce również wykazały działanie przeciwwirusowe i kliniczne u dorosłych pacjentów ambulatoryjnych z zakażeniem SARS-CoV-2.18,19 W USA , Amerykańska Agencja ds. Żywności i Leków wydała zezwolenie na stosowanie w nagłych wypadkach na stosowanie bamlanivimabu z etesevimabem, casirivimabem i imdevimabem oraz sotrovimabem u pacjentów ambulatoryjnych z łagodnym do umiarkowanego COVID-19.

Europejska Agencja Leków zatwierdziła połączenie casirivimabu i imdevimabu do stosowania u pacjentów z wysokim ryzykiem progresji do ciężkiego COVID-19, ale niewymagających dodatkowego tlenu. Wstępne wyniki małego badania20 casirivimabu i imdevimabu u pacjentów przyjętych do szpitala z COVID-19 wymagających tlenu o niskim przepływie były zgodne z korzyścią kliniczną u pacjentów seronegatywnych. Jednak do tej pory nie wykazano, że terapia ukierunkowana na wirusy zmniejsza śmiertelność u pacjentów przyjmowanych do szpitala z COVID-19, w przypadku których jedynymi metodami zmniejszającymi śmiertelność jak dotąd okazały się te, które modyfikują odpowiedź zapalną.21 24 Jedyne opublikowane badanie dotyczące przeciwciała monoklonalnego przeciwko kolcom (bamlaniwimabu) u pacjentów przyjętych do szpitala zostało przerwane z powodu bezskuteczności po losowym przydzieleniu 314 pacjentów do leczenia.25
Dwa inne badania cząstkowe produktów przeciwciał monoklonalnych (monoterapia sotrowimabem i BRII-196 z terapią skojarzoną BRII-198) u pacjentów przyjętych do szpitala z COVID-19 również zostały zakończone ze względu na daremność przy wielkości próby 344 i 343.26 Zgodnie z pierwszymi zasadami, odpowiedź kliniczna na terapie oparte na przeciwciałach może być największa u osób we wczesnym stadium choroby lub u tych, u których nie uzyskano skutecznejodpornyodpowiedź. Teoria ta jest poparta dowodami korzyści klinicznych we wczesnej chorobie i dowodami, że wyjściowy stan przeciwciał anty-SARS-CoV-2 może być ważnym czynnikiem prognostycznym wpływu przeciwciał monoklonalnych przeciwko kolcom na miano wirusa.15,16, 20,27 Znaczna część pacjentów z COVID-19 przyjętych do szpitala jest seronegatywna przy przyjęciu i chociaż większa część ma już wykrywalne przeciwciała anty-SARS-CoV-2, jakość ichimmunologicznyodpowiedź może być słaba, ponieważ nie zapobiegła progresji choroby.28 Jako takie, przeciwciała monoklonalne przeciwko kolcom mogą przynosić korzyści nawet w późniejszej chorobie COVID-19. W tym miejscu przedstawiamy wyniki dużego, randomizowanego, kontrolowanego badania skojarzonego casirivimabu i imdevimabu u pacjentów przyjętych do szpitala z COVID-19.

Metody
Projekt badania i uczestnicy
Badanie Randomized Evaluation of COVID Therapy (RECOVERY) jest inicjowanym przez badacza, indywidualnie randomizowanym, kontrolowanym, otwartym badaniem platformowym zaprojektowanym w celu oceny skutków potencjalnych terapii u pacjentów przyjmowanych do szpitala z COVID{{3 }}. Szczegóły projektu badania i wyniki innych możliwych terapii (deksametazon, hydroksychlorochina, lopinawir-rytonawir, azytromycyna, tocilizumab, osocze rekonwalescencyjne, kolchicyna i aspiryna) zostały opublikowane wcześniej.22,23,28-33 Badanie jest w toku w wieku 177 lat. organizacje szpitalne w Wielkiej Brytanii wspierane przez National Institute for Health Research Clinical Research Network (załącznik s. 3–27). Spośród nich 127 szpitali w Wielkiej Brytanii wzięło udział w ocenie casirivimabu i imdevimabu (Regeneron Pharmaceuticals, Tarrytown, NY, USA). Badanie było koordynowane przez sponsora badania, Departament Zdrowia Populacji Nuffield na Uniwersytecie Oksfordzkim (Oxford, Wielka Brytania).
Badanie jest prowadzone zgodnie z zasadami Międzynarodowej Konferencji w sprawie Harmonizacji – Wytyczne Dobrej Praktyki Klinicznej i zatwierdzone przez brytyjską Agencję ds. Regulacji Leków i Produktów Opieki Zdrowotnej (MHRA) oraz Komisję Etyki Badań nad Cambridge East (ref: 20/EE/0101) . Protokół i plan analizy statystycznej znajdują się w załączniku (str. 69–150) wraz z dodatkowymi informacjami dostępnymi na stronie internetowej badania. Pacjenci przyjmowani do szpitala kwalifikowali się do badania, jeśli mieli klinicznie podejrzewane lub laboratoryjnie potwierdzone zakażenie SARS-CoV-2 i nie mieli historii medycznej, która w opinii lekarza prowadzącego mogłaby narazić pacjenta na znaczne ryzyko, jeśli mieli wziąć udział w procesie. Pacjenci, którzy otrzymali dożylnieimmunoglobulinaleczenie w trakcie aktualnego przyjęcia i ważenia dzieci<40 kg="" or="" aged=""><12 years="" were="" not="" eligible="" for="" randomization="" to="" casirivimab="" and="" imdevimab.="" pregnant="" and="" breastfeeding="" women="" were="" eligible="" for="" inclusion.="" written="" informed="" consent="" was="" obtained="" from="" all="" patients,="" or="" a="" legal="" representative="" if="" they="" were="" too="" unwell="" or="" unable="" to="" provide="">
Randomizacja i maskowanie
Dane wyjściowe zostały zebrane przy użyciu internetowego formularza opisu przypadku, który zawierał informacje na temat cech demograficznych, poziomu wspomagania oddychania, głównych chorób współistniejących, przydatności leczenia badanego dla konkretnego pacjenta oraz dostępności leczenia w miejscu badania (załącznik str. 34– 36). Dane dotyczące statusu szczepień przeciwko SARS-CoV-2 zostały zebrane od 22 grudnia 2020 r.
Wyjściowa obecnośćprzeciw SARS-CoV-2przeciwciała zostały określone dla każdego uczestnika przy użyciu próbek surowicy pobranych w czasie randomizacji. Analiza została wykonana w centralnym laboratorium przy użyciu systemu OxfordTest immunologiczny(Uniwersytet Oksfordzki, Oksford, Wielka Brytania), zwalidowany 384-płytkowy pośredni test ELISA na obecność przeciwciał IgG przeciw kolce (załącznik str. 28).34 Uczestnicy zostali sklasyfikowani jako seropozytywni lub seronegatywni przy użyciu predefiniowanego progu testu z 99% lub wyższa czułość i swoistość w wykrywaniu osób z zakażeniem SARS-CoV-2 co najmniej 20 dni wcześniej.34 Analizy czułości post hoc przeprowadzono przy użyciu dostępnych na rynkutesty immunologicznedla całkowitych przeciwciał antyskokowych i antynukleokapsydowych (Roche Diagnostics, Bazylea, Szwajcaria) z progami seropozytywnymi zdefiniowanymi jako odpowiednio większe niż 0·8 i wyższe niż 0·1 (załącznik str. 28) .
Kwalifikujący się i wyrażający zgodę pacjenci zostali przydzieleni (1:1:1) do zwykłego standardu opieki, standardowego standardu opieki plus casirivimabu i imdevimabu (połączenie przeciwciał), naszego standardowego standardu opieki plus rekonwalescencyjnego osocza (do 15 stycznia 2021 r.), przy użyciu internetowej prostej (niestratyfikowanej) randomizacji z alokacją ukrytą do czasu po randomizacji (załącznik s. 32–34). Badanie nie zostało zaprojektowane w celu bezpośredniego porównania osocza po rekonwalescencji z casirivimabem i imdevimabem, a porównanie osocza po rekonwalescencji ze zwykłą opieką było już wcześniej raportowane.28 U niektórych pacjentów połączenie przeciwciał było niedostępne w szpitalu w momencie włączenia do badania lub było rozważane przez lekarza prowadzącego za zdecydowanie wskazane lub zdecydowanie przeciwwskazane.
Pacjenci ci zostali wykluczeni z randomizowanego porównania casirivimabu i imdevimabu ze standardową opieką. W ramach badania platformowego i w schemacie czynnikowym pacjenci mogli być jednocześnie losowo przydzielani do innych grup terapeutycznych: azytromycyny, kolchicyny, aspiryny lub baricytynibu w porównaniu ze zwykłą opieką. Dalsze szczegóły dotyczące tego, kiedy te czynnikowe przypisania były otwarte, znajdują się w załączniku (s. 32–34). Do 24 stycznia 2021 r. badanie umożliwiło również późniejsze losowe przypisanie pacjentom z postępującym COVID-19 (z objawami hipoksji i stanu hiperzapalnego) do tocilizumabu w porównaniu ze zwykłą opieką. Uczestnicy i lokalny personel badania nie byli maskowani do przydzielonego leczenia. Komitet sterujący badaniem, badacze i wszystkie inne osoby zaangażowane w badanie zostały zamaskowane do analizy danych dotyczących wyników podczas badania.
Procedury
Pacjenci przydzieleni do kombinacji przeciwciał mieli otrzymać pojedynczą dawkę casirivimabu 4 g i imdevimabu 4 g podawane razem w 250 ml 0,9% roztworu soli fizjologicznej we wlewie dożylnym w ciągu 60 minut (plus lub minus 15 minut) jak tylko możliwe po randomizacji. Dawka 4 g na przeciwciało została dobrana tak, aby zmaksymalizować prawdopodobieństwo efektu terapeutycznego przy jednoczesnym zapewnieniu bezpieczeństwa pacjenta, na podstawie wstępnych danych z badań szpitalnych (NCT04426695) i ambulatoryjnych (NCT04425629) dotyczących bezpieczeństwa, tolerancji i skuteczności casirivimabu i imdevimabu ( dane niepublikowane, Regeneron Pharmaceuticals). Wczesne wyniki dotyczące bezpieczeństwa były rejestrowane przez personel ośrodka za pomocą formularza online 72 godziny po randomizacji (załącznik str. 37–41).
Formularz kontrolny online został wypełniony przez personel ośrodka, gdy pacjenci zostali wypisani ze szpitala, zmarli lub 28 dni po randomizacji, w zależności od tego, co nastąpiło wcześniej (załącznik str. 42–48). Odnotowywano informacje dotyczące przestrzegania przydzielonego leczenia w ramach badania, otrzymania innego leczenia COVID-19, czasu trwania przyjęcia, otrzymania wsparcia oddechowego lub nerek oraz stanu życiowego (w tym przyczyny zgonu). Ponadto uzyskano rutynowo gromadzone dane dotyczące opieki zdrowotnej i rejestrów, w tym informacje o stanie życiowym w 28. dniu (z datą i przyczyną zgonu), wypisie ze szpitala oraz otrzymaniu wspomagania oddechowego lub terapii nerkozastępczej.
Wyniki
Wyniki oceniano po 28 dniach od randomizacji, a dalsze analizy określono po 6 miesiącach. Pierwszorzędowym wynikiem była 28-dniowa śmiertelność z jakiejkolwiek przyczyny. Drugorzędowymi punktami końcowymi był czas do wypisu ze szpitala, a u pacjentów niepoddawanych inwazyjnej wentylacji mechanicznej podczas randomizacji, złożony wynik inwazyjnej wentylacji mechanicznej (w tym pozaustrojowej oksygenacji błonowej) lub zgon. Wstępnie określone dodatkowe wyniki kliniczne obejmowały zastosowanie inwazyjnej lub nieinwazyjnej wentylacji u pacjentów niepoddawanych żadnej wentylacji w momencie randomizacji, czas do pomyślnego zaprzestania inwazyjnej wentylacji mechanicznej (definiowany jako zaprzestanie inwazyjnej wentylacji mechanicznej w ciągu, a także przeżycie, 28 dni). oraz stosowanie terapii nerkozastępczej (dializy lub hemofiltracji). Informacje na temat podejrzewanych poważnych działań niepożądanych zostały zebrane w przyspieszony sposób, aby zachować zgodność z wymogami regulacyjnymi. Szczegóły dotyczące metod stosowanych do ustalenia i uzyskania wyników znajdują się w załączniku (str. 151–71).
Wstępnie określone wyniki dotyczące bezpieczeństwa obejmowały śmiertelność specyficzną dla przyczyny, poważne zaburzenia rytmu serca oraz zdarzenia zakrzepowe i poważne krwawienia (gromadzone tylko od 6 listopada 2021 r.). Informacje o wczesnych wynikach bezpieczeństwa w 72 h po randomizacji (pogorszenie stanu oddechowego, ciężkie reakcje alergiczne, gorączka, nagłe niedociśnienie, kliniczna hemoliza i zdarzenia zakrzepowe) ustały 19 lutego 2021 r., za radą komitetu monitorującego dane badania i zgodnie z z protokołem.
Analiza statystyczna
W przypadku wszystkich wyników przeprowadziliśmy analizy intencji leczenia, porównując pacjentów losowo przydzielonych do casirivimabu i imdevimabu z pacjentami losowo przydzielonymi do zwykłej opieki, ale dla których kombinacja przeciwciał była zarówno dostępna, jak i odpowiednia jako leczenie. W przypadku pierwszorzędowego wyniku śmiertelności 28-dniowej, obserwowany log-rank minus oczekiwana statystyka i jego wariancja zostały wykorzystane do przetestowania hipotezy zerowej równych krzywych przeżycia (tj. testu log-rank) i do obliczenia jednoetapowe oszacowanie średniego współczynnika umieralności (RR). Skonstruowaliśmy krzywe przeżycia Kaplana-Meiera, aby przedstawić skumulowaną śmiertelność w ciągu 28-dniowego okresu. Zastosowaliśmy tę samą metodę do analizy czasu do wypisu ze szpitala i pomyślnego zaprzestania inwazyjnej wentylacji mechanicznej, z pacjentami, którzy zmarli w szpitalu, ocenzurowanymi w 29. dniu.
Mediana czasu do wyładowania została wyprowadzona z szacunków Kaplana-Meiera. W przypadku wcześniej określonego złożonego drugorzędowego wyniku progresji do inwazyjnej wentylacji mechanicznej lub zgonu w ciągu 28 dni (u osób, które nie otrzymały inwazyjnej wentylacji mechanicznej w momencie randomizacji) oraz dodatkowych wyników klinicznych polegających na wentylacji i zastosowaniu hemodializy lub hemofiltracji, dokładne daty nie były dostępne, więc zamiast tego oszacowano wskaźnik ryzyka. Oszacowania współczynników wskaźnika i ryzyka przedstawiono z 95-procentowym przedziałem ufności. W świetle nowych dowodów, które stały się dostępne podczas badania, postawiono hipotezę, że jakikolwiek korzystny wpływ casirivimabu i imdevimabu byłby większy wśród uczestników seronegatywnych (i może być nieistotny u uczestników seropozytywnych).20,35

W związku z tym, przed jakimkolwiek ujawnieniem wyników, komitet sterujący badania określił, że testowanie hipotez dotyczących wpływu przydziału do casirivimabu i imdevimabu na pierwszorzędowy wynik 28-śmiertelności dziennej (i drugorzędowych) będzie najpierw przeprowadzane tylko w przypadku seronegatywnych uczestnicy (tj. osoby bez wykrywalnych przeciwciał przeciwko zakażeniu SARS-CoV-2; załącznik str. 144-46). Testowanie hipotezy na temat pierwszorzędowego punktu końcowego u wszystkich losowo przydzielonych pacjentów można było przeprowadzić tylko wtedy, gdy odnotowano zmniejszenie śmiertelności u pacjentów seronegatywnych przy dwustronnej wartości p mniejszej niż 0·05. Przeprowadzone z góry porównanie wpływu przydziału do casirivimabu i imdevimabu na 28-dniową śmiertelność wśród uczestników seronegatywnych i seropozytywnych przeprowadzono przez wykonanie testu na heterogeniczność. Określono również wstępnie testy na niejednorodność lub trend zgodnie z innymi cechami wyjściowymi (wiek, płeć, pochodzenie etniczne, poziom wspomagania oddychania, dni od wystąpienia objawów i stosowanie kortykosteroidów; załącznik str. 135–36).
Pełną bazę danych prowadzi zespół badawczy, który zebrał dane z ośrodków badawczych i przeprowadził analizy w Departamencie Zdrowia Populacji Nuffield Uniwersytetu Oksfordzkiego (Oxford, Wielka Brytania).
Jak stwierdzono w protokole, nie można było oszacować odpowiednich rozmiarów próbek, gdy badanie było planowane na początku pandemii COVID{{0}}. 27 kwietnia 2021 r. komitet sterujący badania, którego członkowie nie znali wyników porównań badań, ustalił, że przy ponad 9700 pacjentach zrekrutowanych do porównania casirivimabu i imdevimabu oraz średniej dziennej rekrutacji czterech pacjentów, dalsza rekrutacja jest mało prawdopodobna. aby istotnie zwiększyć wiarygodność wyników i dlatego należy je przerwać (załącznik s. 34). Plan analizy statystycznej został sfinalizowany i opublikowany 21 maja 2021 r. (bez wiedzy o wynikach badania; załącznik s. 114–50), a rekrutacja do porównania casirivimabu i imdevimabu została zamknięta 22 maja 2021 r. Komitet sterujący badania i wszystkie inne osoby biorące udział w badaniu były maskowane do danych wynikowych aż do zakończenia rekrutacji (załącznik str. 49). Analizy przeprowadzono przy użyciu SAS w wersji 9.4 i R w wersji 4.0.3. Badanie jest zarejestrowane w ISRCTN (50189673) i ClinicalTrials.gov (NCT04381936).
Wyniki
Między 18 września 2020 r. a 22 maja 2021 r. 11 464 (47%) z 24 343 pacjentów włączonych do badania RECOVERY w jednym ze 127 uczestniczących ośrodków kwalifikowało się do losowego przypisania do casirivimabu i imdevimabu (tj. leczenie było wówczas dostępne w szpitalu, a lekarz prowadzący był zdania, że pacjent nie ma znanych wskazań ani przeciwwskazań do jego stosowania; ryc. 1). Spośród tych pacjentów 4839 zostało losowo przydzielonych do skojarzenia casirivimabu i imdevimabu, a 4946 zostało losowo przydzielonych do zwykłej opieki. Średni wiek uczestników badania w tym porównaniu wynosił 61,9 lat (SD 14,5), a mediana czasu od wystąpienia objawów wyniosła 9 dni (IQR 6–12; załącznik p 52).
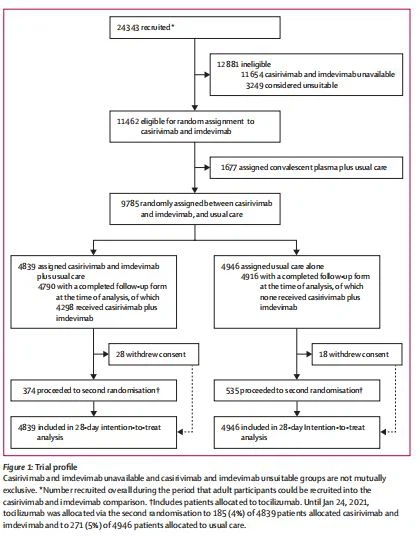
Charakterystykę pacjentów uznanych za nieodpowiednich do tego porównania zamieszczono w załączniku (s. 51). W momencie randomizacji 5272 (54%) było seropozytywnych na początku badania, 3153 (32%) było seronegatywnych, a status serologiczny był nieznany dla 1360 (14%).
Inne parametry wyjściowe, w tym przyjmowanie kortykosteroidów i wyniki testu SARS-CoV-2 PCR, przedstawiono w tabeli 1 i załączniku (str. 52). 812 (8 procent) otrzymało co najmniej jedną dawkę szczepionki SARS-CoV-2. Formularz kontrolny został wypełniony dla 4790 (99%) z 4839 pacjentów w grupie casirivimabu i imdevimabu oraz 4916 (99%) z 4946 pacjentów w grupie zwykłej opieki. Wśród pacjentów z wypełnionym formularzem kontrolnym 90% przypisanych do casirivimabu i imdevimabu otrzymywało casirivimab i imdevimab; żaden z pacjentów przydzielonych do zwykłej opieki nie otrzymywał casirivimabu i imdevimabu (ryc. 1; załącznik str. 53). Stosowanie innych metod leczenia COVID-19 było podobne wśród pacjentów, którym przydzielono casirivimab i imdevimab oraz wśród pacjentów, którym przydzielono zwykłą opiekę, przy czym około 25% otrzymywało ponowne dostarczenie, a około 15% otrzymywało tocilizumab lub sarilumab (załącznik p 53).
Dane dotyczące pierwszorzędowych i drugorzędowych wyników są znane dla ponad 99 procent losowo przydzielonych pacjentów. U pacjentów, o których wiadomo było, że byli seronegatywni na początku leczenia, przydział do casirivimabu i imdevimabu wiązał się ze znaczącym zmniejszeniem pierwszorzędowego punktu końcowego śmiertelności 28-dniowej w porównaniu ze zwykłą opieką: 396 (24%) z 1633 pacjentów w W grupie casirivimabu i imdevimabu zmarło 452 (30 procent) ze 1520 pacjentów w grupie zwykłej opieki (RR 0·79, 95% CI 0,69–0,91; p=0·0009; tabela 2, rysunek 2, rysunek 3).
Proporcjonalny wpływ casirivimabu i imdevimabu na śmiertelność różnił się istotnie między pacjentami seropozytywnymi i seronegatywnymi (test na niejednorodność p{{{{10}}}·002; ryc. 3). Wśród wszystkich losowo przydzielonych pacjentów (w tym tych z ujemnym, dodatnim lub nieznanym wyjściowym stanem przeciwciał) nie było znaczącej różnicy w pierwszorzędowym wyniku 28-dniowej śmiertelności między casirivimabem i imdevimabem w porównaniu do zwykłych grup leczenia: 943 ( 19 procent) z 4839 pacjentów w grupie casirivimabu i imdevimabu zmarło w porównaniu z 1029 (21 procent) z 4946 pacjentów w grupie zwykłej opieki (RR 0,94, 95% CI 086–1,02; p{ {17}}·14; ryc. 2, ryc. 3, załącznik s. 54). Podobne wyniki odnotowano w analizach wrażliwości post-hoc przy użyciu komercyjnego testu immunologicznego w celu określenia statusu serologicznego anty-S lub anty-N (załącznik str. 62–63).

In seronegative patients, the proportional effects of casirivimab and imdevimab on mortality were consistent across all other pre-specified subgroups (figure 4), including by the level of respiratory support received at randomization (test for trend p=0·55; figure 4) and, in a post-hoc exploratory analysis, by use of redelivering at baseline (test for heterogeneity p=0·36; appendix p 64), and by baseline C-reactive protein concentration divided into thirds (test for trend p=0·22). Likewise, among all randomly assigned patients combined (ie, irrespective of serostatus), there was similar consistency across subgroups (appendix p 65). Results were also similar when restricted to participants with a positive SARS-CoV-2 PCR test (appendix p 55). In a sensitivity analysis using a Cox model adjusted for all pre-specified subgroups, allocation to casirivimab and imdevimab was associated with a mortality RR of 0·85 (95% CI 0·74–0·97) in seronegative patients (appendix p 55). In all participants, there was no evidence that the effect of casirivimab and imdevimab on mortality varied depending on concurrent randomized allocation to azithromycin, colchicine, or aspirin (all interaction p values >0·11).

In seronegative patients, discharge alive within 28 days was more common for those assigned to casirivimab and imdevimab than those assigned to usual care (table 2, figure 3, appendix p 66). However, there was no meaningful between-group difference in the overall study population for this outcome (median 10 days [IQR 6 to >28] vs 10 days [5 to >28]; rysunek 3, załącznik str. 54). U seronegatywnych pacjentów, którzy nie stosowali inwazyjnej wentylacji mechanicznej na początku badania, stosowanie casirivimabu i imdevimabu wiązało się z mniejszym ryzykiem progresji do złożonego wtórnego punktu końcowego inwazyjnej wentylacji mechanicznej lub zgonu (tabela 2, ryc. 3). Nie było jednak różnicy między grupami w całej badanej populacji (ryc. 3, załącznik str. 54).
Proporcjonalny wpływ casirivimabu i imdevimabu na drugorzędowe wyniki wypisu żyjącego ze szpitala i inwazyjnej wentylacji mechanicznej lub zgonu różnił się istotnie między pacjentami seropozytywnymi i seronegatywnymi (wartość p dla heterogeniczności dla obu<0·001; figure="" 3).="" in="" all="" participants="" (irrespective="" of="" baseline="" serostatus),="" there="" was="" no="" evidence="" of="" differences="" in="" secondary="" outcomes="" in="" prespecified="" subgroups="" of="" patients="" (appendix="" pp="" 67–68).="" in="" patients="" who="" were="" not="" on="" ventilation="" at="" baseline,="" casirivimab="" and="" imdevimab="" were="" associated="" with="" less="" frequent="" progression="" to="" use="" of="" ventilation="" than="" usual="" care="" in="" those="" who="" were="" seronegative="" (table="" 2)="" but="" not="" in="" the="" overall="" study="" population="" (appendix="" p="">

Nie było znaczących różnic w progresji do terapii nerkozastępczej, śmiertelności poza COVID, zaburzeniach rytmu serca, zakrzepicy lub poważnych krwawieniach zarówno w populacji seronegatywnej, jak i ogólnej (tab. 2, załącznik str. 56–58). Informacje o potencjalnych reakcjach na wlew, które wystąpiły w ciągu pierwszych 72 godzin po randomizacji, zebrano dla 1792 pacjentów w grupie casirivimabu i imdevimabu oraz 1715 pacjentów w grupie zwykłej opieki (przed zatrzymaniem zbierania tych danych 19 lutego 2021 r.). W całej badanej populacji zgłoszona częstość występowania gorączki (u 79 [4%] z 1792 vs. 52 [3%] z 1715), nagłego niedociśnienia (66 [4%] vs 39 [2%]) oraz zdarzeń zakrzepowych ( 31 [2 procent] vs 24 [1 procent]) było liczbowo wyższe w grupie casirivimabu i imdevimabu w porównaniu do zwykłej grupy opieki, a częstotliwość nagłego pogorszenia stanu oddechowego (369 [21 procent] vs 372 [22 procent]) i hemoliza kliniczna (26 [1 procent] vs 31 [2 procent]) była liczbowo niższa (załącznik p 59).

Było siedem raportów (<1% of="" participants)="" of="" a="" serious="" adverse="" reaction="" believed="" to="" be="" related="" to="" treatment="" with="" the="" combination="" of="" casirivimab="" and="" imdevimab="" (three="" allergic="" reactions,="" two="" seizures,="" one="" acute="" desaturation,="" and="" one="" transient="" loss="" of="" consciousness;="" appendix="" p="" 60),="" and="" no="" deaths="" attributed="" to="" the="">
Dyskusja
W tym dużym, randomizowanym badaniu skojarzono casirivimab i imdevimab przeciwciała u pacjentów z ujemnym wynikiem przeciwciał przeciwko SARS-CoV-2 (tj.odpornyodpowiedzi) znacząco zmniejszył 28-śmiertelność w ciągu dnia o około jedną piątą w porównaniu ze zwykłą opieką, co daje bezwzględną korzyść w postaci sześciu mniej zgonów na 100 pacjentów, którym przydzielono leczenie. Ponadto stosowanie casirivimabu i imdevimabu wiązało się ze zwiększoną częstością wypisów ze szpitala żyjących w ciągu pierwszych 28 dni i zmniejszoną częstością progresji do inwazyjnej wentylacji mechanicznej lub zgonu u tych pacjentów. W przeciwieństwie do tego, nie zaobserwowano takich korzyści u pacjentów, u których podczas randomizacji stwierdzono obecność przeciwciał anty-SARS-CoV-2.
W związku z tym, gdy wszyscy pacjenci byli rozpatrywani łącznie (w tym ci o nieznanym statusie przeciwciał), casirivimab i imdevimab wiązały się z nieistotnymi różnicami w wynikach klinicznych. Randomizowane badania kliniczne trzech preparatów neutralizujących przeciwciał monoklonalnych (LY-CoV555, sotrowimab i BRII-196 z BRII-198) u pacjentów przyjętych do szpitala z powodu COVID-19 zostały przedwcześnie zakończone na podstawie tymczasowe analizy daremności.25,26

Chociaż istniały pewne dowody na potencjalną niejednorodność wpływu BRII-196 z BRII-198 w odniesieniu do wyjściowego stanu serologicznego, żadna z tych trzech ocen nie była w stanie wykryć umiarkowanych skutków leczenia w podgrupach zdefiniowanych na podstawie wyjściowego stanu serologicznego. Całkowita liczba pacjentów włączonych do tych trzech badań wyniosła 860, mniej niż 10 procent liczby pacjentów włączonych do oceny RECOVERY casirivimabu i imdevimabu.
Opierając się na naszych odkryciach, jakiekolwiek terapeutyczne zastosowanie casirivimabu i imdevimabu w warunkach szpitalnych najlepiej byłoby ograniczyć do pacjentów seronegatywnych, co zostało obecnie wdrożone w Wielkiej Brytanii na podstawie naszych wyników.36 Podejście to wymaga wykonania testów serologicznych przed podaniem leku. Wysokowydajne, komercyjne testy laboratoryjne na obecność przeciwciał anty-SARS-CoV-2 są dostępne i stosowane w placówkach opieki zdrowotnej o wysokich dochodach. Na przykład, odnotowaliśmy podobne wyniki, gdy analizy pierwszorzędowych i drugorzędowych wyników zostały powtórzone przy użyciu dostępnego w handlu testu na przeciwciała anty-kolcowe lub antynukleokapsydowe.
Jednak testy serologiczne nie są powszechnie dostępne w placówkach o niższych dochodach.37 Opracowano przyłóżkowe testy immunologiczne z przepływem bocznym, ale niektóre mają nieoptymalne wyniki i ich przydatność do podejmowania decyzji terapeutycznych, w przeciwieństwie do badań seroepidemiologicznych, wymaga dalszej oceny. 34,38,39 Opracowano testy o niższych kosztach i wymaganiach technologicznych niż komercyjne systemy laboratoryjne i lepszej wydajności niż testy immunologiczne z przepływem bocznym, które mogą oferować bardziej skalowalne i przystępne opcje oceny stanu serologicznego, ale wymagają one również dalszej oceny przed zastosowaniem klinicznym. 40 Badanie to przeprowadzono głównie w okresie przed powszechnym stosowaniem szczepionek SARS-CoV-2, kiedy stan serologiczny (obecność przeciwciał przeciwko wirusowemu białku wypustek) odzwierciedlał ostrą reakcję na zakażenie. Teraz jednak status seropozytywny może dodatkowo odzwierciedlać odpowiedź na poprzednie szczepienie SARS-CoV-2, a nie ostrą infekcję. Odpowiedź przeciwciał indukowana przez szczepionkę może być ilościowo i jakościowo różna od odpowiedzi przeciwciał indukowanej przez wirusy.
Chociaż strategie testów serologicznych, takie jak testowanie przeciwciał zarówno przeciwko białkom wypustek, jak i nukleokapsydowi, mogą pomóc w rozróżnieniu między odpowiedziami przeciwciał wywołanymi szczepionką a ostrą wywołaną przez wirusy, nie wiadomo, czy leczenie casirivimabem i imdevimabem byłoby korzystne u zaszczepionych pacjentów z COVID -19 którzy są dodatnimi przeciwciałami S, ale ujemnymi przeciwciałami N. Wiarygodność statusu seropozytywnego jako predyktora braku odpowiedzi terapeutycznej na przeciwciała monoklonalne jest dodatkowo komplikowana przez pojawienie się wariantu B.1.1.529 (omikron), który może unikać przeciwciał przeciwko wcześniejszym wariantom SARS-CoV-2. W przyszłości status antygenu może być bardziej znaczącym biomarkerem potencjalnej odpowiedzi terapeutycznej na przeciwciała monoklonalne niż status przeciwciał.26

W październiku 2020 r. niezależna komisja monitorująca dane sponsorowanego przez przemysł badania41 casirivimabu i imdevimabu u pacjentów z COVID-19 przyjętych do szpitala zaleciła zawieszenie rekrutacji pacjentów leczonych tlenem wysokoprzepływowym lub wentylacją mechaniczną z powodu potencjalnego sygnał bezpieczeństwa, podczas gdy analiza pośrednia tego samego badania z grudnia 2020 r. sugerowała możliwą korzyść u pacjentów otrzymujących tlen o niskim przepływie. 20 Nie zaobserwowaliśmy jednak żadnych dowodów na to, że proporcjonalny wpływ casirivimabu i imdevimabu na śmiertelność różnił się w zależności od poziomu wsparcie oddechowe otrzymane podczas randomizacji, albo oceniane u wszystkich uczestników, albo oceniane tylko w podgrupie uczestników seronegatywnych.
Przeciwciała monoklonalne są podatne na ewolucję oporności wirusa, jeśli substytucje w docelowym epitopie zmniejszają lub znoszą wiązanie przeciwciał, a amerykańskie zezwolenie na stosowanie w sytuacjach nadzwyczajnych dla monoterapii przeciwciałem monoklonalnym LY-CoV555 zostało cofnięte z powodu oporności kilku głównych wariantów wirusa.42 ryzyko można zmniejszyć, stosując kombinację przeciwciał monoklonalnych, które wiążą się z nienakładającymi się epitopami.14 Chociaż w tym badaniu nie badaliśmy pojawiania się wariantów oporności, główne warianty krążące w Wielkiej Brytanii przez całe badanie, w tym B.1.1 Wariant .7 (alfa), który był wariantem dominującym w Wielkiej Brytanii od grudnia 2020 r. do kwietnia 2021 r., pozostał wrażliwy na casirivimab i imdevimab.43-46
Chociaż mutacje glikoproteiny kolców w reszcie E484 glikoproteiny kolców w niektórych wariantach (np. B.1.351 [beta, E484K] i B.1.617.1 [kappa, E484Q]) są związane ze znacznym zmniejszeniem aktywności neutralizacyjnej casirivimabu, połączenie casirivimabu z imdevimabem zachowuje siłę działania wobec tych wariantów ze względu na hamujące działanie imdevimabu.43-45,47 Chociaż wariant B.1.617.2 (delta) wiąże się ze znacznie zmniejszoną aktywnością neutralizującą imdevimabu, neutralizująca aktywność casirivimabu jest zachowany, tak że połączenie prawdopodobnie zachowa skuteczność kliniczną wobec wariantu delta.46,48 Pod koniec 2021 r., po zakończeniu badania casirivimabu i imdevimabu, pojawiła się omikronowa odmiana SARS-CoV-2. Dzięki licznym podstawieniom aminokwasów w glikoproteinie kolców, omicron jest w stanie uniknąć neutralizacji przez niektóre naturalnie występujące przeciwciała monoklonalne, wywołane szczepionką.
Zarówno casirivimab, jak i imdevimab mają znacznie zmniejszoną zdolność do neutralizacji omikronu in vitro i dlatego jest mało prawdopodobne, aby zachowały skuteczność kliniczną przeciwko wariantowi omikronu. Jednak to badanie jest dowodem na to, że terapia przeciwciałami monoklonalnymi może przynieść korzyści kliniczne u hospitalizowanych pacjentów z COVID-19. Pojawienie się wariantu omikronu podkreśla znaczenie ciągłego monitorowania oporności, ciągłego rozwoju i oceny preparatów przeciwciał monoklonalnych, które nie są wrażliwe na powszechne i nowo powstające substytucje, oraz badania przeciwwirusowych terapii skojarzonych o różnych mechanizmach działania.
Mocne strony tego badania obejmowały to, że było ono randomizowane, miało dużą wielkość próby, szerokie kryteria kwalifikacyjne, a ponad 99 procent pacjentów było obserwowanych w celu uzyskania pierwszorzędowego punktu końcowego. Badanie ma pewne ograniczenia: nie zebrano informacji na temat wyników wirusologicznych, ani informacji na temat wyników radiologicznych lub fizjologicznych. Chociaż to randomizowane badanie ma charakter otwarty (tj. uczestnicy i personel lokalnego szpitala są świadomi przydzielonego leczenia), wyniki są jednoznaczne i zostały ustalone bez uprzedzeń poprzez powiązanie z rutynową dokumentacją medyczną.
Dawki casirivimabu i imdevimabu zastosowane w tym badaniu były wysokie w porównaniu z dawkami stosowanymi w badaniach ambulatoryjnych; zrozumienie skutków niższych dawek wymagałoby dodatkowych dowodów z randomizowanego, kontrolowanego badania.16 Podsumowując, to duże, randomizowane badanie dostarcza pierwszych dowodów na to, że terapia przeciwwirusowa może zmniejszyć śmiertelność pacjentów przyjmowanych do szpitali z COVID-19. Wyniki potwierdzają zastosowanie kombinacji casirivimabu i imdevimabu z monoklonalnym przeciwciałem neutralizującym u pacjentów seronegatywnych przyjętych do szpitala z COVID-19 spowodowanym przez warianty SARS-CoV-2, które są wrażliwe na te przeciwciała.
Odniesienie
1 Laustsen AH. Jak można wykorzystać przeciwciała monoklonalne przeciwko zaniedbanym chorobom tropikalnym i innym chorobom zakaźnym? Ekspert Opin Drug Discov 2019; 14: 1103–12.
2 Mulangu S, Dodd LE, Davey RT Jr, et al. Randomizowana, kontrolowana próba leków przeciwko wirusowi Ebola. N Engl J Med 2019; 381: 2293-303.
3 Paliwizumab, humanizowane przeciwciało monoklonalne przeciwko syncytialnemu wirusowi oddechowemu, zmniejsza liczbę hospitalizacji z powodu infekcji wirusem syncytium nabłonka oddechowego u niemowląt wysokiego ryzyka. Pediatria 1998; 102: 531–37.
4 Winkler ES, Gilchuk P, Yu J, et al. Ludzkie przeciwciała neutralizujące przeciwko SARS-CoV-2 wymagają nienaruszonych funkcji efektorowych Fc dla optymalnej ochrony terapeutycznej. Komórka 2021; 184: 1804-20. Więcej informacji na temat RECOVERY, wersja próbna, zobacz https://www.recoverytrial.net
5 Walls AC, Park YJ, Tortorici MA, Wall A, McGuire AT, Veesler D. Struktura, funkcja i antygenowość glikoproteiny szczytowej SARS-CoV-2. Komórka 2020; 181: 281-92.
6 Ju B, Zhang Q, Ge J, et al. Ludzkie przeciwciała neutralizujące wywołane przez zakażenie SARS-CoV-2. Natura 2020; 584: 115-19.
7 Wang C, Li W, Drabek D, et al. Ludzkie przeciwciało monoklonalne blokujące zakażenie SARS-CoV-2. Nat Commun 2020; 11:2251.
8 Pinto D, Park YJ, Beltramello M, et al. Krzyżowa neutralizacja SARS-CoV-2 przez ludzkie przeciwciało monoklonalne SARS-CoV. Natura 2020; 583: 290–95.
9 Zost SJ, Gilchuk P, sprawa JB, et al. Silnie neutralizujące i ochronne ludzkie przeciwciała przeciwko SARS-CoV-2. Natura 2020; 584: 443–49.
10 Shi R, Shan C, Duan X, et al. Ludzkie przeciwciało neutralizujące celuje w miejsce wiązania receptora SARS-CoV-2. Natura 2020; 584: 120-24.
11 Cao Y, Su B, Guo X i in. Silne przeciwciała neutralizujące przeciwko SARS-CoV-2 zidentyfikowane przez wysokoprzepustowe sekwencjonowanie pojedynczych komórek limfocytów B pacjentów rekonwalescencyjnych. Komórka 2020; 182: 73–84.
12 Baum A, Ajithdoss D, Copin R, et al. Przeciwciała REGN-COV2 zapobiegają i leczą zakażenie SARS-CoV-2 u makaków rezus i chomików. Nauka 2020; 370: 1110–15.
13 Hansen J, Baum A, Pascal KE, i in. Badania na humanizowanych myszach i ludziach po rekonwalescencji dają koktajl przeciwciał SARS-CoV-2. Nauka 2020; 369: 1010–14.
14 Baum A, Fulton BO, Włoga E i in. Koktajl przeciwciał do białka szczytowego SARS-CoV-2 zapobiega szybkiej ucieczce mutacyjnej obserwowanej w przypadku poszczególnych przeciwciał. Nauka 2020; 369: 1014-18.
15 Weinreich DM, Sivapalasingam S, Norton T, et al. REGN-COV2, koktajl przeciwciał neutralizujących, u pacjentów ambulatoryjnych z COVID-19. N Engl J Med 2021; 384: 238–51.
16 Weinreich DM, Sivapalasingam S, Norton T, et al. Połączenie przeciwciał REGEN-COV i wyniki leczenia ambulatoryjnego z COVID-19. N Engl J Med 2021; 385: e81.
17 O'Brien poseł, Forleo-Neto E, Musser BJ, et al. Podskórne połączenie przeciwciał REGEN-COV w celu zapobiegania COVID-19. N Engl J Med 2021; 385: 1184–95.
18 Gottlieb RL, Nirula A, Chen P, et al. Wpływ bamlanivimabu w monoterapii lub w skojarzeniu z etesevimabem na miano wirusa u pacjentów z COVID o nasileniu łagodnym do umiarkowanego-19: randomizowane badanie kliniczne. JAMA 2021; 325: 632–44.
19 Chen P, Nirula A, Heller B i in. SARS-CoV-2 neutralizujące przeciwciało LY-CoV555 u pacjentów ambulatoryjnych z COVID-19. N Engl J Med 2021; 384: 229–37.
20 Regeneracja. Komunikat prasowy: Firma Regeneron ogłasza zachęcające wstępne dane z badania koktajlu przeciwciał przeciw krowim -19 u hospitalizowanych pacjentów stosujących tlen o niskim przepływie. 2020.
21 Beigel JH, Tomashek KM, Dodd LE i in. Remdesivir w leczeniu COVID-19 — raport końcowy. N Engl J Med 2020; 383: 1813-26.
22 RECOVERY Collaborative Group, Horby P, Lim WS, et al. Deksametazon u hospitalizowanych pacjentów z COVID-19. N Engl J Med 2021; 384: 693–704.
23 Grupa Współpracy ODZYSKIWANIA. Tocilizumab u pacjentów przyjętych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet 2021; 397: 1637-45.
24 Grupa Robocza ds. Szybkiej Oceny Dowodów WHO na temat terapii COVID-19, Sterne JAC, Murthy S, et al. Związek między podawaniem ogólnoustrojowych kortykosteroidów a śmiertelnością wśród pacjentów w stanie krytycznym z COVID-19: metaanaliza. JAMA 2020; 324: 1330–41.
25 Grupa badawcza ACTIV-3/Leczenie pacjentów hospitalizowanych z powodu COVID-19 (TICO) Ly-CoV555. Neutralizujące przeciwciało monoklonalne dla hospitalizowanych pacjentów z COVID-19. N Engl J Med 2021; 384: 905-14.
26 Grupa badawcza ACTIV-3/Leczenie pacjentów hospitalizowanych z powodu COVID-19 (TICO). Skuteczność i bezpieczeństwo dwóch terapii neutralizujących przeciwciałami monoklonalnymi, sotrovimab i BRII-196 plus BRII-198, u dorosłych hospitalizowanych z powodu COVID-19 (TICO): randomizowane badanie z grupą kontrolną. Lancet Infect Dis 2021; opublikowane online 23 grudnia.
27 Weisblum Y, Schmidt F, Zhang F i in. Ucieczka przed przeciwciałami neutralizującymi przez warianty białka wypustek SARS-CoV-2. Życie 2020; 9: e61312.
28 Grupa współpracy ODZYSKIWANIE. Osocze po rekonwalescencji u pacjentów przyjętych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet 2021; 397: 2049–59.
29 Odzyskiwanie Grupy Współpracy. Lopinawir-rytonawir u pacjentów przyjętych do szpitala z COVID-19 (RECOVERY): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet 2020; 396: 1345–52.
30 Odzyskiwanie Grupy Współpracy. Wpływ hydroksychlorochiny na hospitalizowanych pacjentów z COVID-19. N Engl J Med 2020; 383: 2030–40.
31 Odzyskiwanie Grupy Współpracy. Azytromycyna u pacjentów przyjętych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet 2021; 397: 605–12.
32 Odzyskiwanie Grupy Współpracy. Kolchicyna u pacjentów przyjętych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet Respir Med 2021; 9:1419–26.
33 Odzyskiwanie Grupy Współpracy. Aspiryna u pacjentów przyjętych do szpitala z COVID-19 (ODZYSKIWANIE): randomizowane, kontrolowane, otwarte badanie platformowe. Lancet 2021; opublikowane online 17 listopada.
34 Krajowa Grupa Oceny Testów Serologicznych SARS-CoV. Charakterystyka wydajności pięciu testów immunologicznych na SARS-CoV-2: bezpośrednie porównanie benchmarków. Lancet Infect Dis 2020; 20: 1390–400.
35 Weinreich DM, Sivapalasingam S, Norton T, et al. REGN-COV2, koktajl przeciwciał neutralizujących, u pacjentów ambulatoryjnych z COVID-19. N Engl J Med 2021; 384: 238–51.
36 Agencja Regulacyjna ds. Leków i Produktów Opieki Zdrowotnej. Polityka tymczasowego zlecania badań klinicznych: casirivimab i imdevimab dla pacjentów hospitalizowanych z powodu COVID-19. 2021.
37 Amerykańska Agencja ds. Żywności i Leków. Wydajność testów serologicznych autoryzowanych przez EUA. 2021.
38 Moshe M, Daunt A, Kwiat B i in. Testy SARS-CoV-2 przepływu bocznego do ewentualnego wykorzystania w krajowych badaniach seroprewalencji -19 kruków (Reakcja 2): badanie dokładności diagnostycznej. BMJ 2021; 372: n423.
39 ER Adams, M. Ainsworth, R. Anand i in. Testowanie przeciwciał na COVID-19: raport Krajowego Naukowego Panelu Doradczego ds. COVID. Witamy Otwarte Res 2020; 5: 139.
40 Townsend A, Rijal P, Xiao J, et al. Test hemaglutynacji do szybkiego wykrywania przeciwciał przeciwko SARS-CoV-2. Społeczność Nat 2021; 12:1951.
41 Regeneracja. Niezależna komisja monitorowania danych Regn-CoV2 zaleca prowadzenie rekrutacji hospitalizowanych pacjentów z wysokim zapotrzebowaniem na tlen i kontynuację rekrutacji pacjentów z niskim zapotrzebowaniem na tlen lub bez niego. 2020.
42 Amerykańska Agencja ds. Żywności i Leków. List odwołujący bamlanivimab 04162021. 2021.
43 Wang P, Nair MS, Liu L i in. Odporność na przeciwciała wariantów SARS-CoV-2 B.1.351 i B.1.1.7. Przyroda 2021; 593: 130–35.
44 Chen RE, Winkler ES, sprawa JB, et al. Skuteczność przeciwciał monoklonalnych in vivo przeciwko szczepom wariantowym SARS-CoV-2. Przyroda 2021; 596: 103-08.
45 Widera M, Wilhelm A, Hoehl S, et al. Ograniczona neutralizacja autentycznych wariantów koronawirusa 2 zespołu ostrej ostrej niewydolności oddechowej niosących E484K in vitro. J Infect Dis 2021; 224: 1109–14.
46 Wilhelm A, Toptan T, Pallas C, et al. Neutralizacja za pośrednictwem przeciwciał autentycznych wariantów SARS-CoV-2 B.1.617 niosących L452R i T478K/E484Q. Wirusy 2021; 13:1693.
47 Hoffmann M, Hofmann-Winkler H, Kruger N, et al. SARS-CoV-2 wariant B.1.617 jest oporny na bamlanivimab i unika przeciwciał indukowanych przez zakażenie i szczepienie. Rep. komórki 2021; 36: 109415.
48 Mlcochova P, Kemp SA, Dhar MS, et al. SARS-CoV-2 B.1.617.2 replikacja wariantu delta iodpornyuchylanie się. Przyroda 2021; 599: 114-19.
49 Starr TN, Greaney AJ, Addetia A, et al. Prospektywne mapowanie mutacji wirusowych, które wymykają się przeciwciałom stosowanym w leczeniu COVID-19. Nauka 2021; 371: 850–54.

