Część 3: Dopasowana funkcjonalizacja naturalnych fenoli w celu poprawy aktywności biologicznej
Mar 28, 2022
Po więcej informacji. kontakttina.xiang@wecistanche.com
5. Fenole lipidowe
Lipidowyfenole(lub lipidy fenolowe, zwane również fenolipidami) to fenole podstawione łańcuchami lipofilowymi, które nadają cząsteczce cechy amfifilowe. Ważnym lipidem fenolowym jest -tokoferol[330]; jednak sam ten związek zasługuje na recenzję, więc nie został uwzględniony.
Przez długi czas nie doceniano znaczenia naturalnych fenoli lipidowych [331]. Jednak ich doskonałaprzeciwutleniacz, właściwości antygenotoksyczne i cytostatyczne są obecnie ustalone [332], wraz z ich bioaktywnością w wpływaniu na szlaki biologiczne zaangażowane wChoroba Alzheimerapatogeneza 333]. Doniesiono również o działaniu przeciwzapalnym i przeciwzapalnym dla fenoli lipidowych wyekstrahowanych z orzecha nerkowca (Anacardium occidentale) [334].
Ze względu na znaczenie takiej klasy związków, w ostatnich dziesięcioleciach zaproponowano kilka syntetycznych fenoli lipidowych w celu dalszego rozszerzenia ich zastosowań biologicznych.

Kliknij tutaj, aby dowiedzieć się więcej o produktach
5.1. Biokatalizowane syntezy fenoli lipidowych
Lipazy są enzymami z wyboru do przeprowadzania reakcji transestryfikacji w celu uzyskania zmodyfikowanych lub syntetycznych lipidów o zastosowaniach funkcjonalnych lub farmaceutycznych [335, 336]. Wytworzono dużą liczbę estrów katecholu i kwasów tłuszczowych do mieszania zawiesiny katecholu w estrze etylowym kwasu tłuszczowego [337].
Półsyntetyczne fenole lipidowe wytworzono w reakcjach transestryfikacji kwasów fenolowych z olejem lnianym [338,339], oleiną [340], olejem z wątroby ryb [341] i olejem z kryla [342]. Reakcje prowadzone w rozpuszczalnikach organicznych lub w układzie bezrozpuszczalnikowym [343,344] były katalizowane przez Novozym 435 wyizolowany przez Candida Antarctica (Schemat 33).

W ostatnim czasie wydajność poprawiła się przy użyciu dwutlenku węgla w stanie nadkrytycznym jako ośrodka reakcji [345]. Przygotowane mieszaniny fenoli lipidowych badano pod kątem aktywności przeciwutleniającej. Uzyskana aktywność zmiatania rodników wahała się od umiarkowanej do dobrej, ale zawsze była niższa niż w przypadku -tokoferolu. Ponadto otrzymanych z mieszanin wyników nie można było przypisać jednemu związkowi.
Odwrotnie, czyste lipidy fenolowe kwasów tłuszczowych o różnej długości łańcucha wytworzono z kwasem ferulowym [346]. Synteza obejmowała etap biokatalizacji (przez Nosozyme) (Schemat 34).
Theaktywność antyoksydacyjnabadanie dało mieszane wyniki, ponieważ test zmiatania rodników nie wykazał poprawy w stosunku do kwasu ferulowego, podczas gdy samoutlenianie kwasu linolowego w układzie micelarnym wykazało pewną poprawę, przypisywaną zwiększonej rozpuszczalności.

Doniesiono o syntezie chemoenzymatycznej fosfatydylocholiny zawierającej kwas fenolowy i kwasy tłuszczowe [347], z jedną z aktywnych pochodnych, 1-(4-hydroksy-3,5-dimetoksy) cynamoilo-2-acylo-sn-glicerol-3-fosfocholina, wykazująca doskonałe działanie przeciwutleniające.
Innym podejściem było otrzymanie fenoli lipidowych z fenolu i wolnych kwasów tłuszczowych lub odpowiednich estrów, z unieruchomioną lipazą z Candida Antarctica jako biokatalizatorem [348]. Aktywność antyoksydacyjna tyrosolu wzrosła po acylacji, ale nie stwierdzono korelacji z liczbą wiązań podwójnych w tłuszczowej grupie acylowej (Schemat 35).

Niektóre estry zsyntetyzowano z naturalnych fenoli i kwasu liponowego w reakcji katalizowanej przez Novozym 435 (unieruchomiona lipaza B z Candida Antarctica) w mieszaninie butanon-heksan [349]. Aktywność przeciwutleniającą określono nie tylko w teście wymiatania rodników, ale także przez pomiar hamowania utleniania w emulsji oleju z tuńczyka. Ester 2-(3,4-dihydroksyfenylo)-5-(1,2-ditiolan-3-ylo)pentanian, otrzymany z tyrozolu i kwasu -liponowego, przez hydroksylację aromatyczną (Scheme 36), wykazał w obu testach doskonałą aktywność przeciwutleniającą i zdaniem autorów może być stosowany jako prolek, ponieważ po hydrolizie uwalnia związki nietoksyczne, a nawet zdrowe.

Później odkryto, że 2-ester metylowy kwasu S-lipoilo-kafeinowego był inhibitorem tyrozynazy z ludzkich komórek czerniaka [350].
Cel, jakim było przygotowanie pojedynczego fenolu lipidowego, unikając kłopotliwego rozdzielania skomplikowanej mieszaniny, został osiągnięty dzięki wieloetapowej strategii obejmującej zarówno katalizę chemiczną, jak i enzymatyczną. Unieruchomioną lipazę z Candida Antarctica (CAL-B) zastosowano w podłożu organicznym [351] (Schemat 37).
![Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol](/Content/uploads/2022842169/20220328111325cc1b5fb0d7394a028caf7ce4b3cdd52d.png)
Po scharakteryzowaniu przygotowany 1-[11-(ferulyloksy)undekanoilo)glicerol poddano badaniom przeciwbakteryjnym, przeciwutleniającym i cytotoksycznym. Aktywność przeciwdrobnoustrojowa była umiarkowana, aktywność przeciwutleniająca była doskonała, a aktywność przeciwko niektórym liniom komórek nowotworowych była obiecująca, więc autorzy przewidzieli potencjalne zastosowania kosmetyczne i biomedyczne.
Przeprowadzono reakcję transestryfikacji z użyciem lipazy B Candida Antarctica, traktując kwas 4-hydroksyfenylooctowy trioleiną oraz olejem rybim, uzyskując syntetyczne substancje o działaniu zarówno przeciwutleniającym, jak i przeciwbakteryjnym [352].
5.2. Syntezy chemiczne fenoli lipidowych
Fenole lipidowe wytworzono jako estry, albo z fenoli z długołańcuchowymi kwasami karboksylowymi, albo z kwasów fenolowych. Wybrane przykłady syntetycznych fenoli lipidowych przedstawiono w Tabeli 1.

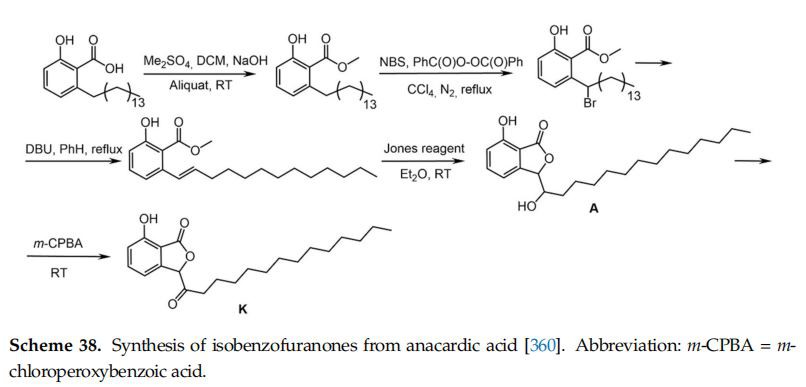
Kwas anacardowy ze świeżych i suchych orzechów nerkowca Anacardium occidentale został przekształcony w izobenzofuranony, jak pokazano na schemacie 38, z grupą funkcyjną alkoholu (A) lub keto (K) w długim łańcuchu [360].
Zarówno izobenzofuranony A i K, jak i prekursor acykliczny, były umiarkowanie lub znacząco aktywne w badaniach przesiewowych cytotoksyczności z różnymi ludzkimi liniami komórek nowotworowych.
Zaobserwowano dobrą zdolność przeciwutleniającą do stabilizacji oliwy z oliwek w przypadku rodziny estrów fenolowych kwasów tłuszczowych, wytworzonych z alkoholu 3,4-dihydroksybenzoilowego (alkoholu protokatechowego) lub hydroksytyrozolu i kwasów tłuszczowych. Reakcję przeprowadzono w bezwodnym THF, w obecności karbodiimidu i DMAP[361]. Wszystkie dwadzieścia związków zbadano jako potencjalne przeciwutleniacze w rafinowanej oliwie z oliwek. Wydaje się, że na aktywność ma wpływ długość łańcucha alkilowego przyłączonego do pierścienia fenylowego.
Po odkryciu, że 5-alkilo- i 5-alkilorezorcynole, wyizolowane z grzybowych wcieleń Meruliusa, hamują oporny na metycylinę Staphylococcus aureus [362], konieczna była dobra metoda syntetyczna, ponieważ nie są one łatwo dostępne dostępne, ale są ważne dla badań analitycznych, metabolicznych i bioaktywności. Opracowano ogólną metodę, opartą na reakcji Wittiga [363], aby przezwyciężyć problem wprowadzania łańcucha alkilowego do pierścienia aromatycznego. Problem został rozwiązany w reakcji długołańcuchowych alkanoli, jeśli były dostępne, z częściowo ustabilizowanymi benzylofosfoniowymiilidami lub alternatywnie 3,5-dimetoksybenzenokarbaldehydem z alkilofosfoniowymi ilidami. Procedura dostarczyła 5-alkilorezorcynole z łańcuchami alkilowymi do 25 atomów węgla. Reakcję prowadzono w wodzie lub mieszaninie woda-DMSO, przy napromieniowaniu MW, w naczyniu pod ciśnieniem lub w otwartym naczyniu. Jeden przykład dla każdej trasy pokazano na Schemacie 39.

Umiarkowaną lub dobrą aktywność przeciwutleniającą in vitro wykazał 1,2-dibutanoiloksy-2-(4-hydroksy-3-metoksyfenylo)etylobutanian, fenol lipidowy otrzymywany z kwasu ferulowego [354] .
2-Metylo-5-[(2Z)-non-2-en-1-ylo]benzeno-13-diol i 5-[(2Z)-non{ {10}}en-1-ylo]benzen-1,2,3-triol zostały przygotowane jako syntetyczne pochodne naturalnego 5-[(2Z)-non{{18} }en-1-yl]benzen-1,3-diol (climacostol), substancja chemiczna obronna w pierwotniakach Climacostomum virens [355]. Modyfikacje strukturalne w pierścieniu aromatycznym (odpowiednio grupa metylowa i grupa hydroksylowa) zwiększyły toksyczność.
Long-chain alkyl hydroxycinnamates were prepared from the corresponding monoesters of malonic acid and benzaldehyde derivatives by Knoevenagel condensation [364]. The observed antioxidant activity followed the order caffeic esters > sinapic esters >estry ferulowe.
Kwas 12-hydroksy-9-oktadekanowy (kwas rycynolowy) został przekształcony w (Z)--12-aminooktadeka-9-enian, a następnie poddany reakcji z kwasami fenolowymi, tworząc odpowiednie amidy [356 ]. Badana aktywność przeciwutleniająca wykazała, że modyfikacja kwasów fenolowych ugrupowaniami lipofilowymi poprawia ich właściwości przeciwutleniające i przeciwnowotworowe.
Warto zasygnalizować koncepcyjnie inny typ fenoli lipidowych, a mianowicie pochodne fenylosulfonylofuroksanu kwasów kawowego i innych kwasów fenolowych [357]. Oprócz dobrej aktywności przeciwutleniającej in vivo, związki te wykazywały działanie przeciwzakrzepowe i rozszerzające naczynia krwionośne, które przypisywano zdolności do uwalniania NO.
Kwas kawowy lub 3,4-dimetylokawowy poddano reakcji z kwasem jabłkowym, a następnie sprzęgano z monoglicerydami kwasów tłuszczowych o długości łańcucha od 8 do 18 atomów C [359]. Kombinacje kwasów fenolowych i tłuszczowych dały serię sześciu związków amfifilowych, które przetestowano pod kątem aktywności. Według autorów okazały się nietoksyczne i dawały stabilne emulsje typu olej w wodzie, które mogą znaleźć zastosowanie w przemyśle spożywczym, farmaceutycznym i kosmetycznym.

6. Polifenole
Naturalnypolifenolestanowią liczną i szeroko rozpowszechnioną grupę cząsteczek bioaktywnych w roślinach jadalnych, o bioaktywnościach od ochrony układu sercowo-naczyniowego po zapobieganie nowotworom [365-368].
Polifenole charakteryzują się obecnością pierścienia heteroaromatycznego skondensowanego z benzoem typu piren lub pirydium. Są one zwykle nazywane według półsystematycznej nomenklatury, opartej na macierzystym heterocyklu. Tak więc pochodne benzopirenu z podstawnikiem fenylowym nazywane są flawonami, podczas gdy benzofenony podstawione fenolem są określane jako flawony. Struktury związków macierzystych i ich pochodnych fenylowych zebrano na Rysunku 9.

Synteza naturalnej i półsyntetycznej wysoko utlenionej substancji bioaktywnejpolifenolezostał poddany przeglądowi w 2008 r., omawiając postępy i wyzwania [369]. Alternatywnie, bardziej wydajna i zrównoważona produkcja może pochodzić z fabryk komórek drobnoustrojów, zgodnie z przeglądem w 2018 r. [370].
Chemiczne przemiany naturalnych fenoli mogą prowadzić do bardziej efektywnych gatunków, jeśli zrozumiemy cechy strukturalne leżące u podstaw aktywności biologicznej. Tak więc wyniki modyfikacji chemicznych dla reprezentatywnych polifenoli przedstawiono poniżej.
6.1.Fenole z Chromanu
Katechina to polifenol z rodziny flawanoli, który można znaleźć w zielonej herbacie. Pochodne przedstawione na Figurze 10 wytworzono z racemicznej katechiny (tetrametoksy, pentaacetoksy i cykliczne) [371]. Katechina i jej pochodne zostały przetestowane pod kątem aktywności przeciwdrobnoustrojowej wobec grzybów zasiedlających korzenie, która została utrzymana, choć z mniejszą skutecznością, w związkach mniej polarnych.

Wychwytywanie rodników antyoksydacyjnych przez (plus)-katechinę, badaną przeciwko rodnikowi galwinoksylowemu, nasila się w reakcji z ninhydryną [374].
Aby rozwiązać problem narastającej odporności drobnoustrojów, przeprowadzono badania mające na celu przygotowanie i przetestowanie syntetycznych pochodnych katechiny. Systematyczna eteryfikacja 3-grup hydroksylowych z liniowymi łańcuchami alkilowymi o różnej długości lub z podstawionymi grupami benzylowymi dała bibliotekę 3-O-alkilowych analogów katechiny [372], które zostały użyte do badania działania przeciwgrzybiczego jako funkcja struktury. Związki o dłuższych łańcuchach (C14-C16) wykazywały słabsze działanie niż związki z łańcuchami C8-C12.
Ponadto, zmieniając grupę funkcyjną -OH w 3, otrzymano dwanaście pochodnych (-)-katechiny [373]. Tylko trzy związki wykazały aktywność przeciwbakteryjną i przeciwgrzybiczą wyższą niż standardowe leki (neomycyna i mikonazol). Badania dokowania molekularnego zgadzały się z wynikami eksperymentalnymi.
Brazylia i utleniony analog brazyliny (Rysunek 11) są pochodnymi chromanu występującymi w roślinach (Caesalpinia sappan L.), znanymi ze swoich właściwości przeciwzapalnych. Przygotowano nowe syntetyczne pochodne, aby zbadać ich działanie przeciwnowotworowe. Syntezę Brazylijczyków [375] osiągnięto zaczynając od 1,3-dihydroksybenzenu (rezorcynolu) i kwasu 3-chloropropanowego, z utworzeniem kluczowego związku pośredniego 7-hydroksy-4-chromanonu . Zsyntetyzowanych Brazylijczyków (Figura 11) testowano pod kątem działania przeciwzapalnego przeciwko wielu ludzkim liniom komórek rakowych, ale tylko niektóre z syntetycznych pochodnych wykazały pewną poprawę w stosunku do niepodstawionej brazyliny.

6.2. Fenole z Chromena
Kumaryna (2H-chromen-2-on), najpowszechniejsza pochodna chromu, oraz podstawione kumaryny znajdują się w roślinach zielonych, gdzie mają różne działanie [377].
Biorąc pod uwagę wszechstronność reakcji prowadzących do heterocykli kumaryny [378, zsyntetyzowano szereg podstawionych kumaryn i stwierdzono obiecującą aktywność ze sprzężonymi z kumaryną 14A-tiazepinami, zsyntetyzowanymi wychodząc z 4-hydroksykumaryn (Schemat 40) [379].

Kumaryny i benzokumaryny podstawione grupą hydroksylową w pozycjach 7-lub 8- zostały przygotowane i przetestowane in vitro pod kątem szeregu aktywności biologicznych [380]. Generalnie dostarczały one silnych zmiataczy anionów ponadtlenkowych i hamowały peroksydację lipidów in vitro; z drugiej strony nie wykazywały znaczącej aktywności hamującej lipooksygenazę.
6.3.Fenole z Chromon
Kwercetyna (3,3'4',5,7-pentahydroksyflawon) to flawonol w dużej mierze obecny w roślinach, żywności i napojach, często razem z fisetyną (3,3'4',7-tetrahydroksyflawon) .
Zainteresowanie kwercetyną wywołało jej działanie przeciwnowotworowe, przeciwzapalne i przeciwutleniające. Szczególne znaczenie ma działanie przeciwnadciśnieniowe [381]. Wiele syntetycznych pochodnych przygotowano w celu uzyskania kandydatów przeciwnowotworowych, które mogłyby przezwyciężyć problemy z kwercetyną: (i) niską rozpuszczalność w wodzie, (ii) niską biodostępność i (ii) szybką degradację. Badania aktywności biologicznej nie były wystarczające do oceny faktycznej skuteczności tych pochodnych, choć niektóre z nich wydawały się obiecujące [382]. Z drugiej strony proste kompleksowanie z Cu(I) dało kompleks Cu(kwercetyna)(bipy) o zwiększonych właściwościach antyoksydacyjnych w porównaniu z wolną kwercetyną [383].
Zainteresowanie terapeutycznymi właściwościami kwercetyny i jej pochodnych nie ogranicza się do cytotoksyczności, o czym świadczy liczba patentów zgłoszonych w latach 2010–2015 [384]. Wybrane znaczące przykłady zebrano w Tabeli 2.

Większość takich pochodnych wiązała się z przekształceniami na wszystkich grupach hydroksylowych, przy czym modyfikacja na grupie hydroksylowej C-3- skutkowała wzmocnieniem działania przeciwnowotworowego. Ponadto bioaktywność została znacznie zwiększona dzięki nanotechnologii.
Problem niedostatecznej rozpuszczalności w wodzieflawonoidypolifenole zostały uwzględnione, biorąc pod uwagę pochodne z hydrofilowymi podstawnikami, takie jak siarczan [385].
Innym podejściem było przygotowanie koniugatów cukrów z flawonoidem będącym aglikonem. Stosowano między innymi glukozę, galaktozę i ramnozę.
Synteza enzymatyczna zakończyła się sukcesem w modyfikowaniu naturalnych związków, dając nie tylko bardziej rozpuszczalne, ale także bardziej wydajne gatunki w zastosowaniach medycznych [386] lub kosmeceutycznych [387].
Interesujące jest to, że rutyna (2-(3,4-dihydroksyfenylo)-5,7-dihydroksy-3-[-L-ramnopiranozyl-(1→6){ {11}}D-glukopiranozyloksyloksy]-4H-chromen-4-on) został dalej przekształcony w reakcji enzymatycznej transestryfikacji w pochodne mono- i dioctanu (Schemat 41) o zachowanych właściwościach przeciwutleniających i nie tylko wydajna zdolność do penetracji błony komórkowej mysich makrofagów [388]. Co więcej, rutyny podstawione grupą acetoksy nie były toksyczne dla komórek ssaków, a enzym można było ponownie wykorzystać.

Przykładem znaczenia flawonoidów podstawionych cukrem jest mirycytryna (myricetin-3-O- -L-ramnopiranozyd), której działanie przeciwutleniające miało działanie ochronne przed uszkodzeniem DNA [389].
Przygotowano nowe rusztowanie flawonoidowe w celu wprowadzenia grup salicylowych i trimetoksybenzenowych do flawonoidów [390]. Wszystkie związki oceniano pod kątem aktywności antyproliferacyjnej wobec trzech ludzkich komórek nowotworowych wykazujących aktywność umiarkowaną do dobrej.
6.4.Fenole z 2,3-dihydrochromonu
Wśród flawanonów zainteresowanie wzbudziły metabolity wtórne roślin o szerokim spektrum aktywności biologicznej, prążkowane (5-hydroksy-7-metoksyflawanon), ponieważ jest to główny składnik kłącza palucha (Kaempferia pandurata), stosowany w kuchni Azji Południowo-Wschodniej, o którym wiadomo, że ma kilka właściwości farmakologicznych, wśród których obiecujące jest działanie przeciwdrobnoustrojowe.
Allilację i prenylację pinostrobiny przeprowadzono przy użyciu napromieniowania MW (reakcje Mitsunobu i metatezy, przegrupowania Claisena i Cope'a) (Schemat 42), dając związki, które zostały przetestowane na wielu liniach komórek rakowych [391]. Pochodne były bardziej reaktywne niż pinostrobina, co autorzy przypisali lepszej interakcji z celami biologicznymi, ze względu na zwiększoną lipofilność zapewnioną przez podstawniki alkenylowe.

Pinostrybinę prenylowano w prostych warunkach SN2 (Schemat 43), dając mieszaninę produktów, z których większość utraciła strukturę flawanonu. Oddzielono je i przebadano pod kątem aktywności przeciwdrobnoustrojowej [392], wykazując umiarkowany efekt. Co ciekawe, kilka prenylowanych kumaryn i kwercetyn wyizolowano z kory korzenia Broussonefia papyrifera jako metabolity o, w niektórych przypadkach, działaniu cytotoksycznym [393].

Astilbina, cukrowa pochodna taksyfoliny flawanolu, jest pozyskiwana z ziołowych roślin leczniczych, powszechnie stosowanych w tradycyjnej medycynie chińskiej. Jednak dla ich możliwego zastosowania farmaceutycznego astilbina dostępna z ekstrakcji nie jest wystarczająca. Wydajny proces otrzymywania astilbiny z taksyfoliny opierał się na fermentacji mikrobiologicznej w genetycznie zmodyfikowanej Escherichia coli (Schemat 44) [394].

Opracowano kaskadowy system biokatalityczny w celu przygotowania pochodnych 4'-O-glukozydowych naringeniny (5,7-dihydroksyflawanon), flawonoidu o kilku właściwościach bioaktywnych, występującego w winogronach i pomarańczach [395]. Metoda polega na regeneracji difosforanu urydyny z sacharozy i jej ponownym wykorzystaniu, a także produkcji na skalę preparatywną. Tą samą metodą otrzymano kwercetynę 7-OaL-ramnozyd.
Co ciekawe, mirycytryna (myrycetyna-3-O- -L-ramnopiranozyd)[389] i naringenina obecne w ekstraktach z Cynara cardunculus, silnego naturalnego herbicydu, wykazywały działanie fitotoksyczne na liście Trifolium incarnatum, otwierając droga do naturalnych herbicydów, dziedzina o coraz większym znaczeniu ze względu na rosnącą odporność chwastów na powszechnie stosowane[396].

7. Kurkumina i kurkuminoidy
Kurkumina, [1,7-bis(4-hydroksy-3-metoksyfenyl)-1,6-heptadien-3,5-dionel, żółty barwnik wyizolowany z kurkumy (Curcuma longa Linn), to wielofunkcyjny związek, który przynajmniej z literatury z ostatnich dwudziestu lat wydaje się być rodzajem panaceum na wszelkie choroby współczesnego społeczeństwa, w tym raka i chorobę Alzheimera. Grupy fenolowo-OH zapewniają właściwości przeciwutleniające, natomiast podstawą aktywności fotodynamicznej jest ekstensywna koniugacja spowodowana równowagą ketoenolową (Schemat 45).

Kilka ostatnich przeglądów omawia aspekty aktywności biologicznej [397-400] i możliwe zastosowania medyczne [70,292,401-404] kurkumin i pochodnych. Omówiono również ważne aspekty, takie jak nowe metody dostarczania i efekty synergiczne z innymi związkami, wraz z mechanizmem działania [405]. Coraz większe zainteresowanie wzbudzają oparte na kurkuminie leki przeciw chorobom neurodegeneracyjnym [406], zwłaszcza chorobie Alzheimera [407] i rakowi [408].
Poszukiwanie nowych pochodnych kurkuminy jest motywowane (i) koniecznością zwiększenia dostępności materiału oraz (i) koniecznością polepszenia rozpuszczalności w roztworze wodnym.
Warto zauważyć, że samo traktowanie kurkuminy Cu(II), wyizolowano kompleks Cu(kurkumina)(bipy), który lepiej wiązał się z przeciwutleniaczem i DNA w porównaniu z wolną kurkuminą, będąc jednocześnie mniej toksyczną, na podstawie jej właściwości przeciwgrzybiczych [383] . Doniesiono również, że nanokoniugaty srebro-kurkumina, przygotowane metodą sonochemiczną, były testowane na liniach komórkowych skóry i pod kątem działania przeciwbakteryjnego przeciwko Escherichia coli. Wyniki wykazały, że nanocząsteczki srebra zostały biokompatybilne dzięki kurkuminie, podczas gdy kurkumina jest bardziej fotostabilna i bardziej aktywna jako środek przeciwbakteryjny [409].
Omawiamy pochodne kurkuminy w zależności od zmian strukturalnych.
7.1. Drobne zmiany strukturalne
Małe zmiany strukturalne mogą zmienić wydajnośćkurkuminabioaktywność. Na przykład, wprowadzenie jednej grupy metylowej w pozycji 2 lub dwóch grup metylowych, jak w 2,7-dimetylokurkuminie, zaobserwowano wzmożoną aktywność przeciw angiogenezie i zahamowanie wzrostu guza [410], wraz ze zwiększoną aktywnością przeciwzapalną [411 ] i stabilność wobec redukcji enzymatycznej [412], w odniesieniu do kurkuminy.
Diacetylokurkumina, łatwo wytwarzana przez acetylację związku macierzystego, wykazała doskonałe działanie przeciwbakteryjne [413] i była skuteczna w działaniu przeciwartretycznym u myszy (tabela 3) [414].
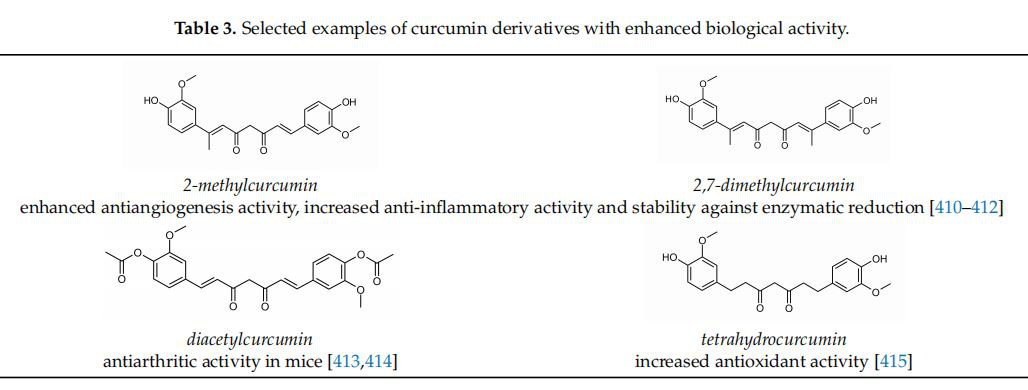


Aktywność przeciwutleniającą kurkuminy porównano z metabolitami dimetoksy i uwodornionymi pochodnymi [415]. Wyniki wskazują, że nasycone pochodne (tetrahydro-, heksahydro- i oktaedron-kumaryny) mają zwiększoną aktywność przeciwutleniającą w stosunku do kumaryny (tabela 3).
Pochodną otrzymaną przez wprowadzenie podstawników prenylowych w oba pierścienie aromatyczne poddano testom na stres oksydacyjny [416] (tabela 3), wykazując równe lub lepsze właściwości przeciwutleniające w stosunku do kurkuminy.
Przeprowadzono bardziej drastyczną substytucję, wprowadzając podstawniki odciągające elektrony do pierścieni benzenowych, a nawet kondensując heterocykle (tabela 3)[417].
7.2. Podstawniki w łańcuchu nienasyconym
Większość syntetycznych pochodnych pochodzi z wprowadzenia podstawników w pozycji 4, wpływając w ten sposób na równowagę tautomeryczną kurkuminy. Ważną bioaktywnością związaną z równowagą keto-enolową jest interakcja z agregacją amyloidu (A) obecną w chorobie Alzheimera. Przeprowadzono szeroko zakrojone badania równowag tautomerycznych keto-enolu w podstawionych kurkuminach [432-434]. Ostatnio doniesiono, że 4,4-dipodstawiona kurkumina (ryc. 12), gdzie forma ketonowa jest jedyną możliwą, wiąże niewłókniste rozpuszczalne oligomery A, stając się, jak twierdzą autorzy, „pierwszą generacją związek ukierunkowany na oligomery A”[435].
Fluorowane pochodne kurkuminy wykazywały znaczące hamowanie białka oddziałującego z tioredoksyną (TXNIP), które jest związane z wieloma chorobami [418].
Wytworzono szereg pochodnych kurkuminy podstawionych grupami kwasowymi lub estrowymi w pozycji 4 [436] (Figura 13). Określono kwasowość, lipofilność i stabilność kinetyczną wraz z aktywnością wymiatania wolnych rodników w celu oceny jakiegokolwiek związku między strukturą a aktywnością. Pochodne estrowe wykazywały selektywność wobec komórek raka okrężnicy, prawdopodobnie ze względu na ich wyższą lipofilność dzięki kurkuminie.
![The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers](/Content/uploads/2022842169/20220328112546d633ce9f0cd54ad68e1c33ed5c4758d7.png)

Innym podejściem było wprowadzenie ugrupowania nienasyconego w pozycji 4 (Tabela 3), w reakcji Knovenagla z benzenokarbaldehydem, 4-hydroksybenzaldehydem i 4-hydroksy-3-metoksybenzaldehydem (waniliną)419 ]. Otrzymane pochodne zostały przetestowane pod kątem działania przeciw malarii wobec P. falciparum, a pochodna waniliny była bardzo silna. 4-Kurkuminy benzylidenowe, przygotowane z 2-hydroksybenzenokarbaldehydu [420] i 4-benzylidenokurkumin, były badane jako środki przeciwutleniające i oba były skuteczne w tłumieniu zaćmy w hodowanych soczewkach szczurzych.
7.3. Modyfikacja ugrupowania -dikarbonylowego
Osiemnaście nowych pochodnych, wciąż zawierających hepta-1,6-dien-3,5-dionową strukturę kurkuminy, ale z jedną z grup karbonylowych włączonych do ugrupowania cykloheptanonu, zostało syntetyzowany przez wszechstronną strategię syntetyczną [421]. Jeden przykład podstawionego tropinonu przedstawiono w Tabeli 3. Autorzy są przekonani, że rodzina kurkumin dikarbonylowych z pierścieniem tropanu będzie miała ważną aktywność, ponieważ proste monokarbonylotropanony były cytotoksyczne wobec komórek raka piersi.
Bibliotekę pochodnych kurkuminy otrzymano po reakcji z jednym lub dwoma równoważnikami sulfonamidów (wybranych spośród sulfonamidów) (Schemat 46) [437]. Aktywność przeciwbakteryjną i przeciwgrzybiczą oceniano wobec drobnoustrojów Gram-dodatnich i Gram-ujemnych, z dobrymi wynikami.

Analogi 3,4-dihydropirymidyny-2(1H)-onu i tionu kurkuminy (Tabela 3) zsyntetyzowano z dobrą wydajnością przez jednonaczyniową wieloskładnikową cyklokondensację przy napromieniowaniu MW [425]. Badania antybakteryjne i przeciwutleniające przeprowadzono in vitro z wynikami uznanymi przez autorów za „umiarkowane” w pierwszym przypadku i „doskonałe” w drugim.
Pochodna pirazolu kurkuminy została przygotowana, aby spróbować włączyć w tę samą cząsteczkę cechy strukturalne kurkuminy i związku asteroidopodobnego (cykloheksylobisfenol A) [422]. Stwierdzono, że związek ma działanie neuroprotekcyjne w testach hodowli komórkowych, także przeciwko wewnątrzkomórkowym i zewnątrzkomórkowym amyloidowi. Ponadto w teście rozpoznawania obiektów u szczurów stwierdzono, że posiada właściwości wzmacniające pamięć [423].

7.4. Częściowe zastąpienie ugrupowania -dikarbonylowego
Częściowe zastąpienie ugrupowania -dikarbonylowego kurkuminy uznano za przydatne do przezwyciężenia problemu jej niezadowalającej stabilności. Seria monokarbonylowych analogów kurkuminy, zsyntetyzowanych z odpowiednio podstawionego benzaldehydu i cykloalkanu [438-440]. Stabilność podstawionych cyklopentanonów i cykloheksanonów została zwiększona in vitro. Aktywność cytotoksyczna była również wyższa w przypadku cykloheksanonów, z niezwykłym znaczeniem efektów elektronowych podstawników (Schemat 47).

Analogi aminokarbonylo-kurkuminy zostały przetestowane pod kątem prozapalnych cytokin, wykazując silniejszą zdolność hamowania niż kurkumina.
Symetryczne bis(arylideno)ketony wytworzono w reakcji cykloalkanonu z podstawionymi benzaldehydami, w kondensacji aldolowej katalizowanej kwasem. Większość zsyntetyzowanych związków wykazywała hamowanie wzrostu komórek raka jajnika, nawet w przypadku komórek opornych na cisplatynę [441].
Kilka syntetycznych analogów kurkuminy aminokarbonylowej zostało przetestowanych przeciwko Trichomonas vaginalis (uważanej za „najczęstszą niewirusową infekcję przenoszoną drogą płciową na świecie”)[442];15-difenylopenta-1,4-dien{ {5}}jeden,15-bis(2-chlorofenylo)penta-1.4-dien-3-jeden i 2,6-bis({ {13}}chlorobenzylideno)cykloheksanon wykazywał znaczące działanie przeciwpasożytnicze w skutecznych stężeniach niższych niż kurkumina.
Niedawno pierwszy, ale bardzo obiecujący wynik uzyskano z użyciem (2E,6E)-2,6-bis(2(trifluorometylo)benzylideno)cykloheksanonu, który okazał się leczyć rany cukrzycowe w myszy [426] (tabela 3).
Zsyntetyzowano kilkanaście analogów kurkuminy z aminokarbonylami, aby znaleźć związki o zwiększonej stabilności chemicznej i, ostatecznie, lepszej aktywności przeciwnowotworowej wobec niektórych ludzkich komórek nowotworowych [427]. Dwa z nich (tab. 3) spełniły wymagania i były sukcesywnie testowane na komórkach czerniaka, co skutkowało selektywną toksycznością428].
Nowe kurkuminoidy zawierające heterocykle 4H-piranu wytworzono przez jednonaczyniową kondensację kurkuminy z propanodinitrylem i podstawionym benzenokarbaldehydem (Schemat 48) [443]. Konsekwentna modyfikacja ugrupowania β-dikarbonylowego poprawiła hamowanie β-glukozydazy, jednego z enzymów odpowiedzialnych za hydrolizę węglowodanów, a zatem za hiperglikemię poposiłkową. Ta cecha, wraz z działaniem antyoksydacyjnym, może mieć korzystny wpływ na cukrzycę, zwłaszcza że nie zaobserwowano toksycznego wpływu na pospolitą mikroflorę jelitową człowieka.

7.5. Zmniejszenie długości łańcucha nienasyconego
Analog kurkuminy, 5-(3,4-dihydroksyfenyl)-3-hydroksy-1-(2-hydroksyfenylo)penta-2,4- diene-1-jeden wykazał działanie przeciwzapalne u myszy (tabela 3) [429]. Podobne związki o tym samym szkielecie zastosowano w celu ustalenia znaczenia regulacji reaktywnych form tlenu w hamowaniu nowotworzenia [444]. Według autorów, związki te są obiecujące dla opracowania leku przeciwnowotworowego o niewielkich skutkach ubocznych.
Wytworzono podobny, ale krótszy związek, (Z)-3-hydroksy-1-(2-hydroksyfenylo)-3-fenyloprop-2-eno-1-on zacząć od 2-hydroksyfenylometyloketonu i benzoilu
chlorek (Schemat 49). Powstała cząsteczka wykazała selektywną cytotoksyczność wobec komórek MCF -7 raka piersi [445], ludzkich linii komórkowych raka okrężnicy [446] i ludzkich komórek kostniakomięsaka [447].

7.6. Derioatioes z tylko „połową” struktury kurkuminy
Rodzina związków, nazwana przez autorów retro-kurkuminoidami, została przygotowana tak, aby zachować tylko „połowę” struktury kurkuminy (Schemat 50), ponieważ ugrupowanie -dikarbonylowe uważano za odpowiedzialne za stabilność niedoboru kurkuminy [448]. Powstałe związki wykazywały istotną aktywność cytotoksyczną wobec ludzkich linii komórek nowotworowych, ale nie uszkadzały zdrowych komórek.

Syntetyczny analog amidu wykazywał właściwości przeciwutleniające i przeciwzapalne. Testowano go z dobrymi wynikami na stłuszczenie wątroby u myszy z indukowaną otyłością [430] (Tabela 3).
Bibliotekę hybryd kurkumina-resweratrol zsyntetyzowano zaczynając od hydrazydowej pochodnej podstawionego kwasu cynamonowego i serii podstawionych benzaldehydów [449]. Przykład przedstawiony na Schemacie 51 odnosi się do najbardziej obiecującej hybrydy jako przeciwnowotworowego środka wielocelowego.

7.7. Fotouczulacze
Kurkumina może być doskonałym fotosensybilizatorem ze względu na dobrą biokompatybilność, ale jej praktyczne zastosowanie jest mocno ograniczone przez jej niską stabilność i słabą rozpuszczalność w wodzie. Poszukiwano rozwiązania przygotowując pochodne kurkuminy z podstawnikami kationowymi [450](Rysunek 14).

Wszystkie pochodne wykazały wysoką stabilność przy pH i temperaturze. Jeśli chodzi o właściwości fotodynamiczne, byli w stanie promować fotodynamiczną dezaktywację E.coli, przy czym związki heksa-kationowe były najskuteczniejsze, prawdopodobnie ze względu na wysoką hydrofilowość.
Przeprowadzono badanie porównawcze różnych pochodnych kurkuminy syntetyzowanych ad hoc, w celu zwiększenia penetracji tkanek, zwiększając maksimum wchłaniania. Tak więc 1,11-difenyl-1,3,8,10-undekatetraen-57-dion i 1,7-bis(4'-dimetyloaminofenyl){{11 }},6-heptadienyl-3,5-dione prezentowały obiecujące właściwości pod względem generowania reaktywnych form tlenu, a zatem skuteczności w terapii fotodynamicznej [431]. 8. Wnioski
Naturalne fenole i ich pochodne o aktywności biologicznej stanowią szybko rozwijający się temat badawczy ze względu na ich wiele obecnych i przyszłych zastosowań. Ich różnorodność strukturalna daje wiele możliwości przemian chemicznych, mających na celu przezwyciężenie wad naturalnych fenoli. Jednak poza pewnymi wytycznymi, które wyłoniły się z ogromnej liczby publikacji, takich jak potrzeba poprawy stabilności i biodostępności związków bioaktywnych, obraz wymagań strukturalnych nie jest jeszcze pełny, z uwagi na optymalizację zastosowań in vivo i polowych .
