Jaki jest związek między niedoborem mitochondrialnego czynnika transkrypcji ukierunkowanych na nabłonek nerki a zespołem policystycznych nerek--Część I
Mar 12, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Niedobór mitochondrialnego czynnika transkrypcyjnego A ukierunkowany na nabłonek nerki powoduje postępującą deplecję mitochondrialną związaną z ciężką chorobą torbielowatą.--Część I
Ken Ishii1,2,11 i inni
Nieprawidłowa funkcja mitochondriów jest dobrze rozpoznaną cechą ostrych i przewlekłychnerka choroby. Aby uzyskać wgląd w rolę mitochondriów wnerkahomeostazy i patogenezy, skupiliśmy się na mitochondrialnym czynniku transkrypcyjnym A (TFAM), białku niezbędnym do replikacji i transkrypcji mitochondrialnego DNA, które odgrywa kluczową rolę w utrzymaniu masy i funkcji mitochondriów. Aby zbadać konsekwencje zaburzonej funkcji mitochondriów w:nerkakomórek nabłonkowych, inaktywowaliśmy TFAM w homeoboxie związanym z sine oculis 2-wyrażającnerkaKomórki progenitorowe. Niedobór TFAM skutkował znacznie obniżoną ekspresją genów mitochondrialnych, zubożeniem mitochondriów, zahamowaniem dojrzewania nefronu i rozwojem ciężkiej pourodzeniowej choroby torbielowatej, co skutkowało przedwczesną śmiercią. Było to związane z nieprawidłową morfologią mitochondriów, zmniejszeniem zużycia tlenu i zwiększonym przepływem glikolitycznym. Ponadto odkryliśmy, że ekspresja TFAM była zmniejszona u myszy i ludzipolicystyczne nerki, któremu towarzyszyło zubożenie mitochondriów. Zatem nasze dane sugerują, że dysregulacja ekspresji TFAM i deplecja mitochondrialna są cechami molekularnyminerkachoroba torbielowata, która może przyczynić się do jej patogenezy.
SŁOWA KLUCZOWE: glikoliza; rozwój nerek; mitochondria;wielotorbielowatość nerek; TFAM

cistanchejest dobre dlawielotorbielowatość nerek
Oświadczenie tłumaczące
Wykorzystaliśmy genetykę myszy, aby zrozumieć rolę dysfunkcji mitochondriów w:nerkahomeostaza. Inaktywacja mitochondrialnego czynnika transkrypcyjnego A (TFAM) w nabłonkowych komórkach progenitorowych homeobox 2 związanych z sine oculis 2 spowodowałanerkowyawariaz powodu ciężkiegopolicystyczna nerka choroba. Nasze odkrycia pokazują, że postępująca dysfunkcja mitochondriów jest związana z wadliwym różnicowaniem nabłonka inerkowycystogeneza. Ponadto ustaliliśmy, że ekspresja TFAM i liczba mitochondriów u ludzi były zmniejszonepolicystyczna nerkapapierowa chusteczka. Nasze badania sugerują, że strategie terapeutyczne, których celem jest poprawa zdrowia mitochondriów, mogą być korzystne w leczeniu pacjentów z autosomalną dominującąpolicystyczna nerkachoroba.
Dysfunkcja mitochondrialna (mt) jest dobrze rozpoznaną patologiczną cechą pospolitejnerka chorobyi może wywołać uszkodzenie komórek, stan zapalny i zwłóknienie.1nerka, komórki nabłonka kanalików są silnie zależne od adenozynotrójfosforanu (ATP) generowanego w wyniku fosforylacji oksydacyjnej (OXPHOS), ponieważ pełnią wiele energochłonnych funkcji transportowych nabłonka. Dlatego utrzymanie wydajnej produkcji ATP mt jest niezbędne dla prawidłowej pracy nerek i ogólnoustrojowej homeostazy elektrolitów. Ponadto ostatnie dowody wskazują, że mitochondria odgrywają ważną rolę w regulacji genów, sygnalizacji komórkowej i różnicowaniu komórek poprzez wytwarzanie pośrednich metabolitów i reaktywnych form tlenu (ROS).2 Pomimo tych postępów, rola sygnalizacji mt w patogenezienerkachorobynie jest dobrze zrozumiana.
Aby zbadać funkcję mt wnerkowyhomeostazę i patogenezę, celowaliśmy w mitochondrialny czynnik transkrypcyjny A (TFAM). TFAM jest kodowanym w jądrze czynnikiem niezbędnym dla funkcji mt, utrzymania liczby kopii mt i stabilności strukturalnej mt DNA, ponieważ reguluje replikację i transkrypcję genomu mt poprzez zginanie promotora DNA.3,4 DNA mt ssaka zawiera 37 genów, 13 z których kodują podjednostki białkowe kompleksu łańcucha oddechowego, 22 kodują transferowe RNA i 2 rybosomalne RNA.3 Tak więc TFAM jest bezpośrednio zaangażowany w regulację transportu elektronów mt i syntezę ATP poprzez transkrypcję genów, takich jak kodowany w mitochondriach cytochrom b ( MT-CYB), kodowana mitochondrialnie podjednostka 1 oksydazy cytochromu c (MT-CO1) i kodowana mitochondrialnie podjednostka 6 błony syntazy ATP (MTATP6). ROS i stopniowo pozbawiają się mitochondriów.6-9 Badania genetyczne wykazały, że TFAM jest niezbędny dla prawidłowej embriogenezy, ponieważ globalna inaktywacja homozygotycznego Tfam spowodowała wewnątrzmaciczną śmiertelność do 10,5 dnia embrionalnego, podczas gdy niedobór heterozygotyczny, chociaż zmniejszył liczbę kopii mt o ~40 procent i doprowadził do niedoboru łańcucha oddechowego, nie doprowadził do śmiertelności embrionalnej. postępującej dysfunkcji mt w różnicowaniu komórek i homeostazie tkanek. Warunkowa inaktywacja Tfam specyficzna dla typu komórki sugerowała, że wytwarzanie OXPHOS i/lub mt ROS ma kluczowe znaczenie dla różnicowania, funkcji i prawidłowej fizjologii komórek.6-10
Pierwotne zaburzenia mt spowodowane mutacjami jądra lub genu mt mogą objawiać się:nerka chorobanajczęściej objawia się uszkodzeniem kanalików śródmiąższowych lub izolowaną dysfunkcją kanalików.11,12nerkowychoroby nie zostały zgłoszone. Ostatnio zmniejszona ekspresja TFAM została powiązana z przewlekłymnerkachoroba. Utrata integralności mt z powodu inaktywacji Tfam spowodowała chorobę kanalikowo-śródmiąższową inerkowy awariau myszy, co częściowo wynikało z aktywacji wywołanej stresem mt DNA cyklicznej syntazy GMP-AMP (cGAS) – stymulatora zależnej od genów interferonu (STING) odpowiedzi zapalnej.14
W tym miejscu donosimy, że u myszy z warunkową inaktywacją Tfam w komórkach progenitorowych nefronów, związanych z sine oculis 2 (SIX2)15, rozwijają się poważne choroby torbielowate i przedwcześnie umierają.nerkowyawariajako młode młodociane myszy.Tfam-/- myszy charakteryzowały się defektami dojrzewania nefronu, co było związane z ubytkiem mt, redukcją OXPHOS i metabolicznym przesunięciem w kierunku glikolizy wTfam-/- nerkowynabłonek. Biorąc pod uwagę nasilenie choroby torbielowatej wTfam-/- myszy, przeanalizowaliśmy 2 mysie modelepolicystyczna nerkachoroba(PKD), które wynikają z mutacji w obu polycystin-1 (PKD(wielotorbielowatość nerek)1) lub cystyna-1 (Cys1), jak również tkanki ludzkie pochodzące od pacjentów z autosomalną dominującą wielotorbielowatością nerek (ADPKD). Ustalamy, żeTfam-/- jest rozregulowany w cystach zarówno mysich, jak i ludzkich PKD(wielotorbielowatość nerek), tkanki. Podsumowując, nasze badania sugerują, że dysregulacja TFAM i zubożenie mt są charakterystycznymi cechaminerkowychoroby torbielowate i mogą mieć udział w ich patogenezie.

cistanchejest dobre dlawielotorbielowatość nerek
WYNIKI
Inaktywacja Tfam w komórkach linii SIX2 powoduje ciężką chorobę torbielowatą, co skutkuje:nerkowyawariaW celu zbadania funkcji mt wnerkowynabłonka, inaktywowaliśmy Tfam w SZEŚCIU 2-ekspresjonujących komórkach progenitorowych, które dają początek wszystkim segmentom nefronu, z wyjątkiem przewodu zbiorczego (CD). wzmocnione białko fuzyjne zielone fluorescencyjne białko/rekombinaza Cre (eGFP/Cre) pod kontrolą transkrypcyjną promotora Six2 (Figura 1a).16 Myszy homozygotyczne pod względem floksowanego allelu Tfam i heterozygotyczne pod względem transgenu eGFP/Cre (Sześć2-eGFP/Cretg/tg plus; Tfamfl/fl) jest odtąd określana jako Sześć2-Tfam-/- mutanty. sześć2-Tfam-/- myszy urodziły się w oczekiwanych proporcjach Mendla i nie można ich było odróżnić od kontrolnych zwierząt z tego samego miotu Cre przez oględziny po urodzeniu. Jednak różnice w masie ciała między Six2-Tfam-/- mutanty i kontrole z tego samego miotu Cre stały się widoczne do 14 dnia po urodzeniu (P) (5,7 plus -0,3 g dla mutantów vs. 7,5 plus -0,3 g dla kontroli, n=4 każdy, P =0.004; Tabela uzupełniająca S1). Sześć2-Tfam-/- zmutowane myszy charakteryzowały się powiększonymnerkiw porównaniu z kontrolami (nerka/masa ciała 1,45% plus -00,19% dla mutantów vs. 0,60% plus - 00,02 procent dla kontroli, n {{8} } każdy, P < 0,001;="" rysunek="" 1b,="" tabela="" uzupełniająca="" s1)="" i="" zmarł="" między="" wiekiem="" p20="" a="" p30="" (rysunek="" 1b).="" śmiertelność="" młodocianych="" w="" kohorcie="" mutantów="" była="" związana="">nerkowyawariaz ciężkiej choroby torbielowatej z poziomem azotu mocznikowego we krwi 68,40 plus -50,32 mg/dl dla myszy zmutowanych w porównaniu z 16,8 2.0 mg/dl dla kontroli ( n= 6 i 7, odpowiednio; P < 00,0001;="" rysunek="" 1b="" i="" c).="" ponadto="" u="" sześciu2-tfam/mutantów="" wystąpiła="" znacząca="" albuminuria="" (stosunek="" albuminy="" w="" moczu/kreatynina="" 43,58="" plus="" -3620,475,18="" mg/g="" u="" sześciu2-tfam/mutantów="" w="" porównaniu="" z="" 3,39="" mg/g="" w="" grupie="" kontrolnej="" w="" p14,="" odpowiednio="" n="6" i="" 10;="" p="">< 0,0001).="" jest="" to="" zgodne="" z="" wzorcem="" ekspresji="" rekombinazy="" cre="" w="" komórkach="" progenitorowych="" nefronu="" six2,="" które="" dają="" początek="" mezenchymom="">nerkowykanaliki i podocyty.15 W przeciwieństwie do sześciu2-Tfam-/- mutanty, myszy z heterozygotycznym niedoborem Tfam w komórkach progenitorowych SIX2 rozwijały się normalnie, były płodne i nie rozwijały się jawnienerkachoroba(rysunek uzupełniający S1).
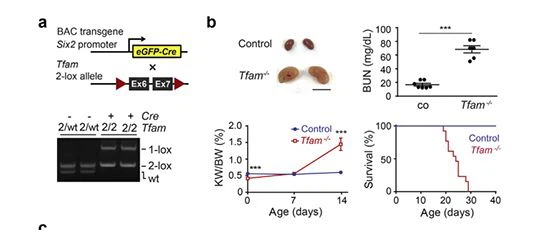

Rysunek 1|Inaktywacja Tfam w komórkach linii SIX2 powoduje ciężką chorobę torbielowatą i niewydolność nerek. (a) Schemat ilustrujący podejście eksperymentalne i lokalizację docelowych sekwencji w allelu floxed Tfam. Analiza reakcji łańcuchowej polimerazy całkowitego genomowego DNA nerki wyizolowanego z kontroli miotu (Cre ) i Six2-Tfam-/-myszy w wieku po urodzeniu dnia (P) 7; nierekombinujący allel Tfam floxed jest oznaczony przez 2-lox (2); allel rekombinowany według 1-lox, allel typu dzikiego według wt; þ lub - wskazuje na obecność lub brak transgenu Six2-eGFP/Cre. (b) Lewe panele, fotografie nerek z kontroli Cre i Six2-Tfam-/- myszy w wieku P20. Masy nerek (KW) są wyrażone jako procent masy ciała (BW) (n= 4-14). Prawe panele, poziomy azotu mocznikowego we krwi (BUN) w kontroli Cre (co) i Six2-Tfam-/-myszy w wieku P7 (odpowiednio n=7 i 6) oraz krzywe przeżycia Kaplana-Meiera dla kontroli Cre i szóstej 2-Tfam-/- myszy w porównaniu z testem log-rank (n=10–13). (c) Reprezentatywne obrazy utrwalonych w formalinie, zatopionych w parafinie skrawków nerki z kontroli Cre i Six2-Tfam-/-myszy w wieku P7 i P29 barwione hematoksyliną i eozyną (H&E) i analizowane immunohistochemicznie pod kątem aktyny a mięśni gładkich (ACTA2) i antygenu 31 różnicowania skupisk (CD) 31. Liczby przedstawiają struktury torbielowate, a gwiazdki przedstawiają kłębuszki. Pręty ¼ 1 mm dla przekrojów całej nerki, 100 mm dla obrazów H&E o dużej mocy i 50 mm dla obrazów IHC. Dane wyrażono jako średnią plus - SEM i analizowano za pomocą 2-ogólnego testu t Studenta. ***P < 0,001.="" aby="" zoptymalizować="" wyświetlanie="" tego="" obrazu,="" zapoznaj="" się="" z="" wersją="" online="" tego="" artykułu="" pod="" adresem="">
Analiza Sześciu2-Tfam-/- myszy, które również eksprymowały allel reporterowy Cre ROSA26-ACTB-tdTomato,-eGFP Cre, określany tu jako Six2-mT/mG;Tfam-/- myszy, co wskazuje, że zdecydowana większość struktur torbielowatychTfam-/- nerki pochodziły z komórek z historią ekspresji Six2-eGFP/Cre (rysunek uzupełniający S2). Cysty w sześciu2-Tfam-/- nerkiwykazały dowody proliferacji, jak wykazano w obecności Ki67-dodatnich komórek nabłonka wyścielających torbiele (średnio 40% wszystkich komórek nabłonkowych wyścielających torbiele), podczas gdy komórki dodatnie pod kątem rozszczepionej kaspazy 3 nie zostały wykryte w torbielach (rysunek uzupełniający S3 ). Odkrycia te są zgodne ze zwiększonymi poziomami fosforylowanej kinazy regulowanej sygnałem zewnątrzkomórkowym (p-ERK) i b-kateniny u Sześciu2-Tfam-/- tkanka nerkowa (rysunek uzupełniający S3). Z naszych danych wynika, że sześć2-Tfam-/- nerki wykazują cechy molekularne, które są często związane znerkowychoroby torbielowate.

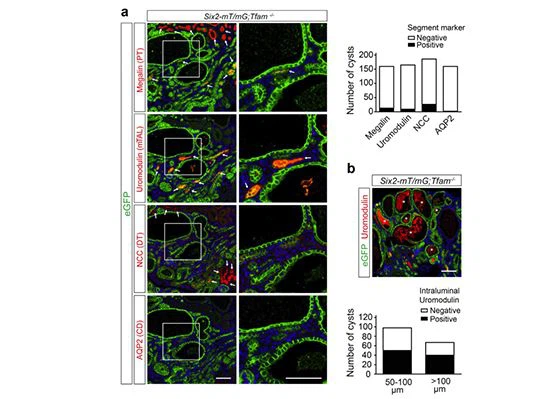
Rysunek 3 |Tfam-/-cysty nie wyrażają wspólnych markerów specyficznych dla segmentu nefronu. (a) Reprezentatywne obrazy utrwalonych w formalinie, zatopionych w parafinie skrawków nerki z Six2-mT/mG;Tfam-/-mice at age postnatal day (P) 14 stained for enhanced green fluorescent protein (eGFP), megalin, uromodulin, thiazide-sensitive sodium chloride cotransporter (NCC), and aquaporin 2 (AQP2) by immunofluorescence (IF). 4',6-diamidino-2-phenylindole was used for nuclear staining (blue fluorescence). Arrows depict tubular structures expressing respective nephron segment-specific markers. Nephron segment marker expression was assessed in cysts with a maximal diameter of >50 mm. (b) Reprezentatywne obrazy utrwalonych w formalinie, zatopionych w parafinie skrawków nerki z Six2-mT/mG;Tfam-/-myszy w wieku P14 barwione na eGFP i uromodulinę metodą IF. Gwiazdki przedstawiają cysty z uromoduliną w świetle światła. Obecność uromoduliny w świetle światła badano w torbielach o maksymalnej średnicy 50–100μm lub w cystach większych niż 100 mm w maksymalnej średnicy. Pręty=(a,b) 100 mm. Aby zoptymalizować wyświetlanie tego obrazu, zapoznaj się z wersją online tego artykułu pod adresemwww.kidney-international.org.

cistanchejest dobre dlanerka
Dojrzewanie nefronu jest wadliwe w Six2-Tfam-/-myszy
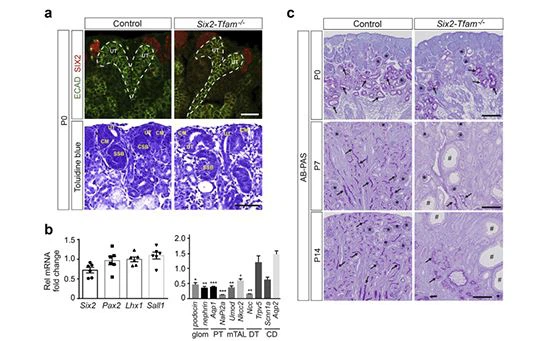
Ponieważ u myszy z tkankowo-specyficzną inaktywacją Tfam może upłynąć nawet kilka tygodni, rozwiną się patologia,17 następnie zbadaliśmy przebiegnerkowyrozwój choroby w szóstym roku2-Tfam-/-myszy. Pobraliśmy nerki od myszy kontrolnych i zmutowanych w wieku P0, P7 i P14 i zastosowaliśmy metody histologiczne, barwienie immunofluorescencyjne (IF) oraz analizę ekspresji genów w całościnerkawyciągi do oceny. Barwienie IF dla SIX2 i E-kadheryny w wieku P0 wykazało, że nerki z grupy kontrolnej i Six2-Tfam-/-były histologicznie podobne. Tworzenie się korowych struktur strefy nefrogennej, takich jak mezenchym kapelusza SIX2þ, końcówki moczowodów z ekspresją E-kadheryny i powstające struktury nefronowe, takie jaknerkowypęcherzyki oraz ciała w kształcie przecinka i litery S nie zostały zablokowane w Six 2-Tfam-/-nerki (ryc. 2a). Te odkrycia histologiczne były zgodne z poziomami ekspresji genów kodujących markery nefrogenne. Poziomy mRNA Six2, sparowanego pudełka 2 (Pax2), białka homeoboxu LIM 1 (Lhx1) i czynnika transkrypcyjnego typu Spalt 1 (Sall1) nie różniły się istotnie między kontrolą a szóstką2-Tfam-/- myszy w sumienerkahomogenaty z P0nerki(Rysunek 2b). Sugerowało to, że inaktywacja TFAM w progenitorach nefronu SIX2 nie wpłynęła znacząco na tworzenie struktur nefrogennych.
Chociaż tworzenie się powstającej struktury nefronu nie zostało zahamowane, barwienie błękitem alcjańskim/lektyną kwasu nadjodowego-Schiffa i lotosu tetragonolobus wykazało wadliwe dojrzewanie terminalnych nefronu w szóstym okresie 2-Tfam-/-myszy w wieku P{{0}}. Błękit alcjanowy/kwas nadjodowy–Schiffa, który barwi błony podstawne kanalików i rąbek szczoteczkowy, oraz lektyna lotosu tetragonolobus, która identyfikuje specyficzne oligosacharydy w rąbku szczoteczkowym komórek kanalików proksymalnych, uległy zmniejszeniu w zmutowanych nerkach. Rycina 2c przedstawia barwienie błękitem alcjanowym/kwasem nadjodowym – Schiffa w punktach czasowych P0, P7 i P14. Histochemia lektyny tetragonolobus lotosu i barwienie IF dla białka guza Wilmsa 1 w punktach czasowych P{{10}}, P7 i P14 przedstawiono na Rycinie Uzupełniającej S4. W wieku P0 względna powierzchnia, która wybarwiła się pozytywnie lektyną lotosu tetragonolobus wynosiła 2,10 procent, 00,51 procent i {{30},39 procent 0,1% w wieku P7 wobec 6,25% 0,28% i 6,2% 1,1% w grupie kontrolnej (odpowiednio n=3–4, P=0,0004 i 0,0007; Rysunek uzupełniający S4). Zgodnie z tymi odkryciami histologicznymi jest znaczący spadek ekspresji genów kodujących kłębuszkowe i specyficzne dla segmentu nefronowego markery podocynę, nefrynę, akwaporynę 1 (Aqp1), kotransporter fosforanu sodu 2a (NaPi2a), uromodulinę, kotransporter chlorku sodu 2 ( Nkcc2) i wrażliwy na tiazyd kotransporter chlorku sodu (Ncc) w Six 2-Tfam-/-myszy (rysunek 2b). Te dane razem wzięte sugerują, że Sześć2-Tfam-/- nerkiwykazują postępującą redukcję liczby dojrzałych proksymalnych segmentów nefronu i kłębuszków.
Ponieważ aktywność Six2-eGFP/Cre skutkuje powstaniem segmentów nefronów pochodzących z mezenchymów czapeczki z niedoborem TFAM, przewidzieliśmy, że dojrzewanie komórek nabłonka CD, które pochodzą z pączków moczowodowych, nie będzie zaburzone w przypadku Six{{2} }Tfam-/-nerki. Zgodnie z tym poglądem barwienie aglutyniną Dolichos biflorus, która reaguje z N-acetylo-D-galaktozą w kanalikach dystalnych i CD, wskazało na względną nadreprezentację aglutyniny Dolichos biflorus-dodatnich struktur w Six2-Tfam-/-nerki. W wieku P7 dodatnie zabarwione obszary pod kątem aglutyniny Dolichos biflorus stanowiły 13,91 procent 0,9 procent całkowitej powierzchni dla mutantów w porównaniu z 1,93 procent 0,1 procent dla kontroli (n=3, P={ {10}}.0002; Rysunek uzupełniający S4). Ekspresja mRNA podjednostki alfa kanału sodowego 1 nabłonka (Scnn1a) lub akwaporyny 2 (Aqp2), które są eksprymowane w komórkach nabłonka CD, nie była znacząco obniżona w porównaniu z kontrolą (Figura 2b). W przeciwieństwie do Sześciu2-Tfam-/-nerki, inaktywacja Tfam w komórkach progenitorowych homeobox B7 (HOXB7), które powodują wzrost komórek nabłonkowych CD, powodując utratę ekspresji markera nefronowego CD i łagodne rozszerzenie kanalików, ale nie cystogenezę (rysunek uzupełniający S5). Podsumowując, nasze dane wskazują, że utrata funkcji TFAM w komórkach progenitorowych SIX2 nie blokuje rozwoju powstających struktur nefronu, ale hamuje końcowe dojrzewanie nefronu.


Tfam-/-torbiele mają niedobór wspólnych markerów segmentu nefronu
Aby scharakteryzować pochodzenie histogenetyczneTfam-/- nerkowycyst, wykonaliśmy analizy IFTfam-/- nerkiat age P14 and examined the expression of nephron segment markers megalin (proximal tubule), uromodulin (medullary thick ascending limb of Henle), thiazide sensitive sodium chloride cotransporter (distal tubule), and aquaporin 2 (CD). The majority of cysts with a maximal diameter of >50 mm did not express these segment-specific markers, indicating a lack of cellular differentiation (Figure 3a, Supplementary Figure S6). Furthermore, approximately 50% of cysts with a maximal diameter of >50 mm charakteryzowały się śródluminowymi złogami uromoduliny, co sugerowało wychodzenie z odcinków nefronu dystalnych do kanalika proksymalnego i zstępującej pętli Henlego (ryc. 3b).
Postępujące nieprawidłowości w funkcji i morfologii mt wTfam-/- komórki nabłonkowe
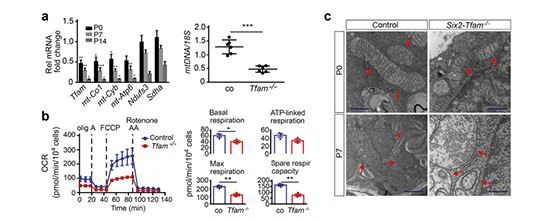
Aby scharakteryzować przebieg w czasie metabolicznych konsekwencji delecji Tfam, najpierw zbadaliśmy poziomy mRNA Tfam i regulowanego przez TFAM mt-Co1, mt-Cyb i mt-Atp6 wTfam-/- nerkiw wieku P0, P7 i P14. Zgodnie z oczekiwaniami, poziomy mRNA Tfam, mt-Co1, mt-Cyb i mt-Atp6 były znacząco obniżone (Figura 4a).Tfam-/-komórki nabłonkowe znakowane eGFP (sześć{{0}}mT/mG; Tfam/myszy) wykazywały znaczące zmniejszenie ekspresji białka MT-CO1 (rysunek uzupełniający S7). Liczba kopii DNA mt została zmniejszona o 63 procent, co jest zgodne z niedoborem mt, cechą charakterystyczną niedoboru TFAM (Figura 4a). W przeciwieństwie do tego ekspresja genów jądrowych kodujących dinukleotyd nikotynoamidoadeninowy: podjednostkę rdzeniową 3 oksydoreduktazy ubichinonowej (Ndufs3) i podjednostkę A kompleksu dehydrogenazy bursztynianowej (Sdha) nie uległa zmianie w wieku P0, ale została zmniejszona w wieku P7 i P14 (Figura 4a). Te wyniki analizy genu mt i białka są zgodne z postępującą utratą liczby kopii mt w Tfam/nabłonku.
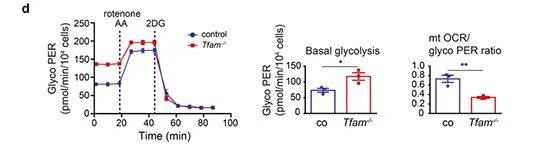
Następnie zbadaliśmy efekty metaboliczne inaktywacji Tfam w pierwotnych komórkach nabłonka kanalików proksymalnych (PTEC) izolowanych w wieku P7.Tfam-/- PTEC wykazywały znaczne zmniejszenie podstawowych wskaźników zużycia tlenu (40.77 4.10 dla mutantów w porównaniu z 61.75 5.18 pmol/min/104 komórek dla kontroli, n=3 każda, P =0.034), oddychanie sprzężone z ATP (33.11 3.91 dla mutantów vs. 46.92 4.91 pmol/min/104 komórek dla kontroli, n{{18} } każdy, P=0.093), maksymalne oddychanie (116.8 14.19 dla mutantów vs. 225.5 13.55 pmol/min/104 komórek dla kontroli, n{{ 28}} każdy, P=00,005) i wolna pojemność oddechowa (76.05 100,18 dla mutantów vs. 163.7 8.61 pmol/min/104 komórek dla kontroli , n =3 każdy, P=0.003; Rysunek 4b).
Aby dalej scharakteryzować stopień wyczerpania i uszkodzenia mt, zbadaliśmyTfam-/- nerkiza pomocą transmisyjnej mikroskopii elektronowej i {{0}}wymiarowej strukturalnej mikroskopii oświetleniowej (3D SIM). W wieku P7 mitochondria wykazywały nieregularne kształty i balony, co jest zgodne z wcześniejszymi odkryciami u myszy z nokautem Tfam. Analiza transmisyjnego mikroskopu elektronowego wykazała, że nieprawidłowości strukturalne mitochondriów, takie jak zwiększony rozmiar i nieprawidłowe grzebienie, postępowały po urodzeniu, ponieważ różnice morfologiczne między mutantami a grupą kontrolną były mniej widoczne w wieku P0 i stawały się bardziej nasilone z wiekiem (ryc. 4c). ). 3D SIM został użyty do zbadania objętości mt i rozmiaru sieci w Six2-mT/mG; Tfam / mutanty w porównaniu z sześcioma myszami kontrolnymi 2-mT/mG w wieku P7; Objętość mt mierzono w przekrojach 5 do 8 kanalików na skrawek, badając 25 do 4 0 eGFP-dodatnich komórek nabłonka kory wybarwionych pod kątem zależnego od napięcia anionselektywnego kanału 1 przez barwienie IF. Stwierdziliśmy, że całkowita objętość mt na komórkę dodatnią pod względem eGFP była znacząco zmniejszona (62.66 16.46 mm3/komórkę dla mutantów vs. 177.4 30.17 mm3 /komórkę dla kontroli, n=3 każda , P ¼ 0.0289) i było związane ze zmianą stosunku całkowitej objętości mt do całkowitej objętości komórek z 0.230 0.01 w kontroli do 0.{{ 33}}0,016 w Six2-Tfam / mutanty (n=3 każdy, P=0,0017; Rysunek 4c). Maksymalny rozmiar sieci mt, który mierzy największą sieć mt napotkaną we wszystkich zbadanych komórkach eGFP-dodatnich, został zmniejszony w sześciu 2-Tfam-/- nerki(143,2 23,2 mm3 dla mutantów vs. 318.3 49,45 mm3 dla kontroli, n=3, P=00,0327). Podsumowując, wyniki badań ultrastrukturalnych i SIM oraz wyniki analizy genu mt i białka są zgodne z postępującą utratą liczby kopii mt wTfam-/- nabłonek.

Cistanchejest dobre dlawielotorbielowatość nerek
Niedobór TFAM przesuwa metabolizm nabłonka nerkowego w kierunku glikolizy
PTEC wnerkawykorzystują b-oksydację kwasów tłuszczowych i OXPHOS do generowania ATP i są glukoneogenetyczne.18 Aby uzyskać dodatkowy wgląd w zmiany metaboliczne związane z inaktywacją Tfam, przeprowadziliśmy analizę sekwencjonowania RNAnerkiod szóstki2-Tfam-/-i myszy kontrolne z miotu Cre w wieku P7. Odkryliśmy, że kluczowe geny regulatorowe zaangażowane w glikolizę, takie jak heksokinaza 2 (Hk2) i enolaza 2 (Eno2), uległy regulacji w górę. Natomiast ekspresja większości genów zaangażowanych w cykl kwasów trikarboksylowych była obniżona (np. dehydrogenaza izocytrynianowa 1 [Idh1]), podobnie jak ekspresja genów zaangażowanych w b-oksydację kwasów tłuszczowych, takich jak acylotransferaza 1B acetylo-koenzymu A ( Acaa1b), średniołańcuchowa dehydrogenaza acylo-koenzymu A (Acadm) (rysunek 5a i b, rysunek uzupełniający S8). Zgodnie ze zmniejszoną ekspresją genów biorących udział w cyklu kwasów trikarboksylowych - geny utleniania było akumulacją obojętnych lipidów, co wykryto za pomocą barwienia czerwieni olejowej O w zamrożonychnerkaprzekroje w wieku P14 (Rysunek 5c).


Zmniejszona ekspresja TFAM w mysich i ludzkich tkankach PKD jest związana z niedoborem mt
Ponieważ Sześć2-Tfam-/- nerkinosiła silne podobieństwo do PKD(wielotorbielowatość nerek) nerki, następnie oceniliśmy, czy TFAM był rozregulowany w PKD(wielotorbielowatość nerek)tkanki. Najpierw zbadaliśmy ekspresję genów regulowaną przez TFAM i TFAM w 2 dobrze znanych genetycznych mysich modelach PKD. Poziomy mRNA Tfam były znacznie zmniejszone w homogenatach całej nerek z Pkd-/- i Cyscpk/cpkmyszy, które niosą mutacje w PKD1(wielotorbielowatość nerek)lub Cys1. Wiązało się to ze spadkiem ekspresji mitochondrialnych i jądrowych genów mt oraz rozregulowaną ekspresją genów glikolitycznych. Podobny do Sześciu2-Tfam-/-nerki, PKD(wielotorbielowatość nerek)-/- i Cyscpk/cpk nerkicharakteryzowały się podwyższonymi poziomami Eno2 i Hk2 oraz istotnie obniżonymi poziomami transkryptu kinazy fosfoglicerynianowej (Pgk) 1, kinazy dehydrogenazy pirogronianowej (Pdk) 1 i Pdk4 (Figura 6a). Ekspresja białka TFAM, oceniana przez barwienie IF, była zmniejszona w komórkach nabłonkowych wyściełających torbiele w porównaniu z komórkami nabłonkowymi z sąsiednich kanalików nietorbielowatych (Figura 6b). Było to związane ze zmniejszoną ekspresją mt-Co1 i mt-Atp6 przez hybrydyzację fluorescencji RNA in situ (Rysunek 6b, Rysunek uzupełniający S9); objętość mt, określona przez 3D SIM, została zmniejszona o 55 procent w porównaniu z komórkami nabłonka z sąsiednich kanalików nietorbielowatych lub PTEC z normalnej kontrolinerki. Nie stwierdzono różnic w objętości mt między prawidłowymi kontrolnymi PTEC i PTEC z kanalików nietorbielowatych (ryc. 6c).
Aby zbadać, czy utrata ekspresji TFAM jest powszechną cechą molekularną ludzkiej PKD(wielotorbielowatość nerek), przeanalizowaliśmy próbki nefrektomii od 5 pacjentów z ADPKD za pomocą immunohistochemii, barwienia IF, hybrydyzacji fluorescencji RNA in situ i 3D SIM. Zmniejszoną ekspresję TFAM zaobserwowano u 75,2 proc. plus -7,5 procnerkowycysty analizowane immunohistochemicznie. Było to związane ze zmniejszoną ekspresją MT-CO1 i MT-ATP6 przez hybrydyzację fluorescencji RNA in situ (Rysunek 7a, Rysunek uzupełniający S10); Objętość mt w komórkach nabłonka wyściełającego torbiele zmniejszyła się o około 70 procent, jak oceniono za pomocą 3D SIM (ryc. 7b). Podsumowując, analiza 2 PKD(wielotorbielowatość nerek)modele mysie i ludzkie tkanki ADPKD sugerowały, że niedobór TFAM i niedobór mt są częstymi objawami w PKD(wielotorbielowatość nerek)tkanek i prawdopodobnie wpłyną na patogenezęnerkowychoroba torbielowata.



Cistanche jest dobre dlawielotorbielowatość nerek
Dyskusja
Kliknij tutaj, aby uzyskać informacje o Części II (Dyskusja) tego artykułu.
Wyciąg z: 'Nerkaniedobór mitochondrialnego czynnika transkrypcyjnego A ukierunkowany na nabłonek skutkuje postępującą deplecją mitochondrialną związaną z ciężką chorobą torbielowatą” Ken Ishii1,2,11 et al.
---NerkaMiędzynarodowy (2021) 99, 657–670
