Glikozydy fenyloetanoidowe Cistanche Tubulosa indukują apoptozę w komórkach Eca‑109 poprzez szlak zależny od mitochondriów
Mar 06, 2022
Kontakt: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
CHANGSHUANG FU , JINYU LI , ADILA AIPIRE , LIJIE XIA , YI YANG , QIUYAN CHEN , JIE LV , XINHUI WANG i JINYAO LI
Abstrakcyjny
Cistanche tubulosapełni różne funkcje biologiczne. W niniejszej pracy badano działanie przeciwnowotworowe rozpuszczalnych w wodzie glikozydów fenyloetanoidowych C. tubulosa (CTPG-W) na raka przełyku. Komórki Eca-109 traktowano CTPG-W, a żywotność komórek mierzono testem MTT. Apoptozę, cykl komórkowy, potencjał błony mitochondrialnej (Δψm) i reaktywne formy tlenu analizowano za pomocą cytometrii przepływowej. Poziomy białek w szlakach apoptotycznych wykryto za pomocą analizy Western blot. Stwierdzono, że CTPG‑W znacząco zmniejsza żywotność komórek Eca-109 poprzez indukcję apoptozy i zatrzymanie cyklu komórkowego. Po leczeniu CTPG-W, Δψm Eca-109 uległ znacznemu zmniejszeniu, co jest związane z podwyższonymi poziomami chłoniaka z komórek B-2 (Bcl-2) i obniżonymi poziomami Bcl-2. W konsekwencji, poziomy kinazy końcowej NH2- cytochromu c i c-Jun wzrosły, co spowodowało wzrost poziomu polimerazy rozszczepionej poli (ADP-rybozy) i rozszczepionej kaspazy-3, {{18} } i -9, ale nie kaspazy-8. Odpowiednio, poziomy reaktywnych form tlenu w komórkach Eca-109 wykazały znaczące zmiany. Wyniki te wskazują, że CTPG-W indukował apoptozę komórek Eca-109 poprzez szlak zależny od mitochondriów.
Wstęp
Rak przełyku jest jednym z najczęstszych typów raka z 11-tym najwyższym wskaźnikiem zachorowalności i 6-tym najwyższym wskaźnikiem śmiertelności na świecie i spowodował ~439,000 śmiertelności w 2015 roku (1). Częstość występowania raka przełyku różni się znacznie w różnych regionach, przy czym w 2012 r. najwyższe wskaźniki zachorowalności miały wschodnia Azja oraz wschodnia i południowa Afryka, a najniższe w Afryce Zachodniej (1,2). W Chinach szacunkowa liczba przypadków raka przełyku i śmiertelność wyniosła odpowiednio 477 000 i 375 000 w 2015 r. (3). Chociaż wskaźnik zachorowalności na raka przełyku zmniejszył się w krajach o średnim i wysokim średnim wskaźniku socjodemograficznym w latach 2005–2015, wskaźnik umieralności pozostaje wysoki ze względu na złe rokowania (1,4). Połączenie chirurgicznej resekcji z chemioterapią lub radioterapią było stosowane w leczeniu raka przełyku, jednak doniesiono, że w latach 2003-2014 wskaźnik przeżycia 5-lat utrzymywał się<20% in="" china,="" the="" usa,="" and="" europe="" (4,5).="" for="" these="" reasons,="" it="" is="" urgent="" to="" develop="" novel="" therapeutic="" agents="" to="" treat="" esophageal="">
Tradycyjna chińska medycyna ziołowa (CHM) jest stosowana w leczeniu różnych typów raka, w tym niedrobnokomórkowego raka płuc (6), raka jelita grubego (7), raka wątrobowokomórkowego (8). Ostatnio badania kliniczne wykazały, że skojarzenie CHM z chemioterapią lub radioterapią nie tylko przyniosło szereg korzyści w zakresie jakości życia i złagodziło skutki uboczne wywołane chemioterapią lub radioterapią (9,10), ale także poprawiło przeżywalność pacjentów z niedrobnokomórkowym rakiem płuc, wątroby, żołądka, jelita grubego, nosogardzieli lub szyjki macicy (9). Istnieją jednak sprzeczne dowody dotyczące skuteczności leczenia CHM w przypadku raka przełyku (10,11). Liczne badania wykazały, że wiele leków lub składników ziołowych może hamować wzrost komórek raka przełyku in vitro i in vivo, w tym Andrographis paniculata (12,13), Daikenchuto (14), icariin (15), Rosa Roxburghii Tratt i Fagopyrum Cymosum (16), Jaridonin (17), Marsdenia tenacissima (18), OP16 (nowy diterpenoid ent-kaurenowy) (19), Qigesan (20) i wywar Tonglian (21). Cistanche jest rodzajem CHM i pełni różne funkcje biologiczne, w tym antyoksydacyjne, przeciwzapalne i neuroprotekcyjne (22,23). Nasze poprzednie badanie wykazało, żeGlikozydy fenyloetanoidowe Cistanche tubulosa(CTPG) może hamować wzrost komórek czerniaka B16-F10 in vitro i in vivo (24). Jednak słaba rozpuszczalność w wodzie wcześniej stosowanego CTPG ogranicza rozwój leku (24). W związku z tym zastosowano rozpuszczalny w wodzie CTPG (CTPG-W) i zbadano działanie przeciwnowotworowe na komórki raka przełyku (Eca-109). Ustalono, że CTPG-W może w sposób zależny od dawki hamować żywotność komórek Eca-109 poprzez indukcję apoptozy na szlaku zależnym od mitochondriów.
Materiały i metody Zwierzęta.
Samice myszy C57BL/6 (6-8 tygodnie, ~25 g) zakupiono w Beijing Laboratory Animal Research Center (Pekin, Chiny) i trzymano w kontrolowanej temperaturze (25˚C) z cyklem świetlnym (12/ 12) Ośrodek dla Zwierząt Uniwersytetu Xinjiang (Urumqi, Chiny). Wszystkie zwierzęta otrzymywały wodę i karmę wolną od patogenów.
Linia komórkowa i hodowla. Ludzka linia komórkowa raka przełyku (Eca-109) została zachowana przez Kluczowe Laboratorium Zasobów Biologicznych i Inżynierii Genetycznej w Xinjiang (Kolegium Nauk Przyrodniczych i Technologii, Uniwersytet Xinjiang, Urumqi, Chiny) i hodowana w RPMI{{1} } podłoże (Gibco; Thermo Fisher Scientific, Inc., Waltham, MA, USA) uzupełnione 10% inaktywowaną termicznie płodową surowicą bydlęcą (FBS; MRC, EN MOASAI Biological Technology Co., Ltd, Jiangsu, Chiny), 1 procent L -glutamina (100 mM), 100 U/ml penicyliny i 100 µg/ml streptomycyny w 37°C w wilgotnej atmosferze zawierającej 5% CO2.
Wysokosprawna chromatografia cieczowa (HPLC). CTPG-W (nr kat. SGJG20170410) zakupiono od Shanghai Upbio Tech Co., Ltd. (Szanghaj, Chiny). Główne związki CTPG sklasyfikowano i oznaczono ilościowo metodą HPLC zgodnie z naszym poprzednim badaniem (24). W skrócie, HPLC przeprowadzono na kolumnie ZORBAX SB‑C18 (250x4,6 mm; 5 µm) w 30˚C i eluowano 0,2% roztworem kwasu mrówkowego i gradientem metanolu zaczynającym się od 23%, dodając 1 ml co minutę przez 45 min, aż do osiągnięcia 31 proc. Łącznie 10 µl próbki wstrzyknięto i wykryto przy 330 nm. Wzorzec echinakozydu zakupiono od Shanghai Baoban Biotech Co., Ltd. (Szanghaj, Chiny), a wzorzec akteozydu zakupiono od Sigma-Aldrich (Merck KGaA, Darmstadt, Niemcy). Wzorce zostały wykorzystane do analizy składników CTPG-W.
Test MTT. Proliferację komórek mierzono testem MTT. Komórki Eca{{0}} inokulowano do 96-dołkowych płytek przy gęstości 5x103 komórek w 100 µl RPMI{{5 }} medium/studzienkę i hodowane w 37˚C przez 24 h, a następnie traktowane różnymi stężeniami (0, 200, 400, 600 i 800 µg/ml) CTPG-W lub 0,4% dimetylosulfotlenku (DMSO) przez 24, 48 i 72 godz. Jako kontrolę rozpuszczalnika zastosowano DMSO (800 ug/ml CTPG-W zawierający 0,4% DMSO). Jako kontrolę pozytywną zastosowano cisplatynę (20 µg/ml). Następnie supernatant odrzucono po odwirowaniu przy 225 xg przez 5 min w temperaturze pokojowej i do każdego dołka dodano 100 µl roztworu MTT (0,5 mg/ml w pożywce RPMI-1640 bez FBS) i inkubowano w 37˚C przez 3 godz. Utworzone kryształy formazanu rozpuszczono w 200 µl DMSO. Wartości gęstości optycznej (OD) mierzono przy długości fali 490 nm za pomocą czytnika mikropłytek 96-dołkowych (Bio-Rad Laboratories, Inc., Hercules, CA, USA). Względną żywotność komórek obliczono według wzoru: Żywotność komórek (procent)=(ODtraktowany/ODnietraktowany)x100 procent. Morfologię komórek Eca‑109 obserwowano za pomocą odwróconego mikroskopu fluorescencyjnego (powiększenie, x200) (Nikon Eclipse Ti‑E; Nikon Corporation, Tokio, Japonia).
W celu proliferacji splenocytów myszy C57BL/6 uśmiercono przez zwichnięcie szyjki macicy i wyizolowano śledziony. Przygotowano zawiesinę pojedynczych komórek i splenocyty wysiano na 96-dołkowe płytki z gęstością 1x105 komórek/dołek w 100 µl pożywki RPMI-1640, a następnie potraktowano różnymi stężeniami (0, 200, 400, 600 i 800 µg/ml) CTPG-W przez 24, 48 i 72 godziny w 37˚C z 5% CO2. Proliferację splenocytów mierzono testem MTT, zgodnie z wyżej wymienionym protokołem. Wskaźnik stymulujący=ODleczony/ODnieleczony.
Pomiar apoptozy i cyklu komórkowego. Komórki Eca{{0}} hodowano na szalkach 60 mm przy gęstości 2,5x105 komórek/płytkę przez 24 godziny i traktowano różnymi stężeniami ({{31} }, 200, 400, 600 i 800 µg/ml) CTPG-W lub 0,4% DMSO przez 24 godziny w 37˚C z 5% CO2. Komórki zebrano i wybarwiono za pomocą zestawu do wykrywania apoptozy aneksyny V-fluoresceiny (FITC)/jodku propidyny (PI) (Shanghai Shengsheng Biotechnology Co., Ltd., Szanghaj, Chiny), zgodnie z protokołami producenta. Próbki zbierano metodą cytometrii przepływowej (BD FACSCalibur; BD Biosciences, Franklin Lakes, NJ, USA) i analizowano za pomocą FlowJo 7.6 (Tree Star, Inc., Ashland, OR, USA). Aby przeanalizować wpływ CTPG-W na cykl komórkowy, 2,5x105 komórek Eca-109 wysiano na 60 mm szalkach hodowlanych i potraktowano CTPG-W (0, 100, 200 i 400 µg/ml) lub 0,4 procent DMSO przez 24 godziny w 37˚C z 5 procentami CO2. Wszystkie komórki zebrano i dwukrotnie przemyto lodowatym PBS (Gibco; Thermo Fisher Scientific, Inc.), a następnie utrwalono w 70 procentowym lodowatym etanolu w 4°C przez 30 min. Po dwukrotnym przemyciu lodowatym PBS komórki ponownie zawieszono w 300 µl buforu do barwienia PI/RNazy (BD Biosciences, San Jose, CA, USA) na 10 minut w temperaturze pokojowej. Rozkład cyklu komórkowego analizowano za pomocą oprogramowania ModFit LT 3.0 metodą cytometrii przepływowej (BD FACSCalibur).
Analiza potencjału błony mitochondrialnej (Δψm) i reaktywnych form tlenu (ROS). Aby przeanalizować Δψm, komórki Eca{{0}} potraktowano CTPG-W (0, 400, 600 i 800 µg/ml) lub 0,4% DMSO przez 24 h w 37˚C z 5% CO2 i wybarwione zestawem testowym potencjału błony mitochondrialnej z JC-1 (Beyotime Institute of Biotechnology, Szanghaj, Chiny), zgodnie z protokołem producenta, przez 20 min w 37˚C . Po dwukrotnym przemyciu buforem do płukania JC-1 (Beyotime Institute of Biotechnology), próbki ponownie zawieszono w 300 µl buforu do płukania JC‑1 i analizowano metodą cytometrii przepływowej (BD FACSCalibur). Fluorescencję barwnika JC‑1 w komórkach Eca‑109 obserwowano również za pomocą odwróconego mikroskopu fluorescencyjnego (powiększenie, x200; Nikon Eclipse Ti‑E). Do analizy ROS komórki Eca-109 traktowano CTPG-W (0, 400, 600 i 800 µg/ml) przez 2, 4, 6, 12 i 24 godziny i barwiono reaktywnymi gatunkami tlenu Assay Kit (Beyotime Institute of Biotechnology), zgodnie z protokołem producenta, przez 20 min w 37˚C. Po trzykrotnym przemyciu lodowatym PBS próbki zebrano metodą cytometrii przepływowej (BD FACSCalibur) i przeanalizowano za pomocą oprogramowania FlowJo 7.6.
Aktywność zmiatania rodników 2,2-difenylo-1-pikrylohydrazylowych (DPPH). Aktywność zmiatania wolnych rodników CTPG-W została określona w teście wolnych rodników DPPH zgodnie z opublikowanym protokołem z niewielką modyfikacją, ponieważ metanol został zastąpiony etanolem w celu rozpuszczenia DPPH (25, 26). Do pomiarów w stanie stacjonarnym, 150 µl DPPH (100 mmol/l) w etanolu zmieszano z różnymi stężeniami CTPG-W (25, 50, 75, 100, 250, 300, 400, 500 i 600 µg/ml) w 50 µl PBS i inkubowano w ciemności przez 30 min w temperaturze pokojowej. Absorbancję przy 517 nm wykrywano w obecności i nieobecności CTPG-W. Łącznie 50 µl witaminy C zastosowano jako kontrolę pozytywną. Aktywność wymiatania rodników DPPH obliczono ze wzoru: Wychwytywanie ( procent )=[1-(Próbka-ślepa)/A0]x100, gdzie Ślepa jest absorbancją kontroli (bez DPPH), Próbka to absorbancja próbki, a A0 to absorbancja PBS z DPPH.
Analiza Western blot. Komórki Eca{{0}} traktowano CTPG-W (0, 200, 600 µg/ml) lub 0,4% DMSO przez 24 godziny w 37°C z 5% CO2. Po dwukrotnym przemyciu PBS komórki poddano lizie w buforze do lizy radioimmunoprecypitacyjnej (Beijing ComWin Biotech Co., Ltd., Pekin, Chiny) przez 20 min na lodzie. Po odwirowaniu przy 10,000 xg przez 10 min w 4°C zebrano supernatanty i wykryto stężenia białka za pomocą zestawu kwasu bicynchoniowego (Thermo Fisher Scientific, Inc.) zgodnie z protokołami producenta. Analizę Western blot przeprowadzono zgodnie z naszym poprzednim opisem (24). Przeciwciała przeciwko kaspazie-7 (nr kat. D120077), kaspazie-8 (nr kat. D155240), kaspazie-9 (nr kat. D220078), chłoniakowi z komórek B{ {24}} (Bcl-2) X (Bax) (nr kat. D220073) i Bcl-2 (nr kat. D260117) oraz anty-mysia IgG-peroksydaza chrzanowa (HRP ) (nr kat. D111050) i przeciwkrólicze IgG-HRP (nr kat. D110058) zakupiono z BBI Life Sciences (Szanghaj, Chiny). Przeciwciała przeciwko kaspazie-3 (nr kat. E-AB-10050) i aktywnej kaspazie-3 (nr kat. E-AB-22115) zostały zakupione w firmie Elabscience ( Wuhan, Chiny). Inne przeciwciała przeciwko kaspazie-7 (nr kat. 9492), polimerazie poli(ADP-rybozy) (PARP) (nr kat. 9542), cytochromowi c (nr kat. AC909), c-Jun NH{ {48}} kinazę końcową (JNK) (nr kat. 9252S) i -aktynę (nr kat. 58169) otrzymano z Cell Signaling Technology, Inc. (Danvers, MA, USA). Wszystkie przeciwciała pierwszorzędowe i drugorzędowe rozcieńczono w stosunku 1:1 000. Pierwszorzędowe przeciwciała inkubowano w 4˚C przez noc, a drugorzędowe przeciwciała inkubowano w 37˚C przez 1 godz.

Białka docelowe wykrywano za pomocą zestawu do wzmocnionego testu chemiluminescencji (Beyotime Institute of Biotechnology), zgodnie z protokołem producenta.
Analiza statystyczna. Istotność statystyczną obliczono za pomocą jednokierunkowej analizy wariancji testem post hoc Tukeya, a wyniki analizowano przy użyciu oprogramowania GraphPad Prism 5.0 (GraphPad Software, La Jolla, CA, USA) wśród grup leczonych i kontrolnych. Wszystkie dane przedstawiono jako średnią ± odchylenie standardowe. P<0.05 was="" considered="" to="" indicate="" a="" statistically="" significant="">

Glikozydy fenyloetanoidowe Cistanche tubulosa(CTPG)
Wyniki
CTPG‑W hamuje wzrost komórek Eca‑109. Składniki CTPG-W sklasyfikowano i oznaczono ilościowo metodą HPLC (ryc. 1), które porównano ze standardami echinakozydu i akteozydu. Zgodnie z czasami retencji pików i powierzchniami pików, CTPG-W zawierał 39,16 procent echinakozydu i 2,44 procent akteozydu. Po pierwsze, wpływ CTPG-W na żywotność komórek Eca-109 określono za pomocą testu MTT. CTPG-W rozpuszczono w DMSO przy 200 mg/ml i rozcieńczono pożywką RPMI-1640 zawierającą 10 procent inaktywowanej termicznie FBS do wskazanych stężeń. Komórki Eca-109 traktowano CTPG-W, a żywotność komórek analizowano za pomocą testu MTT we wskazanych punktach czasowych. Leczenie CTPG‑W znacząco zmniejszyło żywotność komórek Eca-109 w sposób zależny od dawki i czasu (P<0.001; fig.="" 2a).="" the="" morphology="" of="" eca-109="" cells="" was="" observed="" with="" an="" inverted="" fluorescence="" microscope="" (magnification,="" x200)="" following="" ctpg‑w="" treatment="" for="" 24="" h,="" which="" changed="" notably="" in="" a="" dose-dependent="" manner,="" with="" the="" cells="" shrinking="" and="" becoming="" round="" following="" ctpg-w="" treatment="" (fig.="" 2b).="" these="" results="" indicate="" that="" ctpg-w="" suppresses="" the="" growth="" of="" eca-109="" cells.="" the="" effect="" of="" ctpg-w="" on="" the="" proliferation="" of="" splenocytes="" was="" also="" detected="" with="" an="" mtt="" assay.="" ctpg-w="" significantly="" promoted="" the="" proliferation="" of="" splenocytes="" in="" a="" dose-dependent="" manner="" (fig.="" 2c),="" indicating="" that="" it="" has="" no="" cytotoxic="" effect="" on="">
CTPG‑W indukuje apoptozę w komórkach Eca‑109. Aby zbadać, czy CTPG-W hamował wzrost komórek Eca-109 poprzez indukcję apoptozy lub martwicy, komórki traktowano różnymi stężeniami CTPG-W. Po 24 godzinach apoptozę i martwicę komórek Eca-109 wykryto za pomocą barwienia aneksyną V/PI. Jak przedstawiono na Fig. 3A, komórki aneksyna V-/PI plus bramkowano jako komórki nekrotyczne, a komórki aneksyna V plus/PI plus i aneksyna V plus/PI- bramkowano jako komórki apoptotyczne. CTPG-W indukował przede wszystkim apoptozę komórek Eca-109 w sposób zależny od dawki, chociaż martwicze komórki Eca-109 również znacznie wzrosły pod wpływem leczenia 600 i 800 µg/ml CTPG-W (P<0.001 at="" 600="" µg/ml="" and=""><0.05 at="" 800="" µg/ml).="" consistently,="" the="" levels="" of="" pro-apoptotic="" bax="" and="" anti-apoptotic="" bcl-2="" in="" eca-109="" cells="" were="" upregulated="" and="" downregulated,="" respectively,="" upon="" ctpg-w="" treatment="" (fig.="" 3b).="" the="" results="" indicated="" that="" ctpg-w="" primarily="" inhibited="" the="" growth="" of="" eca-109="" cells="" through="" the="" induction="" of="">
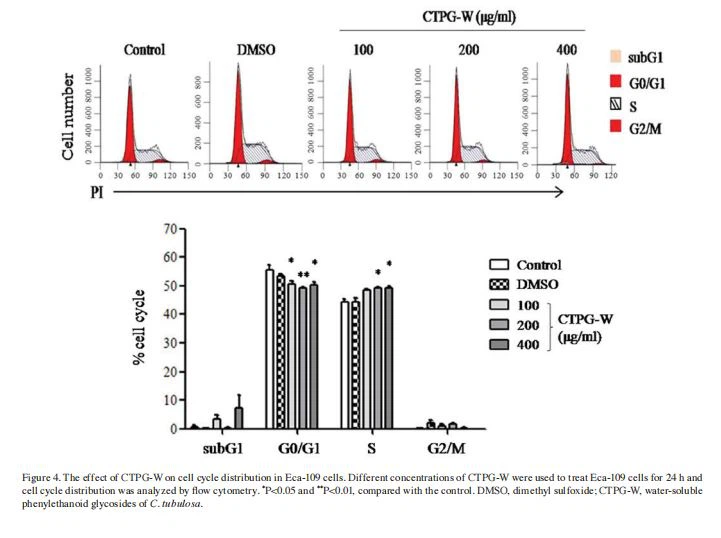
CTPG‑W indukuje zatrzymanie cyklu komórkowego w fazie S w komórkach Eca‑109. Zakłócenie cyklu komórkowego raka hamuje wzrost komórek i promuje apoptozę (27). Rozkład cyklu komórkowego w komórkach Eca-109 wykrywano za pomocą barwienia PI po traktowaniu CTPG-W przez 24 godziny. Zaobserwowano, że komórki w fazie S wzrosły, a komórki w fazach G0/G1 wykazały ogólny istotny spadek po leczeniu CTPG‑W (P<0.05; fig.="" 4),="" indicating="" that="" ctpg-w="" arrests="" the="" eca-109="" cell="" cycle="" at="" the="" s="">
CTPG‑W zmniejsza Δψm i indukuje uwalnianie cytochromu c. Apoptozę można wywołać szlakiem zależnym od mitochondriów (28,29). Pro- i antyapoptozy członkowie rodziny białek BCL-2 pełnią ważną rolę w regulacji integralności błony mitochondrialnej (30,31). Po leczeniu CTPG-W przez 24 godziny, m oceniano za pomocą barwienia JC‑1. Agregat JC‑1 (czerwona fluorescencja wykryta w FL‑2) rozpadnie się na monomer (zielona fluorescencja wykryta w FL-1), gdy Δψm się zmniejsza (32). Jak przedstawiono na ryc. 5A, częstości komórek FL-1 plus FL-2-/plus znacząco wzrosły w sposób zależny od dawki, co wskazuje na zmniejszenie Δψm komórek Eca‑109. Zmiany fluorescencji w komórkach Eca‑109 obserwowano również za pomocą odwróconego mikroskopu fluorescencyjnego (ryc. 5B). Wraz ze wzrostem stężeń CTPG‑W czerwona fluorescencja zmniejszyła się, a zielona fluorescencja wzrosła, co jest zgodne z danymi z cytometrii przepływowej. Zaobserwowano również znaczny wzrost poziomu cytochromu c w cytozolu (ryc. 5C), co jest wynikiem zmniejszenia Δψm. Potwierdza to wniosek wyciągnięty ze zwiększonej liczby komórek FL-1 plus FL-2-/plus, których Δψm zmniejszył się w wyniku leczenia CTPG-W. Doniesiono, że JNK może regulować aktywację rodziny białek BCL-2, powodując uwalnianie cytochromu c (33-35). Ustalono również, że poziom JNK był znacznie podwyższony po leczeniu CTPG-W (ryc. 5C). Wyniki wskazują, że CTPG-W może indukować apoptozę komórek Eca-109 poprzez szlak zależny od mitochondriów.

Wpływ CTPG‑W na wewnątrzkomórkowe wytwarzanie ROS. ROS może zmniejszyć Δψm w celu wywołania apoptozy (36). Aby zbadać, czy CTPG-W może zwiększyć produkcję ROS, komórki Eca-109 potraktowano różnymi stężeniami CTPG-W. Komórki zbierano we wskazanych punktach czasowych i barwiono DCFH-DA. Wytwarzanie wewnątrzkomórkowych ROS w komórkach Eca-109 określono metodą cytometrii przepływowej. Jak pokazano na Fig. 6A, 800 µg/ml CTPG-W znacząco zwiększyło wytwarzanie ROS z 2-6h i zmniejszyło się z 12-24h. Dodatkowo 400 µg/ml CTPG‑W znacząco zwiększyło produkcję ROS z 12-24 godz. Ponadto 200 µg/ml CTPG-W nie zmieniło w szczególności wytwarzania ROS. Dynamiczne zmiany wytwarzania ROS mogą być związane z apoptozą komórek Eca-109. Ustalono również, że CTPG-W ma aktywność wymiatania wolnych rodników (ryc. 6B), co może być związane ze zmniejszonym wytwarzaniem ROS w komórkach Eca-109 traktowanych 800 µg/ml CTPG-W po 12 godzinach.

CTPG‑W zwiększa aktywność kaspazy‑3, kaspazy‑7, kaspazy‑9 i PARP. Uwalnianie cytochromu c w wyniku redukcji Δψm może aktywować proteazy kaspazowe do indukowania apoptozy (29,30,37). Po traktowaniu CTPG-W przez 24 godziny, aktywację kaspazy-3, 7, 8, 9 i PARP wykryto za pomocą analizy Western blot. W porównaniu z kontrolą, poziomy ciętej-kaspazy-9, ciętej-kaspazy-7, ciętej-kaspazy-3 i rozszczepionej-PARP, ale nie poziomy ciętej-kaspazy{{ 20}}, były regulowane w górę przez leczenie CTPG w sposób zależny od dawki (ryc. 7). Wyniki te wskazują, że CTPG-W zmniejsza Δψm i promuje uwalnianie cytochromu c w celu aktywacji kaspaz, które indukują apoptozę komórek Eca-109.

Ekstrakt z Cistanche tubulosa
Dyskusja
Tradycyjna CHM może indukować apoptozę komórek raka przełyku różnymi szlakami, w tym zewnętrznym receptorem śmierci, wewnętrznymi szlakami stresu mitochondrialnego i retikulum endoplazmatycznego (29). Nasze poprzednie badanie wykazało, że CTPG, jako główny składnik C. tubulosa, hamuje wzrost komórek czerniaka B16-F10 poprzez indukcję apoptozy poprzez szlak zależny od mitochondriów (24). W niniejszym badaniu zbadano działanie przeciwnowotworowe CTPG-W na komórki Eca-109 i ustalono, że CTPG-W hamuje wzrost komórek Eca-109, indukuje apoptozę i zatrzymanie cyklu komórkowego, zmniejszone Δψm, zwiększone uwalnianie cytochromu ci aktywowanych kaspaz. CTPG i CTPG-W mogą indukować apoptozę i zatrzymanie cyklu komórkowego w komórkach nowotworowych. Jednak dokładne mechanizmy różnią się ze względu na różne składniki CTPG (26,64 procent echinakozydu, 10,19 procent akteozydu i 1,71 procent izoakteozydu) i CTPG-W (39,16 procent echinakozydu i 2,44 procent akteozydu). CTPG zatrzymało komórki B16-F10 w fazie G0/G1, ale CTPG-W zatrzymało komórki Eca-109 w fazie S (24). Produkcja ROS była zależnie od dawki zwiększona przez CTPG, ale wskazywała na zmianę w sposób zależny od czasu przez wysoką dawkę CTPG‑W, która znacznie wzrosła na początku leczenia CTPG-W (2-6 h) i zmniejszyła się znacząco po 12 godzinach w porównaniu z kontrolą. Możliwym powodem jest to, że głównym składnikiem CTPG-W jest echinakozyd. Wiele badań wykazało, że echinakozyd może hamować produkcję ROS i apoptozę wywołaną przez ROS, aby wywierać działanie neuroprotekcyjne i przeciwstarzeniowe (38-40). Podobnie w niniejszym badaniu zaobserwowano aktywność zmiatania wolnych rodników. Dlatego spekulowano, że niektóre składniki, w tym werbaskozyd, izowerbaskozyd i salidrozyd w wysokiej dawce CTPG-W, mogą natychmiast wywołać wytwarzanie ROS, powodując apoptozę komórek Eca-109 (41,42), a następnie ROS został wymieciony przez echinakozyd. Inną możliwą przyczyną różnic w produkcji ROS przez CTPG i CTPG-W jest to, że w tym badaniu i w poprzednim badaniu zastosowano różne linie komórkowe (24). Dong i wsp. (43) donieśli, że echinakozyd może indukować apoptozę ludzkich komórek raka jelita grubego SW480 poprzez generowanie oksydacyjnych uszkodzeń DNA bez zwiększonych poziomów ROS.
Traktowanie CTPG-W zmniejszyło Δψm i spowodowało uwolnienie cytochromu c, który sprzyja rozszczepianiu kaspazy-9 (28). Konsekwentnie, poziomy rozszczepionej kaspazy-9 były podwyższane przez traktowanie CTPG-W. Następnie aktywna kaspaza-9 może aktywować kaspazę-3 w celu wywołania apoptozy (44). Poziomy rozszczepionej kaspazy -3 były również podwyższone przez traktowanie CTPG-W. Jednak kaspaza -8 nie była aktywowana przez CTPG-W, co wskazuje, że szlak zewnętrznego receptora śmierci nie był zaangażowany w apoptozę indukowaną przez CTPG-W. Obserwacje te wskazują, że CTPG-W indukuje apoptozę komórek Eca-109 poprzez aktywację szlaku zależnego od mitochondriów.
PARP odgrywa ważną rolę w stabilności genomowej i może być rozszczepiana przez aktywne kaspazy, zwłaszcza kaspazy-3 i -7 (45). Ustalono, że leczenie CTPG-W aktywowało kaspazę-3 i -7, które mogą rozszczepiać PARP w celu zahamowania naprawy DNA i wywołania apoptozy.
CTPG-W również zależnie od dawki i czasu hamuje wzrost komórek ludzkiego raka wątrobowokomórkowego BEL-7404 (dane niepublikowane). Chociaż CTPG-W hamuje wzrost komórek Eca-109 i BEL-7404, sprzyja proliferacji splenocytów, co może wynikać z zawartości polisacharydów (~50%) w CTPG-W (46 ). Podobnie, wiele badań wykazało, że polisacharydy mogą promować proliferację splenocytów (46-49). W modelu mysim ustalono, że CTPG‑W istotnie zwiększał wskaźnik śledziony w porównaniu z grupą kontrolną, ale nie wpływał na masę ciała i inne wskaźniki narządowe, w tym serce, wątrobę, nerki i płuca (dane niepublikowane), wskazując, że CTPG-W nie ma działania cytotoksycznego na normalne komórki.
Łącznie dane wskazują, że CTPG-W hamuje wzrost komórek Eca-109 poprzez indukcję apoptozy na szlaku zależnym od mitochondriów.

korzyści cistanche: antyapoptoza
Podziękowanie
Autorzy pragną podziękować dr. Jianhua Yang (Baylor College of Medicine) za dopracowanie rękopisu.
Finansowanie
Badanie to było wspierane przez 13-ty plan pięcioletni dla Key Discipline Biology Bidding Project (dotacja nr 17SDKD0202), Xinjiang Normal University i Key Laboratory of Special Environment Biodiversity Application and Regulation w Xinjiang (dotacja nr XJTSWZ-2017-04) JL i grantu Chińskiej Narodowej Fundacji Nauk Przyrodniczych (nr grantu 31760260) dla XW.
Dostępność danych i materiałów
Dane i materiały wykorzystane i przeanalizowane podczas niniejszego badania są dostępne u odpowiedniego autora na uzasadnione żądanie.
Wkład autorów
Eksperymenty przeprowadziły CF, AA, YY i QC. LX, JLv i XW przeanalizowali dane i przygotowane liczby. JinyuL i JinyaoL zaprojektowali projekt i napisali manuskrypt.
Zatwierdzenie etyki i zgoda na udział
Wszystkie eksperymenty na zwierzętach zostały zatwierdzone przez Komitet ds. Etyki Eksperymentów na Zwierzętach Xinjiang Key Laboratory of Biological Resources and Genetic Engineering (zatwierdzenie, nr BRGE-AE001; Xinjiang University).
Zgoda pacjenta na publikację
Nie dotyczy.
Konkurujące interesy
Autorzy deklarują brak sprzecznych interesów.
Bibliografia
Wu CR, Lin HC i Su MH: odwrócenie przez wodneekstrakty z Cistanche tubulosaz deficytów behawioralnych w modelu szczurzym podobnym do choroby Alzheimera: związek z odkładaniem się amyloidu i funkcją ośrodkowego neuroprzekaźnika. BMC Uzupełnienie Altern Med 14: 202, 2014.
Li J, Aspire A, Gao L, Huo S, Luo J i Zhang F:Glikozydy fenyloetanoidowe z Cistanche tubulosahamuje wzrost komórek B16-F10 zarówno in vitro, jak i in vivo poprzez indukcję apoptozy przez szlak zależny od mitochondriów. J Rak 7: 1877-1887, 2016.
Brand-Williams W, Culver ME i Berset C: Zastosowanie metody wolnorodnikowej do oceny aktywności przeciwutleniającej. LWT-Food Sci Technol 28: 25-30, 1995.

