Agoniści receptora GLP{0}} w cukrzycowej chorobie nerek: aktualne dowody i przyszłe kierunki
Jul 14, 2023
Abstrakcyjny
Wraz z pojawieniem się różnych klas leków hipoglikemizujących, w leczeniu cukrzycy kładzie się duży nacisk na wybór odpowiedniego leku dla każdego pacjenta. Wśród leków opartych na inkretynach agoniści receptora glukagonopodobnego peptydu 1 (GLP{4}}) są obiecującą opcją terapeutyczną dla pacjentów z cukrzycową chorobą nerek (DKD). W kilku badaniach oceniających wyniki sercowo-naczyniowe wykazano, że agoniści receptora GLP-1 mają korzystny wpływ na wyniki sercowo-nerkowe poza działaniem obniżającym poziom glukozy we krwi u pacjentów z cukrzycą typu 2 (T2DM). Ochronne działanie agonistów receptora GLP{9}} na nerki prawdopodobnie wynika z ich bezpośredniego działania na nerki, oprócz ich pośredniego działania, które poprawia konwencjonalne czynniki ryzyka DKD, takie jak obniżenie poziomu glukozy we krwi, ciśnienia krwi i masy ciała . Hamowanie stresu oksydacyjnego i stanu zapalnego oraz indukcja natriurezy to główne mechanizmy renoprotekcyjne analogów GLP{10}}. Wczesne dowody z rozwoju leków o podwójnej i potrójnej kombinacji sugerują, że agoniści receptora GLP -1 prawdopodobnie staną się popularnymi opcjami leczenia pacjentów z T2DM.
Słowa kluczowe
Nefropatie cukrzycowe, peptyd glukagonopodobny 1, cukrzyca typu 2

Kliknij tutaj, aby kupić ekstrakt Cistanche
Wstęp
Liczba pacjentów z cukrzycą (DM) stale rośnie na całym świecie, a cukrzyca jest główną przyczyną przewlekłej choroby nerek (CKD) i schyłkowej niewydolności nerek (ESRD) [1]. W Korei częstość występowania cukrzycy wynosiła 13,8% u dorosłych w wieku powyżej 30 lat w 2018 r. [2], a przewidywano, że do 2030 r. wyniesie 29,2% u mężczyzn i 19,7% u kobiet [3]. Całkowita liczba nowych pacjentów, którzy rozpoczęli terapię nerkozastępczą (RRT) z powodu ESRD, wzrosła z 10,{14}} w 2011 r. do 18 642 w 2019 r. [4], a odsetek pacjentów z cukrzycą jako podstawową przyczyną ESRD wzrósł z 19,5 procent w 1992 roku do 50,6 procent w 2012 roku [5], co czyni DM najczęstszą przyczyną ESRD w Korei [4]. Pomimo postępów w technologii medycznej i leczeniu, zapotrzebowanie na RRT wzrasta na całym świecie i oczekuje się, że do 2030 r. wzrośnie ponad dwukrotnie w porównaniu z 2010 r. [6].
Cukrzycowa choroba nerek (DKD) jest główną przyczyną zachorowalności i śmiertelności w cukrzycy [7,8]. Dlatego kluczowe znaczenie ma hamowanie początku i progresji DKD, częściowo poprzez opracowanie metod terapeutycznych zapobiegających lub opóźniających jej wystąpienie. Kontrolowanie poziomu cukru we krwi i ciśnienia krwi za pomocą inhibitorów konwertazy angiotensyny lub blokerów receptora angiotensyny jest obecnie celem w leczeniu DKD [9] i żadne specjalne leki ani inne opcje terapeutyczne nie są szeroko stosowane w celu opóźnienia progresji DKD. Jednak kilka badań oceniających wyniki sercowo-naczyniowe (CVOT) wykazało, że inhibitory kotransportera sodowo-glukozowego 2 (SGLT2) i agoniści receptora glukagonopodobnego peptydu 1 (GLP{9}}) mają korzystny wpływ na wyniki sercowo-nerkowe, zwłaszcza u pacjentów z cukrzycą typu 2 DM (T2DM), u których występuje duże ryzyko chorób sercowo-naczyniowych (CVD) [10–12]. Opierając się na wynikach badań klinicznych, aktualne wytyczne American Diabetes Association i Korean Diabetes Association zalecają klinicystom rozważenie przepisywania inhibitorów SGLT2 lub agonistów receptora GLP-1 po metforminie w ramach schematu zmniejszania stężenia glukozy u pacjentów z cukrzycą typu 2 i PChN [13,14]. W tym artykule przeglądowym skupiamy się na agonistach GLP{20}} i omawiamy kliniczne i przedkliniczne dowody ich działania nefroprotekcyjnego oraz potencjalne mechanizmy leżące u podstaw tego działania.
Fizjologia i efekty metaboliczne glukagonopodobnego peptydu 1
Doustne spożycie glukozy powoduje wydzielanie większej ilości insuliny niż wstrzyknięcie glukozy ze względu na obecność hormonów jelitowych zwanych inkretynami [15]. Peptyd żołądkowo-jelitowy (GIP) i GLP (GLP-1, GLP-2) to hormony inkretynowe wytwarzane przez enteroendokrynowe komórki L dystalnej części jelita cienkiego i okrężnicy [16]. U ludzi stężenie całkowitego GLP{5}} na czczo waha się od 5 do 10 pmol/l i może wzrosnąć do 40–50 pmol/l w odpowiedzi na posiłki [17]. Stężenie biologicznie czynnego, nienaruszonego GLP w osoczu-1 jest znacznie niższe niż to (na czczo,<2 pmol/L; peak postprandial concentrations, 5–10 pmol/L) [18].
Uwolnienie GLP{0}} po posiłku następuje w sposób dwufazowy. Początkowy szybki wzrost poziomu krążącego GLP{1}} występuje 15 do 30 minut po posiłku, po czym następuje drugi mniejszy szczyt po 90 do 120 minutach [19,20]. Szybki wzrost wydzielania GLP{8}} po posiłkach jest związany z pętlą proksymalnie-dystalną regulowaną przez neuroprzekaźniki, takie jak acetylocholina i peptydy uwalniające gastrynę [21]. Uważa się, że drugi późniejszy szczyt GLP{12}} ma miejsce, gdy połknięte składniki odżywcze przemieszczają się w dół światła i oddziałują bezpośrednio z dystalnymi komórkami L [22,23].
Natywny GLP{0}} ma niezwykle krótki okres półtrwania, poniżej 2 minut, ze względu na rozkład przez enzymy dipeptydylo-peptydazy IV (DPP IV) i eliminację przez nerki [24].
Enzymy DPP IV rozszczepiają aktywne formy GLP-17-36 i GLP-17-37, tworząc odpowiednio nieaktywne GLP-19-36 lub GLP-19-37, które mają niskie powinowactwo do GLP{{4 }} receptor [25,26]. Tylko 10 do 15 procent wydzielanego GLP{9}} dociera do trzustki poprzez krążenie ogólnoustrojowe [25], a zarówno aktywna, jak i nieaktywna postać GLP-1 jest szybko usuwana z krążenia przez nerki. Chociaż upośledzenie czynności nerek nie wpływa na początkową degradację GLP{13}}, w której pośredniczy DPP IV, klirens GLP-1 jest opóźniony u pacjentów z niewydolnością nerek [24]. U ludzi receptor GLP{16}} ulega ekspresji w trzustce, płucach, mózgu, nerkach, żołądku i sercu, ale nie w wątrobie, mięśniach szkieletowych ani tkance tłuszczowej [27]. Związanie GLP-1 z jego receptorem aktywuje cyklazę adenylanową, po czym następuje wzrost poziomu cyklicznego AMP i cytoplazmatycznego Ca plus 2 indukującego wydzielanie insuliny [28]. Oprócz krótkotrwałego efektu GLP{21}} polegającego na wzmocnieniu zależnej od glukozy stymulacji wydzielania insuliny, ciągła aktywacja GLP{24}} zwiększa również syntezę insuliny [29], moduluje proliferację komórek beta [30], oraz hamuje apoptozę komórek beta [31] i uwalnianie glukagonu [32]. Hormony inkretynowe zmniejszają również opróżnianie żołądka [33], hamują przyjmowanie pokarmu [34] oraz zwiększają natriurezę i diurezę [35,36].

Cistanche tubulosa
Klasyfikacja agonistów receptora glukagonopodobnego peptydu 1
Agoniści receptora GLP{0}} mają dwie główne struktury szkieletowe i są klasyfikowani jako eksendyna-4- lub związki oparte na ludzkim GLP-1- [37]. Dzieli się je na krótko i długodziałające, a niektóre preparaty miesza się z insuliną (tab. 1). Eksendyna -4 jest białkiem wyizolowanym w 1992 roku ze śliny jaszczurki olbrzymiej (Heloderma podejrzanym) [38]. Białko to składa się z 39 aminokwasów i ma 53% podobieństwa sekwencji zasad do natywnego ludzkiego GLP{12}}. Eksenatyd i liksysenatyd są oparte na strukturze eksendyny-4. Eksenatyd jest rekombinowaną postacią peptydu eksendyny-4 i był pierwszym agonistą receptora GLP-1 opracowanym do leczenia T2DM. Liksysenatyd jest analogiem eksendyny -4 z dodatkowymi sześcioma lizynami przyłączonymi do C-końca, co zapewnia mu dłuższy okres półtrwania niż eksenatyd. Te środki na bazie eksendyny-4-mają stosunkowo krótki okres półtrwania (~3 godziny) i silnie hamują opróżnianie żołądka [39], co może powodować działania niepożądane ze strony przewodu pokarmowego, takie jak nudności. Ale mają one również silne działanie przeciwhiperglikemiczne po posiłku i mogą potencjalnie zastąpić szybko działającą insulinę doposiłkową [39]. Te krócej działające środki są mniej skuteczne w obniżaniu poziomu glukozy na czczo ze względu na ich krótki okres półtrwania.
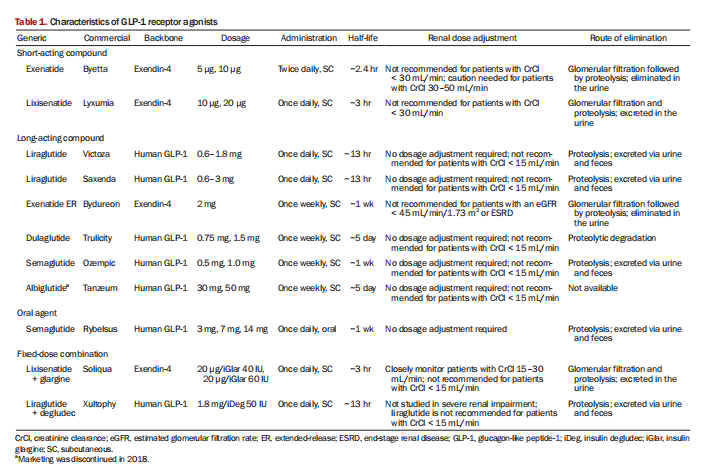
Ludzkie środki oparte na GLP{0}} są strukturalnie bardziej podobne do natywnych GLP-1 niż do tych opartych na eksendynie-4. Wykazują one od 90 do 97 procent homologii aminokwasowej z endogennym ludzkim GLP{6}} i wydłużonym okresem półtrwania wynikającym z oporności na DPP IV i niekowalencyjnego wiązania z albuminami surowicy. Te dłużej działające środki prowadzą do większego zmniejszenia stężenia glukozy w osoczu na czczo i stężenia hemoglobiny A1c (HbA1c) niż środki krócej działające [39,40]. Ludzkie związki GLP-1 to liraglutyd, albiglutyd, dulaglutyd i liraglutyd, z których wszystkie są środkami do wstrzykiwań. Albiglutyd i dulaglutyd to duże cząsteczki skoniugowane z dużymi białkami, co wydłuża ich okres półtrwania i umożliwia podawanie raz w tygodniu. Semaglutyd jest dostępny zarówno w postaci do wstrzykiwań, jak i doustnych. Wraz z wycofaniem albiglutydu z rynku z powodów handlowych, liraglutyd, dulaglutyd i liraglutyd (podawany doustnie i podskórnie) są obecnie dostępnymi zatwierdzonymi agonistami ludzkiego receptora GLP-1.
W tabeli 1 przedstawiono zalecane zastosowania agonistów receptora GLP-1 zgodnie z szacowanym współczynnikiem przesączania kłębuszkowego (eGFR). Ludzki dulaglutyd, liraglutyd i semaglutyd pochodzące z GLP{2}} nie są wydalane przez nerki i można je stosować do wartości eGFR 15 ml/min/1,73 m2; nie ma wystarczających doświadczeń, aby zalecać stosowanie tych leków przy niższych wartościach eGFR [41]. Z kolei eksenatyd i liksysenatyd, które są wydalane przez nerki, są przeciwwskazane poniżej eGFR 30 ml/min/1,73 m2 ze względu na ryzyko kumulacji i toksyczności [24]. Eksenatyd należy stosować ostrożnie u pacjentów z eGFR 30–50 ml/min/1,73 m2 (tab. 1).
Wpływ na nerki agonistów receptora glukagonopodobnego peptydu 1 u pacjentów z cukrzycą typu 2
Kilka CVOT zbadało agonistów receptora GLP-1; jednakże żaden z nich nie koncentrował się na pierwszorzędowym punkcie końcowym, jakim były zdarzenia nerkowe; wyniki dotyczące nerek były zgłaszane jako drugorzędne punkty końcowe po pierwotnych punktach sercowo-naczyniowych. W tej części skupiono się na nerkowych wynikach leczenia agonistą receptora GLP-1 zgłaszanych w badaniach z randomizacją (Tabela 2).

Pierwszym badaniem CVOT dla agonisty receptora GLP-1 było badanie ELIXA (ang. Evaluation of Lixisenatide in Acute Coronary Syndrome), którego wyniki opublikowano w 2015 roku [42]. Do badania włączono łącznie 6068 uczestników z T2DM, zawałem mięśnia sercowego lub niestabilną dusznicą bolesną w wywiadzie, średnią początkową wartością HbA1c wynoszącą 7,7% i medianą czasu obserwacji wynoszącą 25 miesięcy. Chociaż zdarzenia nerkowe nie były badane w pierwotnym badaniu ELIXA, przeprowadzono eksploracyjną analizę wyników nerkowych [43]. Po okresie obserwacji, którego mediana wyniosła 108 tygodni, liksysenatyd zmniejszał progresję stosunku albumin do kreatyniny w moczu (UACR) u pacjentów z makroalbuminurią i był związany z niższym ryzykiem wystąpienia makroalbuminurii po dostosowaniu do początkowej i badanej HbA1c i inne tradycyjne czynniki ryzyka nerek. Nie stwierdzono istotnych różnic w spadku eGFR między grupami terapeutycznymi. Badanie to miało krótki okres obserwacji wynoszący 2 lata, wysoki odsetek uczestników leczonych statyną i niską zgodność z lekami w porównaniu z innymi badaniami w tabeli 2.
W badaniu LEADER (Liraglutide Effect and Action in Diabetes: Evaluation of Cardiovascular Outcome Results), opublikowanym w 2016 [44], uczestnicy z cukrzycą typu 2 mieli co najmniej 50 lat i co najmniej jedną chorobą sercowo-naczyniową lub co najmniej 60 lat z co najmniej jednym czynnikiem ryzyka sercowo-naczyniowego. Do badania włączono łącznie 9340 uczestników, których mediana okresu obserwacji wynosiła 3,8 roku, a średnia początkowa wartość HbA1c wynosiła 8,7 procent. Około 23 procent uczestników miało PChN o nasileniu od umiarkowanego do ciężkiego, co sugeruje populację bardzo wysokiego ryzyka. Warto zauważyć, że badanie to obejmowało 220 osób z eGFR 15–30 ml/min/1,73 m2. Liraglutyd zmniejszał ryzyko wystąpienia drugorzędowego złożonego nerkowego punktu końcowego (makroalbuminuria o nowym początku, utrzymująca się duplikacja kreatyniny w surowicy, rozpoczęcie RRT lub śmierć nerek) o 22% (współczynnik ryzyka 0,78; 95% przedział ufności [CI] 0,67–0,92; p=0.003) [45]. Odkrycie to było spowodowane przede wszystkim zmniejszeniem przetrwałej makroalbuminurii o nowym początku. To badanie było pierwszym, które wykazało, że agonista GLP{36}} przynosi korzyści sercowo-naczyniowe, chociaż może nie mieć zastosowania u pacjentów z niskim ryzykiem sercowo-naczyniowym.
SUSTAIN{0}} (Trial to Evaluate Cardiovascular and Other Long-term Outcomes with Semaglutide in Subjects with Type 2 Diabetes) był kolejnym CVOT, również opublikowanym w 2{21}}16 [46]. W sumie 3297 pacjentów zostało losowo przydzielonych, a 3232 pacjentów ukończyło badanie w okresie obserwacji wynoszącym średnio 2,1 roku. Osiemdziesiąt trzy procent uczestników miało ustaloną chorobę sercowo-naczyniową, przewlekłą chorobę nerek lub obie choroby, a średnia HbA1c w całej badanej populacji wynosiła 8,7 procent. Semaglutyd podawany raz w tygodniu wpłynął na 36-procentową redukcję (HR, 0,64; 95% CI, 0,46–0,88; p=0,005) drugorzędowego złożonego nerkowego punktu końcowego (makroalbuminuria o nowym początku, podwojenie kreatyniny w surowicy, eGFR ok<45 mL/min/1.73 m2, initiation of RRT, or renal death). This result was mainly driven by a reduction in new-onset macroalbuminuria. Across the SUSTAIN 1–7 trials [47], semaglutide lowered albuminuria compared with placebo beginning as early as 16 weeks and lasting over the entire treatment period.
Kolejnym badaniem, opublikowanym w 2017 roku, było badanie EXSCEL (Exenatide Study of Cardiovascular Event Lowering), którego celem była ocena wpływu podawanego raz w tygodniu eksenatydu o przedłużonym uwalnianiu (ER) na wyniki sercowo-naczyniowe u uczestników z T2DM [48]. W sumie 14 752 pacjentów, z których 73,1 procent miało wcześniejszą chorobę sercowo-naczyniową, było obserwowanych przez medianę 3,2 roku. Eksenatyd ER nie miał istotnego wpływu na wyniki nerek w dodatkowej analizie danych z badania EXSCEL [49]. Eksenatyd podawany dwa razy dziennie również nie wpływał na eGFR ani albuminurię w porównaniu z insuliną glargine w ciągu 52-tygodniowego okresu badania [50].
Wpływ albiglutydu na układ sercowo-naczyniowy oceniano u pacjentów z T2DM i CVD w badaniu HARMONY (NCT02465515) [51], opublikowanym w 2018 r. Do badania włączono łącznie 9463 uczestników z medianą HbA1c wynoszącą 8,7%. była to populacja stosunkowo wysokiego ryzyka z wysokim wyjściowym poziomem glukozy. Po medianie obserwacji wynoszącej 1,6 roku, albiglutyd nie przyniósł znaczącej korzyści w spowolnieniu tempa spadku eGFR.
Wpływ leczenia dulaglutydem na nerki oceniano w dwóch reprezentatywnych badaniach. Pierwszym badaniem było badanie AWARD{{0}} (NCT01621178), opublikowane w 20}18 [52]. Do badania włączono pięciuset siedemdziesięciu siedmiu uczestników z T2DM i PChN o nasileniu umiarkowanym do ciężkiego. Wstrzyknięcie dulaglutydu raz w tygodniu wiązało się ze znacznie mniejszym spadkiem eGFR w porównaniu z insuliną glargine w ciągu 52 tygodni. Średni spadek eGFR po dawce 1,5-mg dulaglutydu wynosił około 10% wartości obserwowanej dla insuliny glargine (–0,5 ml/min/1,73 m2 w 1,{{ 19}} mg dulaglutydu w porównaniu z –5,5 ml/min/1,73 m2 w grupie insuliny glargine). Ten związek między dulaglutydem a zmniejszonym spadkiem eGFR był najbardziej widoczny u uczestników z makroalbuminurią. Innym badaniem oceniającym wpływ dulaglutydu podawanego we wstrzyknięciach na wyniki sercowo-naczyniowe w cukrzycy typu 2 było badanie REWIND (Researching Cardiovascular Events with a Weekly Incretin in Diabetes) [53,54], opublikowane w 2{55}}19. To badanie zostało zaprojektowane w celu wykazania wyższości, w przeciwieństwie do poprzednich prób. W sumie 9,901 uczestników z T2DM było obserwowanych przez medianę 5,4 roku, czyli dłużej niż w poprzednich badaniach. To badanie było wyjątkowe, ponieważ uczestnicy byli niskiego ryzyka, ze średnią wyjściową wartością HbA1c 7,2 procent, medianą eGFR 74,9 ml/min/1,73 m2, wyjściową częstością występowania CVD 31,5 procent i wyjściową częstością albuminurii 35.{{ 60}} procent . Złożony wynik nerkowy występował znacznie rzadziej w grupie dulaglutydu niż w grupie placebo (HR, 0,85; 95 procent CI, 0,77-0,93; p=0, 0004), a największym efektem było zmniejszenie rozwoju makroalbuminurii w grupie dulaglutydu (HR 0,77; 95% CI 0,68–0,87; p < 0,0001).
Badanie PIONEER 6 (Peptide Innovation for Early Diabetes Treatment) zostało zaprojektowane w celu oceny wyników sercowo-naczyniowych po doustnym podawaniu semaglutydu raz dziennie u pacjentów z cukrzycą typu 2 z wysokim ryzykiem sercowo-naczyniowym [55], a jego wyniki opublikowano w 2019 r. W badaniu tym wzięło udział 3183 uczestników, którzy byli obserwowani przez medianę 15,9 miesiąca, co stanowi najkrótszy czas trwania badań wymienionych w Tabeli 2. Jednak w tym badaniu nie zdefiniowano z góry żadnego nerkowego punktu końcowego do oceny.
Ostatnim CVOT dla agonistów GLP{0}} było badanie AMPLITUDE-O (Effect of Efpeglenatide on Cardiovascular Outcomes) u pacjentów z cukrzycą typu 2 i CVD lub CKD w wywiadzie [56]; wyniki opublikowano w 2021 r. Epeglenatyd do wstrzykiwań raz w tygodniu jest nowym agonistą receptora GLP-1 na bazie eksendyny. W sumie 4076 uczestników zostało zapisanych i obserwowanych przez medianę 1,81 roku. W porównaniu z placebo, efpeglenatyd prowadził do zmniejszenia o 32% ryzyka złożonego zdarzenia związanego z nerkami (incydent makroalbuminurii, zwiększenie UACR o co najmniej 30% w stosunku do wartości początkowej, utrzymujące się zmniejszenie eGFR o co najmniej 40%, rozpoczęcie RRT lub trwały eGFR z<15 mL/min/1.73 m2 ), independently of baseline use of SGLT2 inhibitors or metformin and baseline eGFR (HR, 0.68; 95% CI, 0.57–0.79; p < 0.001). However, a kidney function outcome event, defined as a composite of a decrease in eGFR of at least 40% for ≥30 days, ESRD, or death from any cause, did not differ between the efpeglenatide group and the placebo group (HR, 0.77; 95% CI, 0.57–1.02; p = 0.07).

Suplement Cistanche
Sugerowane mechanizmy nefroprotekcyjne agonistów receptora glukagonopodobnego peptydu 1
1 Efekty pośrednie poprzez poprawę konwencjonalnych czynników ryzyka cukrzycowej choroby nerek
Hiperglikemia odgrywa kluczową rolę w patogenezie DKD [57,58], a agoniści receptora GLP -1 mają silne działanie obniżające stężenie glukozy [59–62]. Wytyczne dotyczące praktyki klinicznej The Kidney Disease: Improving Global Outcomes (KDIGO) 2020 zalecają stosowanie agonistów receptora GLP -1 jako doskonałą opcję dla pacjentów z DKD, którzy nie osiągnęli docelowej glikemii lub jako alternatywę dla pacjentów nietolerujących metforminy lub inhibitor SGLT2 [63]. Chociaż podkreśla się również mechanizmy niezależne od glukozy, uważa się, że przeciwhiperglikemiczne działanie agonistów receptora GLP -1 przyczynia się do ich działania nefroprotekcyjnego u pacjentów z DKD. Ponadto agoniści receptora GLP{12}} powodują zmniejszenie masy ciała, ciśnienia tętniczego i dyslipidemii, co również może przyczynić się do ich działania przeciw albuminurii [64,65].
W badaniu LEADER [44] grupa otrzymująca liraglutyd wykazała zmniejszenie HbA1c o 0,4% w porównaniu z grupą otrzymującą placebo. Utrata masy ciała była o 2,3 kg większa, a skurczowe ciśnienie krwi o 1,2 mmHg niższe w grupie liraglutydu niż w grupie placebo. W badaniu REWIND [54] uczestnicy w grupie otrzymującej 1,{11}} mg dulaglutydu raz w tygodniu mieli o 0,61% niższe HbA1c, o 1,46 kg niższą masę ciała i o 1,7 mmHg niższe skurczowe ciśnienie krwi niż uczestnicy z grupy placebo. W badaniu SUSTAIN{19}} [46] średni poziom HbA1c był niższy o 1,{23}} punktu procentowego, średnia masa ciała zmniejszyła się o 4,3 kg więcej, a średnie skurczowe ciśnienie krwi było o 2,6 mmHg niższe w grupie otrzymującej 1,{29}} mg semaglutydu raz w tygodniu niż w grupie placebo. W badaniu PIONEER 5 [55] doustny semaglutyd (14 mg) raz dziennie skuteczniej niż placebo zmniejszał HbA1c i masę ciała u pacjentów z cukrzycą typu 2. Jednak statystyczna poprawka na poziom HbA1c w próbie, zmianę ciśnienia krwi i spadek masy ciała nie zmieniła znacząco obserwowanego spadku albuminurii wywołanego przez agonistów receptora GLP -1 w kilku CVOT [66], co sugeruje, że ochronne działanie nerek agonistów receptora GLP{40}} nie wynika wyłącznie z poprawy czynników ryzyka.
Oprócz wpływu na masę ciała, ciśnienie krwi i poziom glukozy, GLP-1 reguluje również metabolizm lipidów. Dyslipidemia jest silnym czynnikiem ryzyka zarówno CKD, jak i DKD. Badania eksperymentalne dostarczyły danych potwierdzających tezę, że zaburzenia lipidowe przyczyniają się do zapoczątkowania i progresji choroby kłębuszków nerkowych [67]. Przegląd systematyczny i metaanaliza 35 badań wykazały, że agoniści receptora GLP -1 są powiązani ze zmniejszeniem poziomu cholesterolu całkowitego i lipoprotein o małej gęstości oraz trójglicerydów [68]. GLP{7}} hamuje wydzielanie lipazy żołądkowej [69] oraz produkcję lipoprotein i chylomikronów jelitowych u ludzi [70]. Sygnalizacja receptora GLP{10}} zmniejsza zawartość trójglicerydów w wątrobie i upośledza lipogenezę w wątrobie poprzez stymulację szlaku kinazy białkowej aktywowanej przez AMP [71,72]. Zwiększa również obwodowe wykorzystanie lipoprotein bogatych w trójglicerydy poprzez zwiększone spalanie tłuszczu i aktywację funkcji brunatnej tkanki tłuszczowej [73,74]. Nie jest jednak pewne, czy te działania bezpośrednio przyczyniają się do ochronnego działania agonistów receptora GLP-1 na nerki.
2 Potencjalne bezpośrednie mechanizmy odpowiadające za ochronne działanie agonistów receptora glukagonopodobnego peptydu 1 na nerki
Receptor GLP{0}} ulega ekspresji w korze nerkowej i układzie naczyniowym, a także w komórkach kanalików proksymalnych [75,76], chociaż nadal nie ma pewności co do lokalizacji receptora w nerkach z powodu braku przeciwciał o wysokiej czułości i swoistości. Hamowanie stresu oksydacyjnego i stanu zapalnego, indukcja natriurezy i obniżenie ciśnienia wewnątrzkłębuszkowego to potencjalne bezpośrednie mechanizmy leżące u podstaw ochronnego działania analogów GLP -1 na nerki (ryc. 1). Ogólnoustrojowy stres oksydacyjny zwiększa stadium początkowej DKD [77]. Badanie przeprowadzone na szczurach z cukrzycą wykazało, że rekombinowany ludzki GLP{6}} osłabia stres oksydacyjny w kłębuszkach nerkowych i kłębuszkowych komórkach śródbłonka mikronaczyniowego poprzez hamowanie kinazy białkowej C i aktywację kinazy białkowej A (PKA) [78]. Liraglutyd zmniejszał również stres oksydacyjny i albuminurię u szczurów z cukrzycą typu 1 indukowaną streptozotocyną poprzez hamowanie za pośrednictwem PKA nerkowych oksydaz fosforanowych dinukleotydu nikotynoamidoadeninowego [79]. Wykazano, że eksendyna -4 aktywuje szlak sygnałowy Nrf2, który odgrywa kluczową rolę w zapobieganiu stresowi oksydacyjnemu i utrzymywaniu homeostazy redoks w komórkach mięśni gładkich naczyń [80,81].

Zapalenie odgrywa kluczową rolę w rozwoju DKD. Zgromadzone dane eksperymentalne sugerują, że działanie przeciwzapalne leży u podstaw ochronnego działania GLP na nerki-1. Agoniści receptora GLP{2}} zmniejszają wytwarzanie cytokin prozapalnych, cząsteczek adhezyjnych i sygnalizacji profibrotycznej [82–84]. Liraglutyd hamował aktywację jądrowego czynnika martwicy nowotworu (TNF)- -, w której pośredniczy czynnik jądrowy kappa B (NF-κB) oraz aktywowaną mitogenem aktywację szlaku kinazy białkowej w podocytach kłębuszków nerkowych modelu mysiego związanego z glomerulopatią związaną z otyłością [82]. Eksendyna -4 osłabiała albuminurię, hiperfiltrację kłębuszków nerkowych, przerost kłębuszków nerkowych i ekspansję macierzy mezangialnej bez obniżania poziomu glukozy we krwi u szczurów z cukrzycą poprzez hamowanie stresu oksydacyjnego i aktywacji NF-κB [83]. U ludzi eksenatyd zmniejsza wytwarzanie reaktywnych form tlenu i ekspresję NF-κB, TNF- , interleukiny-1, kinazy N-końcowej c-Jun-1, receptora toll-podobnego-4 i supresor cytokin sygnalizacyjnych 3 u otyłych pacjentów z T2DM, niezależnie od utraty masy ciała [84]. Eksenatyd zmniejszał również stężenie białka C-reaktywnego o wysokiej czułości o 61 procent [85] oraz zmniejszał wydalanie transformującego czynnika wzrostu w moczu- 1 i kolagenu typu IV u pacjentów z T2DM [86]. Leczenie liraglutydem było związane ze zmniejszonym poziomem cytokin zapalnych i wzrostem poziomu adiponektyny w surowicy u otyłych pacjentów z T2DM [87]. Liraglutyd poprawiał również stres oksydacyjny, zwiększając stężenie glutationu i zmniejszając poziomy wodoronadtlenków lipidów w surowicy i oksygenazy hemowej -1 u osób z cukrzycą typu 2, niezależnie od jego działania obniżającego poziom glukozy [88].
Zaproponowano, że efekt natriuretyczny agonistów receptora GLP-1 leży u podstaw wywołanego przez GLP-1 obniżenia ciśnienia krwi zgłaszanego w dużych CVOT. Wydaje się, że natriureza i diureza, w których pośredniczy GLP{2}}, obejmują redystrybucję i redukcję aktywności wymiennika 3 Na plus/H plus (NHE3), który znajduje się na rąbku szczoteczkowym kanalików proksymalnych nerki [89]. Agoniści receptora GLP{6}} fosforylowali NHE3 w miejscach konsensusowych PKA Ser552 i Ser605, zmniejszając jego aktywność [36]. Agoniści receptora GLP -1 również zwiększali natriurezę i diurezę poprzez zwiększenie przepływu krwi przez nerki u szczurów [90]. Badania na ludziach wykazały, że wlew GLP-1 zmniejsza reabsorpcję sodu w kanalikach proksymalnych i zmniejsza stężenie angiotensyny II w osoczu [91]. Ponadto pojedyncze podskórne wstrzyknięcie liraglutydu zwiększyło wydalanie sodu u osób z T2DM [92]. Hamowanie NHE3 przez GLP{18}} może również wpływać na hemodynamikę kłębuszków nerkowych poprzez aktywację sprzężenia zwrotnego kanalikowo-kłębuszkowego. Zwiększenie dostarczania sodu do plamki gęstej spowodowane niską aktywnością NHE3 skutkuje zwężeniem naczyń tętniczek doprowadzających oraz zmniejszeniem hiperfiltracji i ciśnienia kłębuszkowego. Liraglutyd wiąże się z ostrym zmniejszeniem eGFR i późniejszą stabilizacją w czasie, co sugeruje, że GLP -1 ma wpływ na hemodynamikę nerek [93].

Herba Cistanche
Trwają badania i opracowywane są leki kandydujące
Obecnie trwa badanie FLOW (NCT03819153) mające na celu ocenę wpływu semaglutydu podawanego raz w tygodniu na postęp niewydolności nerek. Pierwszorzędowy wynik nerkowy obejmuje trwałe zmniejszenie eGFR większe lub równe 50 procent lub trwałe eGFR<15 mL/min/1.73 m2, initiation of RRT, or death from kidney disease or CVD. This study recently began recruiting more than 3,000 T2DM patients with moderate/advanced CKD and albuminuria, and its estimated completion date is 2024. This trial will be the first to investigate the effects of a GLP-1 receptor agonist on primary kidney outcomes.
Ponadto badanie SOUL (NCT03914326) jest obecnie trwającym badaniem CVOT mającym na celu ocenę hipotezy, że doustny semaglutyd zmniejsza ryzyko zdarzeń sercowo-naczyniowych u pacjentów z cukrzycą typu 2, u których występuje wysokie ryzyko CVD. W tym badaniu złożony nerkowy punkt końcowy jest drugorzędnym punktem końcowym składającym się z utrzymującego się większego niż lub równego 50-procentowego zmniejszenia eGFR lub trwałego eGFR<15 mL/min/1.73 m2, initiation of RRT, and renal death. Oral semaglutide received the approval of the U.S. Food and Drug Administration in September 2019.
Polifarmakologia odnosi się do połączenia kilku strukturalnie powiązanych hormonów w jedną całość. Leczenie podwójnymi agonistami GLP{0}}/glukagonu powodowało utratę masy ciała i skuteczność przeciwhiperglikemiczną lepszą niż stosowanie samych selektywnych agonistów GLP-1 u myszy z otyłością wywołaną dietą [94]. GLP{4}} i glukagon są strukturalnie podobne, a glukagon działa również na receptor GLP-1 [95], co budzi oczekiwania, że połączenie tych dwóch leków może być bardziej skuteczne niż zastosowanie któregokolwiek z leków na jego własny. Obecnie trwa kilka badań klinicznych fazy 2 podwójnych agonistów GLP{8}}/glukagonu. Ponadto podwójni agoniści GLP{9}}/GIP mają wydłużony okres półtrwania z powodu acylacji tłuszczów lub PEGylacji. Podawany raz w tygodniu koagonista GLP{12}}/GIP, nazwany tripeptydem (LY3298176), był lepszy od dulaglutydu pod względem utraty masy ciała i poprawy poziomu HbA1c w badaniu fazy 2 pacjentów z T2DM [96]. Badania kliniczne fazy 1 potrójnej kombinacji GLP{20}}/glukagonu/GIP zostały przeprowadzone przez firmy Hanmi Pharmaceuticals (HM15211) i Novo Nordisk (NNC{22}}).
Stwierdzono, że terapie skojarzone oparte na GLP{0}}zapewniają większe korzyści metaboliczne niż te osiągane przez leczenie każdym z tych związków osobno. Na podstawie zwiększonej skuteczności GLP{1}}/glukagonu i koagonistów GLP{2}}/GIP uzasadnione jest ustalenie, czy podwójni lub potrójni agoniści mogą zapewniać większą skuteczność niż odpowiedni monoagoniści. Różne możliwe kombinacje to GLP-1 z GLP-2 [97], leptyną [98], gastryną [99], amyliną [100], peptydem YY [101], cholecystokininą [102], insuliną [103 ], adrenomedulina [104], czynnik wzrostu fibroblastów 21 [105], estrogen [106], deksametazon [107], przeciwciało konwertazy probiałkowej subtylizyny/keksyny typu 9 [108], agonista melanokortyny -4 [109], farnezoid -x [110] lub inhibitor SGLT2 [111]. Konieczne są dalsze badania w celu oceny, czy którakolwiek z tych kombinacji środków ma lepsze działanie nefroprotekcyjne niż monoagoniści GLP{27}} u pacjentów z DKD.

Standaryzowane Cistanche
Wnioski i perspektywy na przyszłość
Agoniści receptora GLP{0}} są obiecującymi opcjami terapeutycznymi dla pacjentów z DKD, przynoszącymi korzyści wykraczające poza ich działanie obniżające poziom glukozy we krwi. Wydaje się, że czynniki te wpływają głównie na makroalbuminurię, podczas gdy ich wpływ na twarde nerkowe punkty końcowe jest mniej jasny. Chociaż leki te można stosować u pacjentów z CKD z eGFR poniżej 15 ml/min/1,73 m2, należy zbadać bezpieczeństwo stosowania agonistów receptora GLP{6}} u pacjentów z CKD w stadium 5 CKD. Jeśli chodzi o kierunek przyszłych badań, należy przeprowadzić więcej badań podobnych do trwającego badania FLOW w celu oceny głównych wyników leczenia agonistą receptora GLP -1 w odniesieniu do nerek. Ponadto konieczne jest zbadanie, czy leczenie skojarzone agonistami receptora GLP-1 i innymi klasami środków o korzystnym wpływie na nerki będzie miało synergistyczne działanie ochronne na nerki u pacjentów z DKD.
Bibliografia
1. Alicia RZ, Rooney MT, Tuttle KR. Cukrzycowa choroba nerek: wyzwania, postęp i możliwości. Clin J Am Soc Nephrol 2017;12:2032–2045.
2. Jung CH, Son JW, Kang S i in. Arkusze informacyjne dotyczące cukrzycy w Korei, 2020: ocena obecnego stanu. Cukrzyca Metab J 2021;45:1–10.
3. Baik I. Prognoza rozpowszechnienia cukrzycy u dorosłych Koreańczyków na rok 2030 na podstawie czynników ryzyka zidentyfikowanych na podstawie danych krajowych. Cukrzyca Metab J 2019;43:90–96.
4. Hong YA, Ban TH, Kang CY i in. Trendy w charakterystyce epidemiologicznej schyłkowej niewydolności nerek z koreańskiego systemu danych dotyczących nerek (KORDS) z 2019 r. Kidney Res Clin Pract 2021;40:52–61.
5. Jin DC, Han JS. Terapia nerkozastępcza w Korei, 2012. Kidney Res Clin Pract 2014;33:9–18.
6. Liyanage T, Ninomiya T, Jha V i in. Światowy dostęp do leczenia schyłkowej niewydolności nerek: przegląd systematyczny. Lancet 2015;385:1975–1982.
7. Li S, Wang J, Zhang B, Li X, Liu Y. Cukrzyca i śmiertelność związana z przyczyną: badanie populacyjne. Cukrzyca Metab J 2019;43:319–341.
8. Afkarian M, Sachs MC, Kestenbaum B i in. Choroba nerek i zwiększone ryzyko zgonu w cukrzycy typu 2. J Am Soc Nephrol 2013;24:302–308.
9. Yamazaki T, Mimura I, Tanaka T, Nangaku M. Leczenie cukrzycowej choroby nerek: obecne i przyszłe. Cukrzyca Metab J 2021;45:11–26.
10. Kristensen SL, Rørth R, Jhund PS i in. Wyniki sercowo-naczyniowe, śmiertelność i nerki z agonistami receptora GLP -1 u pacjentów z cukrzycą typu 2: systematyczny przegląd i metaanaliza prób sercowo-naczyniowych. Lancet Cukrzyca Endocrinol 2019;7:776–785.
11. Neuen BL, Young T, Heerspink HJ i in. Inhibitory SGLT2 w zapobieganiu niewydolności nerek u pacjentów z cukrzycą typu 2: przegląd systematyczny i metaanaliza. Lancet Cukrzyca Endocrinol 2019;7:845–854.
12. Oh TJ, Moon JY, Hur KY i in. Inhibitor kotransportera sodowo-glukozowego -2 w celu zachowania funkcji nerek u pacjentów z cukrzycą typu 2: zgodne oświadczenie Koreańskiego Stowarzyszenia Diabetologicznego i Koreańskiego Towarzystwa Nefrologicznego. Kidney Res Clin Pract 2020;39:269–283.
13. Hur KY, Moon MK, Park JS i in. 2021 Wytyczne praktyki klinicznej dotyczące cukrzycy Koreańskiego Stowarzyszenia Diabetologicznego. Cukrzyca Metab J 2021;45:461–481.
14. Amerykańskie Towarzystwo Diabetologiczne. 9. Farmakologiczne podejście do leczenia glikemii: standardy opieki medycznej nad cukrzycą-2021. Opieka nad cukrzycą 2021;44 (Suppl 1): S111–S124.
15. Elrick H, Stimmler L, Hlad CJ Jr, Arai Y. Odpowiedź insuliny w osoczu na doustne i dożylne podawanie glukozy. J Clin Endocrinol Metab 1964;24:1076-1082.
16. Eissele R, Göke R, Willemer S, et al. Komórki peptydopodobne glukagonopodobne -1 w przewodzie pokarmowym i trzustce szczurów, świń i mężczyzn. Eur J Clin Invest 1992;22:283–291.
17. Orskov C, Wettergren A, Holst JJ. Wydzielanie hormonów inkretynowych, peptydu glukagonopodobnego-1 i polipeptydu hamującego czynność żołądka, koreluje z wydzielaniem insuliny u zdrowych mężczyzn w ciągu dnia. Scand J Gastroenterol 1996;31:665-670.
18. Kuhre RE, Wewer Albrechtsen NJ, Hartmann B, Deacon CF, Holst JJ. Pomiar poziomu hormonów inkretynowych: peptydu glukagonopodobnego-1 i zależnego od glukozy peptydu insulinotropowego. J Powikłania cukrzycy 2015;29:445–450.
19. Rask E, Olsson T, Söderberg S, et al. Upośledzona odpowiedź inkretynowa po mieszanym posiłku jest związana z insulinoopornością u mężczyzn bez cukrzycy. Opieka nad cukrzycą 2001;24:1640–1645.
20. Elliott RM, Morgan LM, Tredger JA, Deacon S, Wright J, Marks V. Glukagonopodobny peptyd -1 (7-36) amid i zależne od glukozy wydzielanie polipeptydu insulinotropowego w odpowiedzi na spożycie składników odżywczych w mężczyzna: ostre wzorce wydzielania poposiłkowego i 24-h. J Endocrinol 1993;138:159-166.
21.Roberge JN, Brubaker PL. Regulacja jelitowego wydzielania peptydu pochodzącego z proglukagonu przez zależny od glukozy peptyd insulinotropowy w nowej pętli enteroendokrynnej. Endokrynologia 1993;133:233–240.
22. Lim GE, Brubaker PL. Wydzielanie glukagonopodobnego peptydu 1 przez komórkę L: widok od wewnątrz. Cukrzyca 2006;55(Suppl_2):S70–S77.
23. Plaisancie P, Bernard C, Chayvialle JA, Cuber JC. Regulacja wydzielania glukagonopodobnego peptydu -1-(7-36) amidu przez neuroprzekaźniki jelitowe i hormony w wyizolowanej naczyniowo perfundowanej okrężnicy szczura. Endokrynologia 1994;135:2398-2403.
24. Meier JJ, Nauck MA, Kranz D i in. Wydzielanie, degradacja i eliminacja glukagonopodobnego peptydu 1 i polipeptydu hamującego żołądek u pacjentów z przewlekłą niewydolnością nerek i zdrowych osób kontrolnych. Cukrzyca 2004;53:654–662.
25. Deacon CF, Johnsen AH, Holst JJ. Degradacja peptydu glukagonopodobnego-1 przez ludzkie osocze in vitro daje skrócony na N-końcu peptyd, który jest głównym endogennym metabolitem in vivo. J Clin Endocrinol Metab 1995;80:952-957.
26. Kieffer TJ, McIntosh CH, Pederson RA. Degradacja zależnego od glukozy polipeptydu insulinotropowego i skróconego glukagonopodobnego peptydu 1 in vitro i in vivo przez peptydazę dipeptydylową IV. Endokrynologia 1995;136:3585–3596.
27. Wei Y, Mojsov S. Tkankowo specyficzna ekspresja ludzkiego receptora glukagonopodobnego peptydu-I: formy mózgowe, sercowe i trzustkowe mają te same wydedukowane sekwencje aminokwasowe. Luty Lett 1995;358:219–224.
28. Doyle ME, Egan JM. Mechanizmy działania glukagonopodobnego peptydu 1 w trzustce. Pharmacol Ther 2007;113:546–593.
29. Wang Y, Egan JM, Raygada M, Nadiv O, Roth J, Montrose-Rafizadeh C. Peptyd podobny do glukagonu -1 wpływa na transkrypcję genów i stabilność przekaźnikowego kwasu rybonukleinowego składników układu wydzielania insuliny w RIN {{ 4}} komórek. Endokrynologia 1995;136:4910–4917.
30. Sygnalizacja receptora Buteau J. GLP{1}}: wpływ na proliferację i przeżycie komórek beta trzustki. Cukrzyca Metab 2008;34 Suppl 2:S73–S77.
31. Li Y, Hansotia T, Yusta B, Ris F, Halban PA, Drucker DJ. Sygnalizacja receptora peptydu glukagonopodobnego -1 moduluje apoptozę komórek beta. J Biol Chem 2003;278:471-478.
32. Hare KJ, Knop FK, Asmar M i in. Zachowana siła hamowania GLP-1 na wydzielanie glukagonu w cukrzycy typu 2. J Clin Endocrinol Metab 2009;94:4679–4687.
33. Little TJ, Pilichiewicz AN, Russo A, et al. Wpływ dożylnego peptydu glukagonopodobnego-1 na opróżnianie żołądka i dystrybucję w żołądku u zdrowych osób: związki z poposiłkowymi reakcjami glikemicznymi i insulinemicznymi. J Clin Endocrinol Metab 2006;91:1916-1923.
34. Toft-Nielsen MB, Madsbad S, Holst JJ. Ciągły podskórny wlew glukagonopodobnego peptydu 1 obniża poziom glukozy w osoczu i zmniejsza apetyt u pacjentów z cukrzycą typu 2. Opieka nad cukrzycą 1999;22:1137–1143.
35. Asmar A, Cramon PK, Simonsen L i in. Zwiększenie objętości płynu zewnątrzkomórkowego ujawnia natriuretyczne działanie GLP-1: funkcjonalną GLP-1-oś nerkową u człowieka. J Clin Endocrinol Metab 2019;104:2509–2519.
36. Crajoinas RO, Oricchio FT, Pessoa TD i in. Mechanizmy pośredniczące w działaniach moczopędnych i natriuretycznych hormonu inkretyny, peptydu glukagonopodobnego-1. Am J Physiol Renal Physiol 2011;301:F355-F363.
37. Trujillo JM, Nuffer W. Agoniści receptora GLP{1}} dla cukrzycy typu 2: najnowsze osiągnięcia i nowe środki. Farmakoterapia 2014;34:1174–1186.
38. Drucker DJ, Nauck MA. Układ inkretynowy: agoniści receptora glukagonopodobnego peptydu -1 i inhibitory dipeptydylopeptydazy -4 w cukrzycy typu 2. Lancet 2006;368:1696-1705.
39. Meier JJ. Agoniści receptora GLP-1 do zindywidualizowanego leczenia cukrzycy typu 2. Nat Rev Endocrinol 2012;8:728–742.
40. Neumiller JJ. Farmakologia inkretyn: przegląd efektu inkretyn i aktualnych terapii opartych na inkretynach. Cardiovasc Hematol Agents Med Chem 2012;10:276–288.
41. Jespersen MJ, Knop FK, Christensen M. GLP{1}} agoniści cukrzycy typu 2: rozważania farmakokinetyczne i toksykologiczne. Opinia eksperta Drug Metab Toxicol 2013;9:17–29.
42. Pfeffer MA, Claggett B, Diaz R i in. Liksysenatyd u pacjentów z cukrzycą typu 2 i ostrym zespołem wieńcowym. N Engl J Med 2015;373:2247–2257.
43. Muskiet MH, Tonneijck L, Huang Y i in. Wyniki liksysenatydu i nerek u pacjentów z cukrzycą typu 2 i ostrym zespołem wieńcowym: analiza eksploracyjna randomizowanego, kontrolowanego placebo badania ELIXA. Lancet Cukrzyca Endocrinol 2018;6:859– 869.
44. Marso SP, Daniels GH, Brown-Frandsen K i in. Liraglutyd i wyniki sercowo-naczyniowe w cukrzycy typu 2. N Engl J Med 2016;375:311–322.
45. Mann JF, Ørsted DD, Brown-Frandsen K, et al. Wyniki leczenia liraglutydem i nerek w cukrzycy typu 2. N Engl J Med 2017;377:839–848.
46. Marso SP, Bain SC, Consoli A i in. Semaglutyd i wyniki sercowo-naczyniowe u pacjentów z cukrzycą typu 2. N Engl J Med 2016;375:1834–1844.
47. Mann JF, Hansen T, Idorn T i in. Wpływ podskórnego semaglutydu raz w tygodniu na czynność nerek i bezpieczeństwo u pacjentów z cukrzycą typu 2: analiza post hoc randomizowanych badań kontrolowanych SUSTAIN 1-7. Lancet Cukrzyca Endocrinol 2020;8:880–893.
48. Holman RR, Bethel MA, Mentz RJ i in. Wpływ eksenatydu raz w tygodniu na wyniki sercowo-naczyniowe w cukrzycy typu 2. N Engl J Med 2017;377:1228–1239.
49. Bethel MA, Mentz RJ, Merrill P i in. Wyniki mikronaczyniowe i sercowo-naczyniowe w zależności od czynności nerek u pacjentów leczonych eksenatydem raz w tygodniu: spostrzeżenia z badania EXSCEL. Opieka nad cukrzycą 2020;43:446–452.
50. Muskiet MH, Bunck MC, Heine RJ i in. Eksenatyd podawany dwa razy na dobę nie wpływa na czynność nerek ani albuminurię w porównaniu z insuliną glargine w dawce miareczkowanej u pacjentów z cukrzycą typu 2: analiza post hoc 52-tygodniowego badania z randomizacją. Diabetes Res Clin Pract 2019;153:14–22.
51. Hernandez AF, Green JB, Janmohamed S i in. Albiglutyd i wyniki sercowo-naczyniowe u pacjentów z cukrzycą typu 2 i chorobami sercowo-naczyniowymi (wyniki Harmony): podwójnie ślepe, randomizowane badanie kontrolowane placebo. Lancet 2018;392:1519–1529.
52. Tuttle KR, Lakshmanan MC, Rayner B i in. Dulaglutyd w porównaniu z insuliną glargine u pacjentów z cukrzycą typu 2 i przewlekłą chorobą nerek o nasileniu umiarkowanym do ciężkiego (AWARD{4}}): wieloośrodkowe, otwarte, randomizowane badanie. Lancet Cukrzyca Endocrinol 2018;6:605–617.
53. Gerstein HC, Colhoun HM, Dagenais GR, et al. Wyniki dulaglutydu i nerek w cukrzycy typu 2: analiza eksploracyjna randomizowanego, kontrolowanego placebo badania REWIND. Lancet 2019;394:131–138.
54. Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutyd i wyniki sercowo-naczyniowe w cukrzycy typu 2 (REWIND): podwójnie ślepe, randomizowane badanie kontrolowane placebo. Lancet 2019;394:121–130.
55. Husain M, Birkenfeld AL, Donsmark M i in. Doustny semaglutyd i wyniki sercowo-naczyniowe u pacjentów z cukrzycą typu 2. N Engl J Med 2019;381:841–851.
56. Gerstein HC, Sattar N, Rosenstock J, et al. Wyniki sercowo-naczyniowe i nerkowe z efpeglenatydem w cukrzycy typu 2. N Engl J Med 2021;385:896–907.
57. Coca SG, Ismail-Beigi F, Haq N, Krumholz HM, Parikh CR. Rola intensywnej kontroli glikemii w rozwoju nerkowych punktów końcowych w cukrzycy typu 2: systematyczny przegląd i metaanaliza intensywnej kontroli glikemii w cukrzycy typu 2. Arch Intern Med 2012;172:761–769.
58. Tuttle KR, Bruton JL, Perusek MC, Lancaster JL, Kopp DT, DeFronzo RA. Wpływ ścisłej kontroli glikemii na odpowiedź hemodynamiczną nerek na aminokwasy i powiększenie nerek w cukrzycy insulinozależnej. N Engl J Med 1991;324:1626–1632.
59. Blonde L, Jendle J, Gross J i in. Dulaglutyd podawany raz w tygodniu w porównaniu z insuliną glargine stosowaną przed snem, obie w skojarzeniu z insuliną lispro podawaną do posiłków, u pacjentów z cukrzycą typu 2 (AWARD{3}}): randomizowane, otwarte badanie fazy 3, równoważności. Lancet 2015;385:2057–2066.
60. Mosenzon O, Blicher TM, Rosenlund S, et al. Skuteczność i bezpieczeństwo doustnego semaglutydu u pacjentów z cukrzycą typu 2 i umiarkowanymi zaburzeniami czynności nerek (PIONEER 5): kontrolowane placebo, randomizowane badanie fazy 3a. Lancet Cukrzyca Endocrinol 2019;7:515–527.
61. Lingvay I, Catarig AM, Frias JP i in. Skuteczność i bezpieczeństwo semaglutydu podawanego raz w tygodniu w porównaniu z codzienną kanagliflozyną jako dodatkiem do metforminy u pacjentów z cukrzycą typu 2 (SUSTAIN 8): podwójnie ślepa faza 3b, randomizowane badanie kontrolowane. Lancet Cukrzyca Endocrinol 2019;7:834–844.
62. Nauck M, Rizzo M, Johnson A, Bosch-Traberg H, Madsen J, Cariou B. Liraglutyd podawany raz dziennie w porównaniu z liksysenatydem jako dodatek do metforminy w cukrzycy typu 2: 26-tygodniowe randomizowane badanie kliniczne test. Opieka nad cukrzycą 2016;39:1501–1509.
63. Choroba nerek: poprawa globalnych wyników (KDIGO) Diabetes Work Group. Wytyczne KDIGO 2020 dotyczące postępowania w cukrzycy w przewlekłej chorobie nerek. Nerki Int 2020;98(4S): S1–S115.
64. Vitale M, Haxhi J, Cirrito T, Pugliese G. Ochrona nerek za pomocą agonistów receptora glukagonopodobnego peptydu{2}}. Curr Opin Pharmacol 2020;54:91–101.
65. Dalsgaard NB, Vilsbøll T, Knop FK. Wpływ agonistów receptora glukagonopodobnego peptydu -1 na czynniki ryzyka sercowo-naczyniowego: narracyjny przegląd bezpośrednich porównań. Cukrzyca Obes Metab 2018;20:508–519.
66. Mosterd CM, Bjornstad P, van Raalte DH. Nefroprotekcyjne działanie agonistów receptora GLP-1: na czym stoimy? J Nephrol 2020;33:965–975.
67. Kamanna VS, Roh DD, Kirschenbaum MA. Hiperlipidemia i choroba nerek: koncepcje wywodzące się z histopatologii i biologii komórki kłębuszków nerkowych. Histol Histopatol 1998;13:169-179.
68. Sun F, Wu S, Wang J i in. Wpływ agonistów receptora glukagonopodobnego peptydu -1 na profile lipidowe wśród cukrzycy typu 2: przegląd systematyczny i metaanaliza sieciowa. Clin Ther 2015;37:225–241.
69. Wøjdemann M, Wettergren A, Sternby B, et al. Hamowanie wydzielania ludzkiej lipazy żołądkowej przez peptyd glukagonopodobny-1. Dig Dis Sci 1998;43:799–805.
70. Xiao C, Bandsma RH, Dash S, Szeto L, Lewis GF. Eksenatyd, agonista receptora glukagonopodobnego peptydu -1, gwałtownie hamuje produkcję lipoprotein jelitowych u zdrowych ludzi. Arterioscler Thromb Vasc Biol 2012;32:1513–1519.
71. Ben-Shlomo S, Zvibel I, Schnell M, et al. Peptyd glukagonopodobny-1 zmniejsza lipogenezę w wątrobie poprzez aktywację kinazy białkowej aktywowanej przez AMP. J Hepatol 2011;54:1214–1223.
72. Ding X, Saxena NK, Lin S, Gupta NA, Anania FA. Eksendyna -4, agonista receptora glukagonopodobnego białka -1 (GLP{4}}), odwraca stłuszczenie wątroby u myszy ob/ob. Hepatologia 2006;43:173–181.
73. Kooijman S, Wang Y, Parlevliet ET i in. Centralna sygnalizacja receptora GLP{1}} przyspiesza klirens osoczowy triacyloglicerolu i glukozy poprzez aktywację brunatnej tkanki tłuszczowej u myszy. Diabetologia 2015;58:2637–2646.
74. Beiroa D, Imbernon M, Gallego R i in. Agonizm GLP{1}} stymuluje termogenezę i brązowienie brunatnej tkanki tłuszczowej poprzez podwzgórzowy AMPK. Cukrzyca 2014;63:3346–3358.
75. Pyke C, Heller RS, Kirk RK i in. Lokalizacja receptora GLP{1}} w tkance małpy i człowieka: nowa dystrybucja ujawniona dzięki obszernie zweryfikowanemu przeciwciału monoklonalnemu. Endokrynologia 2014;155:1280–1290.
76. Schlatter P, Beglinger C, Drewe J, Gutmann H. Ekspresja receptora glukagonopodobnego peptydu 1 w pierwotnych komórkach proksymalnych kanalików świńskich. Regul Pept 2007;141:120–128.
77. Fujita H, Sakamoto T, Komatsu K i in. Redukcja aktywności krążącej dysmutazy ponadtlenkowej u chorych na cukrzycę typu 2 z mikroalbuminurią i jej modulacja przez terapię telmisartanem. Hypertens Res 2011;34:1302–1308.
78. Yin W, Jiang Y, Xu S i in. Kinaza białkowa C i kinaza białkowa A biorą udział w ochronie rekombinowanego ludzkiego peptydu glukagonopodobnego -1 na kłębuszkach i kanalikach u szczurów z cukrzycą. J Diabetes Investig 2019;10:613–625.
79. Hendarto H, Inoguchi T, Maeda Y i in. Liraglutyd analogowy GLP{1}} chroni przed stresem oksydacyjnym i albuminurią u szczurów z cukrzycą indukowaną streptozotocyną poprzez hamowanie nerkowych oksydaz NAD(P)H za pośrednictwem kinazy białkowej A. Metabolizm 2012;61:1422–1434.
80. Wang C, Li C, Peng H i in. Aktywacja szlaku Nrf{1}}ARE łagodzi uszkodzenia wywołane hiperglikemią w podocytach myszy. Cell Physiol Biochem 2014;34:891–902.
81. Zhou T, Zhang M, Zhao L, Li A, Qin X. Aktywacja Nrf2 przyczynia się do ochronnego działania eksendyny -4 przeciwko indukowanemu przez angiotensynę II starzeniu się komórek mięśni gładkich naczyń. Am J Physiol Komórka Physiol 2016;311:C572-C582.
82. Ye Y, Zhong X, Li N, Pan T. Ochronne działanie liraglutydu na podocyty kłębuszków nerkowych u otyłych myszy poprzez hamowanie szlaku NF-κB i MAPK, w którym pośredniczy czynnik zapalny TNF- -. Obes Res Clin Pract 2019; 13: 385–390.
83. Kodera R, Shikata K, Kataoka HU i in. Agonista receptora glukagonopodobnego peptydu -1 łagodzi uszkodzenie nerek poprzez działanie przeciwzapalne bez obniżania poziomu glukozy we krwi w szczurzym modelu cukrzycy typu 1. Diabetologia 2011;54:965–978.
84. Chaudhuri A, Ghanim H, Vora M i in. Eksenatyd wywiera silne działanie przeciwzapalne. J Clin Endocrinol Metab 2012;97:198–207.
85. Bunck MC, Diamant M, Eliasson B i in. Eksenatyd wpływa na krążące biomarkery ryzyka sercowo-naczyniowego niezależnie od zmian składu ciała. Opieka nad cukrzycą 2010;33:1734–1737.
86. Zhang H, Zhang X, Hu C, Lu W. Eksenatyd zmniejsza transformujący czynnik wzrostu w moczu - 1 i wydalanie kolagenu typu IV u pacjentów z cukrzycą typu 2 i mikroalbuminurią. Prasa do krwi nerkowej Res 2012;35:483–488.
87. Hogan AE, Gaoatswe G, Lynch L i in. Terapia analogiem peptydu glukagonopodobnego 1 bezpośrednio moduluje wrodzone zapalenie o podłożu immunologicznym u osób z cukrzycą typu 2. Diabetologia 2014;57:781–784.
88. Rizzo M, Abate N, Chandalia M i in. Liraglutyd zmniejsza stres oksydacyjny i przywraca poziom oksygenazy hemowej -1 oraz greliny u pacjentów z cukrzycą typu 2: prospektywne badanie pilotażowe. J Clin Endocrinol Metab 2015;100:603–606.
89. Yip KP, Tse CM, McDonough AA, Marsh DJ. Redystrybucja izoformy wymiennika Na plus / H plus NHE3 w kanalikach proksymalnych wywołana ostrym i przewlekłym nadciśnieniem tętniczym. Am J Physiol 1998;275:F565-F575?
90. Ronn J, Jensen EP, Wewer Albrechtsen NJ, Holst JJ, Sorensen CM. Peptyd podobny do glukagonu -1 ostro wpływa na przepływ krwi przez nerki i szybkość przepływu moczu u szczurów z samoistnym nadciśnieniem pomimo znacznie zmniejszonej ekspresji receptorów GLP {3}} w nerkach. Przedstawiciel firmy Physiol 2017;5:e13503.
91. Skov J, Dejgaard A, Frøkiær J, et al. Peptyd podobny do glukagonu-1 (GLP-1): wpływ na hemodynamikę nerek i układ renina-angiotensyna-aldosteron u zdrowych mężczyzn. J Clin Endocrinol Metab 2013;98:E664-E671.
92. Skov J, Pedersen M, Holst JJ i in. Krótkoterminowy wpływ liraglutydu na czynność nerek i hormony wazoaktywne w cukrzycy typu 2: randomizowane badanie kliniczne. Cukrzyca Obes Metab 2016;18:581–589.
93. von Scholten BJ, Hansen TW, Goetze JP, Persson F, Rossing P. Agonista receptora glukagonopodobnego peptydu 1 (GLP{3}} RA): długotrwały wpływ na czynność nerek u pacjentów z cukrzycą typu 2. J Powikłania cukrzycy 2015;29:670–674.
94. Pocai A, Carrington PE, Adams JR i in. Podwójny agonizm glukagonopodobnego peptydu 1/receptora glukagonu odwraca otyłość u myszy. Cukrzyca 2009;58:2258–2266.
95. Capozzi ME, Svendsen B, Encisco SE i in. Ton komórkowy jest określany przez peptydy proglukagonu poprzez sygnalizację cAMP. JCI Insight 2019;4:e126742.
96. Frias JP, Nauck MA, Van J i in. Skuteczność i bezpieczeństwo LY3298176, nowego podwójnego agonisty receptora GIP i GLP -1, u pacjentów z cukrzycą typu 2: randomizowane, kontrolowane placebo i aktywne badanie porównawcze fazy 2. Lancet 2018;392:2180–2193.
97. Madsen KB, Askov-Hansen C, Naimi RM i in. Ostre skutki ciągłych wlewów peptydu glukagonopodobnego (GLP)-1, GLP{4}} i kombinacji (GLP-1 plus GLP{6}}) na wchłanianie jelitowe w zespole krótkiego jelita (SBS): badanie kontrolowane placebo. Regul Pept 2013;184:30–39.
98. Müller TD, Sullivan LM, Habegger K i in. Przywrócenie odpowiedzi leptyny u otyłych myszy indukowanych dietą przy użyciu zoptymalizowanego analogu leptyny w połączeniu z eksendyną -4 lub FGF21. J Pept Sci 2012;18:383–393.
99. Suarez-Pinzon WL, Power RF, Yan Y, Wasserfall C, Atkinson M, Rabinovitch A. Terapia skojarzona z peptydem glukagonopodobnym -1 i gastryną przywraca normoglikemię u myszy NOD z cukrzycą. Cukrzyca 2008;57:3281–3288.
100. Trevaskis JL, Mack CM, Sun C i in. Poprawiona kontrola glukozy i obniżona masa ciała u gryzoni z podwójnym mechanizmem działania hybryd peptydowych. PLoS One 2013;8:e78154.
101. Neary NM, Small CJ, Druce MR i in. Peptyd YY3-36 i peptyd glukagonopodobny-17-36 hamują addytywnie przyjmowanie pokarmu. Endokrynologia 2005;146:5120–5127.
102. Gutzwiller JP, Degen L, Matzinger D, Prestin S, Beglinger C. Interakcja między GLP{1}} a CCK{2}} w hamowaniu przyjmowania pokarmu i apetytu u mężczyzn. Am J Physiol Regul Integr Comp Physiol 2004;287:R562-R567.
103. Balena R, Hensley IE, Miller S, Barnett AH. Terapia skojarzona z agonistami receptora GLP{1}} i insuliną bazową: przegląd systematyczny literatury. Cukrzyca Obes Metab 2013;15:485–502.
104. Bech EM, Voldum-Clausen K, Pedersen SL i in. Adrenomedulina i peptyd glukagonopodobny-1 mają addytywny wpływ na przyjmowanie pokarmu u myszy. Biomed Pharmacother 2019;109:167–173.
105. Pan Q, Lin S, Li Y i in. Nowy podwójny agonista GLP{1}} i FGF21 ma potencjał terapeutyczny w leczeniu cukrzycy i niealkoholowego stłuszczeniowego zapalenia wątroby. EBioMedycyna 2021;63:103202.
106. Finan B, Yang B, Ottaway N i in. Ukierunkowane dostarczanie estrogenu odwraca zespół metaboliczny. Nat Med 2012;18:1847–1856.
107. Quarta C, Clemmensen C, Zhu Z, et al. Integracja molekularna działania inkretyn i glukokortykoidów odwraca dysfunkcję immunometaboliczną i otyłość. Cell Metab 2017;26:620–632.
108. Chodorge M, Celeste AJ, Grimsby J i in. Inżynieria fuzyjna peptydu analogowego GLP- 1/przeciwciała anty-PCSK9 do leczenia cukrzycy typu 2. Przedstawiciel nauk ścisłych 2018;8:17545.
109. Clemmensen C, Finan B, Fischer K, et al. Podwójny agonizm receptora melanokortyny-4 i receptora GLP-1 wzmacnia korzyści metaboliczne u otyłych myszy wywołanych dietą. EMBO Mol Med 2015;7:288–298.
110. Jouihan H, Will S, Guionaud S, et al. Lepsze zmniejszenie stłuszczenia i zwłóknienia wątroby dzięki jednoczesnemu podawaniu agonisty receptora glukagonopodobnego -1 i kwasu obetycholowego u myszy. Mol Metab 2017;6:1360–1370.
111. Frías JP, Guja C, Hardy E i in. Eksenatyd raz w tygodniu plus dapagliflozyna raz dziennie w porównaniu z samym eksenatydem lub dapagliflozyną u pacjentów z cukrzycą typu 2 niedostatecznie kontrolowaną za pomocą metforminy w monoterapii (CZAS TRWANIA -8): 28-tydzień, wieloośrodkowe, podwójnie zaślepione, faza 3, randomizowane Kontrolowane badanie. Lancet Cukrzyca Endocrinol 2016;4:1004–1016.
Ji Hee Yu, So Young Park, Da Young Lee, Nan Hee Kim, Ji A Seo
Oddział Endokrynologii i Metabolizmu, Oddział Chorób Wewnętrznych, Koreański Szpital Uniwersytecki Ansan, Korea University College of Medicine, Ansan, Republika Korei






