Lipidomika ujawnia wywołane cisplatyną zmiany lipidów w nerkach podczas ostrego uszkodzenia nerek i ich osłabienie przez cylastatynę
Feb 21, 2022
Abstrakcyjny: Nefrotoksyczność jest głównym powikłaniem chemioterapii opartej na cisplatynie, prowadzącym do ostregouszkodzenie nerekw ca. 30 procent pacjentów, bez interwencji zapobiegawczej lub leczenia dostępnego do użytku klinicznego. Cilastatyna okazała się wywierać działanie nefroprotekcyjne w terapiach cisplatyną w modelach in vitro i in vivo, po wprowadzeniu niedawno do badań klinicznych. Głębsze zrozumienie na poziomie molekularnym wywołanej cisplatynąuszkodzenie nereka wpływ potencjalnych środków ochronnych może być kluczem do opracowania skutecznych terapii nefroprotekcyjnych i ustanowienia nowych biomarkerówuszkodzenie nerekoraznefroprotekcja. Do oznaczania ilościowego 108 rodzajów lipidów (obejmujących fosfolipidy, sfingolipidy oraz wolny i estryfikowany cholesterol) zastosowano ukierunkowane podejście lipidomiczne, wykorzystujące LC-MS/MS.nerkawyciągi z kory i rdzenia szczurów leczonych cisplatyną i/lub cylastatyną. Stwierdzono, że po leczeniu cisplatyną odpowiednio do 56 i 63 gatunków lipidów uległo zmianie w korze i rdzeniu. Jednoczesne leczenie cylastatyną osłabiało wiele z tych zmian lipidowych, całkowicie lub częściowo w odniesieniu do poziomów kontrolnych. Analiza wielowymiarowa wykazała, że rodzaje lipidów można wykorzystać do rozróżnianiauszkodzenie nerekoraznefroprotekcja, przy czym estry cholesterolu są najbardziej dyskryminującymi gatunkami, wraz z sulfatydami i fosfolipidami. Potencjalne biomarkery diagnostyczne indukowanej cisplatyną uszkodzenie nereki cylastatynęnefroprotekcjazostały również znalezione.
Słowa kluczowe:lipidomika; cisplatyna; ostre uszkodzenie nerek; cylastatyna; nefroprotekcja; biomarkery; estry cholesterolu; sfingolipidy; fosfolipidy; chemoterapia
Wstęp Nefrotoksyczność jest poważnym skutkiem ubocznym chemioterapii cisplatyną [1], z ostrymuszkodzenie nerek(AKI) opracowywany w ca. 30 proc. leczonych pacjentów [2]. Jest to również główny czynnik ograniczający dawkę i poważna wada terapii opartych na cisplatynie, jednej z najistotniejszych metod leczenia guzów litych [2]. Cisplatyna gromadzi się i powoduje obrażenianerkowykomórki nabłonka kanalika proksymalnego (RPTEC), a uszkodzenie szczególnie lokalizuje się w segmencie S3 kanalika proksymalnego, schodząc odnerkowykora w kierunku połączenia korowo-rdzeniowego i rdzenia zewnętrznego [3]. Sugerowano jednak również bezpośrednie uszkodzenie rdzeniowej pętli Henlego [4,5]. Seria zdarzeń komórkowych ma miejsce w związku znerkowyuszkodzenie komórek kanalików, następujące po wychwytywaniu cisplatyny, w tym stres oksydacyjny, stres nitrozowy, uszkodzenie naczyń, stan zapalny, uszkodzenie mitochondriów lub zahamowanie Na+, K+-ATPazy w błonie komórkowej oraz stres retikulum endoplazmatycznego, po którym następuje śmierć komórek kanalików proksymalnych, głównie przez apoptoza (zarówno obejmująca szlaki wewnętrzne, jak i zewnętrzne) lub martwica, prowadząca do utratyczynność nerek[2,6,7]. Przejawia się to spadkiem współczynnika przesączania kłębuszkowego (GFR) oraz stężenia magnezu i potasu w surowicy, przy zwiększonym poziomie azotu mocznikowego (BUN) we krwi i kreatyniny w surowicy [2].

Zbadano różne podejścia donefroprotekcjapodczas terapii cisplatyną zarówno in vitro, jak i in vivo, w oparciu o szereg celów molekularnych [7–9]. Jednak możliwe zaburzenie cytotoksycznego działania cisplatyny na komórki nowotworowe i często niepełny efekt ochronny ograniczyły rozwój renoprotektorów [9]. W rezultacie nie ma interwencji do użytku klinicznego, która skutecznie zapobiegałaby lub leczyła AKI wywołane cisplatyną [7]. Głębsze zrozumienie szlaków molekularnych związanych z AKI indukowanym cisplatyną i potencjalnych celów dlanefroprotekcjawydaje się w tym względzie kluczowa.
Udowodniono, że cylastatyna skutecznie chroninerkaod uszkodzeń spowodowanych przez kilka czynników, w tym cisplatynę [10,11], gentamycynę [12], wankomycynę [13], cyklosporynę A i takrolimus [14], zarówno w modelach in vitro, jak i in vivo. Cilastatyna wywiera działanie ochronne poprzez selektywne hamowanienerkowydehydropeptydaza I (DHP-I) zlokalizowana w raftach lipidowych na rąbku szczoteczkowym RPTECs [11]. W rezultacie cylastatyna osłabia procesy obejmujące eksternalizację błony, takie jak apoptoza zewnętrzna za pośrednictwem Fas i progresjauszkodzenie nerekpo znieważeniu toksycznym zostaje zatrzymany [11]. Oprócz zewnętrznego upośledzenia apoptozy przez cylastatynę, stwierdzono zmniejszenie stresu oksydacyjnego, stanu zapalnego i akumulacji związków nefrotoksycznych [10–13,15,16]. Zatem,czynność nerekszczątki zachowane podczas jednoczesnego leczenia cisplatyną i cylastatyną [11]. Ostatnio cylastatyna pomyślnie zakończyła badania kliniczne I fazy pod kątem jej zastosowania jako nefroprotektor i wkrótce wejdzie w badania II fazy. Niedawne obiecujące badanie wykazało również, że cylastatyna (podawana jako imipenem z cylastatyną) może wywierać działanie renoprotekcyjne u pacjentów z rakiem otrzewnej podczas hipertermicznego dootrzewnowego leczenia cisplatyną [17].
W ostatnich latach technologie omiczne, zwłaszcza proteomika [18,19] i metabolomika [20–23], okazały się przydatne do odkrycia nowych wczesnych biomarkerów diagnostycznych AKI, oprócz BUN czy kreatyniny w surowicy [18,20]. Ponadto analiza metabolomiczna może dostarczyć cennych informacji dla zrozumienia mechanizmów cisplatyny nefrotoksyczności [5,24] oraz terapeutycznego wpływu potencjalnych nefroprotektorów [25–27].
W szczególności lipidomika może również dostarczyć odpowiednich informacji dotyczących:choroba nerek[28], biorąc pod uwagę, że lipidy pełnią kluczowe role strukturalne, sygnalizacyjne i metaboliczne, i mogą być zmieniane w komórkach, tkankach i biofluidach pod wpływemnerkowystany patologiczne [29,30]. W związku z tym stwierdzono podwyższony poziom trójglicerydów i niezestryfikowanych kwasów tłuszczowych wnerkapodczas leczenia cisplatyną [31], oprócz talowych lipidów neutralnych [32]. Podwyższony poziom sfingolipidów — ceramidów (Cer) i heksozyloceramidów (HexCer) — zaobserwowano również wnerkowykora mózgowa podczas AKI wywołanej cisplatyną [33]. Z drugiej strony stwierdzono również zmiany w rodzajach fosfolipidów, w tym fosfatydylocholiny (PC), fosfatydyloetanoloaminy (PE) i lizofosfatydylocholiny (LPC).tkanka nerkowalub komórki podczas leczenia cisplatyną [26]. Stwierdzono również zmiany poziomów różnych gatunków LPC w surowicy szczurów po podaniu cisplatyny [23]. Co więcej, spektrometria mas obrazująca niecelowane podejście półilościowe umożliwiło porównanie dystrybucji lipidów u szczuranerkai zasugerował, że cis platyna prowadzi do zmian w różnych fosfolipidach (PC, PE, fosfatydyloglicerole (PG), fosfatydyloinozytole (PI), fosfatydyloseryny (PS), kwasy fosfatydowe (PA)), sulfatydy (Sulf) lub kardiolipiny) [34] (wykazujące odmienne zachowanie w korze i rdzeniu), podczas gdy jednoczesne leczenie cylastatyną osłabiało niektóre z tych zmian [4].
W tej pracy poszliśmy o krok dalej i przyjrzeliśmy się bliżej ważnym strukturalnym lipidom wnerkatakie jak fosfolipidy (PC, LPC i PE), sfingolipidy (Sulf, sfingomieliny (SM), dihydrosfingomieliny (dhSM), Cer, dihydroceramidy (dhCer), HexCer, dihydroheksozyloceramidy (dhHexCer) oraz wolny cholesterol (FC) i jego zestryfikowany formy (estry cholesterolu (CE)), obejmujące nowe klasy i gatunki lipidów oraz wykorzystujące bardziej wiarygodne ukierunkowane podejście ilościowe oparte na chromatografii cieczowej połączonej z analizą tandemowej spektrometrii masowej (LC-MS/MS). Ogółem oznaczono 108 rodzajów lipidów, zarówno nanerkowywyciągi z kory i rdzenia z leczonych szczurów, aby lepiej zrozumieć nefrotoksyczne działanie cisplatyny i nefroprotekcyjne działanie cylastatyny. Nowe informacje na temat wpływu cisplatyny związanej z AKI nanerkowyuzyskano rodzaje lipidów i uzyskano dodatkowe informacje na temat ochronnego działania cylastatyny, co doprowadziło do osłabienia niektórych specyficznych zmian lipidowych spowodowanych przez cisplatynę zarówno wnerkowykora lub rdzeń. Różnorodne potencjalne biomarkery indukowanej cisplatynąuszkodzenie nerekoraznefroprotekcjaz cylastatyną również znaleziono.
Wyniki
Działanie ochronne cylastatyny przeciwko uszkodzeniom nerek wywołanym przez cisplatynę
Ocenaczynność nereku szczurów leczonych cisplatyną i/lub cylastatyną przeprowadzono najpierw z wykorzystaniem kilku wskaźników biochemicznych w surowicy i moczu. Jak pokazano w Tabeli 1, stężenie kreatyniny w surowicy, BUN, białka w moczu, objętość moczu i frakcjonowane wydalanie sodu i potasu były istotnie zwiększone dzięki leczeniu cisplatyną w porównaniu z grupą kontrolną, podczas gdy jednoczesne leczenie cylastatyną i cisplatyną prowadziło do ich zmniejszenia w porównaniu z grupą kontrolną. z poziomami kontrolnymi. Z drugiej strony, GFR był obniżony u szczurów leczonych cisplatyną w porównaniu z próbkami kontrolnymi, podczas gdy jednoczesne podawanie cylastatyny zmniejszyło ten efekt. Te wyniki potwierdzająuszkodzenie nerekindukowana przez cisplatynę i ochrona przez cylastatynę. Sama cylastatyna nie wykazywała żadnego wpływu naczynność nerekparametry.

Analizę histopatologiczną przeprowadzono również w skrawkach barwionych hematoksyliną/eozyną w celu zbadania zmian morfologicznych związanych zuszkodzenie nerek. Rycina 1 przedstawia oznaki uszkodzenia w proksymalnym odcinku wywołane cisplatynąnerkowykanaliki, w tym obrzęk kanalików, oderwanie się resztek komórek lub utrata błony rąbka szczoteczkowego (ryc. 1C, G, I). Akumulację wałeczków białkowych zaobserwowano również w kanalikach kory i rdzenia (rys. 1C, G, odpowiednio). Jest to sprzeczne z prawidłową morfologią obserwowaną w grupie kontrolnej lub cylastatynie w korze (odpowiednio ryc. 1A, B) i rdzeniu (odpowiednio ryc. 1E, F). Jednoczesne leczenie cisplatyną i cisplatyną spowodowało wyraźne zmniejszenie wszystkich tych wywołanych cisplatyną zmian w korze i rdzeniu (Figura 1D, H, J).
Cisplatynowa zmiana globalnych klas lipidów nerkowych w korze i rdzeniu. Ochronne działanie Cilastatyny
Wnerkowykora mózgowa i rdzeń, w celu oceny globalnego wpływu cisplatyny na lipidy podczas AKI. Pełne wyniki analizy lipidów znajdują się w Tabeli S1. Jak widać na rycinie 2A, B, dość podobne trendy zaobserwowano w korze i rdzeniu dla wszystkich grup. CE i Cer były istotnie zwiększone, podczas gdy SM, dhSM i PE uległy zmniejszeniu, zarówno w korze mózgowej, jak i rdzeniu podczas leczenia cisplatyną, w porównaniu z grupami kontrolnymi. Wśród nich Cer i CE cierpią na najbardziej widoczne zmiany wywołane cisplatyną. Ponadto, podczas leczenia cisplatyną, dhCer i HexCer były znacząco podwyższone w rdzeniu, podczas gdy w korze, dhHexCer był podwyższony, a LPC i Sulf spadły.

Rycina 1. Analiza histopatologiczna wybarwionych hematoksyliną/eozynąnerkowysekcje przedstawiają ochronę cylastatyną przed uszkodzeniami wywoływanymi przez cisplatynę. Obrazy pokazano w powiększeniu 20x dla kory kontrolnej (A); (B) kora cylastatyny; (C) kora cisplatynowa; (D) cisplatyna plus kora cylastatynowa; (E) rdzeń kontrolny; (F) rdzeń cylastatyny; (G) rdzeń cisplatyny; i (H) cisplatyna plus rdzeń cylastatynowy. Skala od A do H przedstawia 100 µm. Szczegółowe obrazynerkowykanaliki w powiększeniu 60x są wyświetlane dla (I) cisplatyny i (J) cisplatyny z cylastatyną. Skala dla I i J reprezentuje 25 µm.Nerkowyreprezentowane są wskaźniki uszkodzeń: →: nagromadzenie łusek białkowych wnerkowykanaliki. & region: obrzęk kanalików. *: utrata błony rąbka szczoteczkowego. #: oderwanie szczątków komórkowych.
Jednoczesne podawanie cylastatyny i cisplatyny miało tendencję do osłabiania niektórych z tych wywołanych cisplatyną zmian lipidowych, co skutkuje brakiem różnic w stosunku do grup kontrolnych w przypadku poziomów Cer i dhHexCer w korze lub dhCer, HexCer, SM, dhSM i PE poziomy w rdzeniu. Ponadto, w przypadku wywołanego cisplatyną wzrostu CE w korze, cylastatyna podawana razem z cisplatyną prowadziła do znacznego obniżenia poziomów w porównaniu z grupą cisplatyny, chociaż poprawa była częściowa w odniesieniu do grup koiatrolowych. Pozostałe klasy lipidów zmienione przez cisplatynę pozostały nieodzyskane podczas jednoczesnego leczenia cilastatisi. Z drugiej strony sama cylastatyna nie miała wpływu na korę i szpik, z wyjątkiem LPC i dhCer w korze, które wydawały się odpowiednio zmniejszone i zwiększone w porównaniu z grupą kontrolną. Całkowite poziomy FC, PC i dhHexCer nie wykazały istotnych zmian w korze i rdzeniu po leczeniu cisplatyną.
Rycina 2C,D przedstawia mapy cieplne korelacji dla klas lipidów odpowiednio w korze i rdzeniu, oferując podobne trendy.

Alitracja poszczególnych gatunków lipidów nerkowych za pomocą leczenia cisplatyną. Efekt łagodzący cylastatynę
Estry CholestesolAnaliza pięciu poszczególnych gatunków CE (CE 18:1, CE 18:2, CE 18:0, CE 20:4 i CE 22:6) przeprowadzona wnerkowykora i rdzeń wykazały, że cisplatyna znacząco zwiększała każdy z nich w porównaniu z poziomem kontrolnym (ryc. 3). Z drugiej strony, jednoczesne podawanie cylastatyny i cisplatyny doprowadziło do ogólnego obniżenia poziomu poszczególnych gatunków CE w odniesieniu do leczenia cisplatyną, co było statystycznie istotne dla wszystkich gatunków CE w korze i CE 18:2 w rdzeniu, co może być widoczne na rycinie 3. Ta poprawa w gatunkach CE kory mózgowej spowodowana równoczesnym stosowaniem cylastatyny była częściowa w porównaniu z poziomami w grupie kontrolnej, podczas gdy nie zaobserwowano statystycznie istotnej poprawy w większości gatunków CE medella (z wyjątkiem CE 18:2) w przypadku jednoczesnego podawania cylastatyny w porównaniu z cisplatyną. Pełne wyniki analizy statystycznej rodzajów lipidów kory i rdzenia przedstawiono odpowiednio w tabelach S2 i S3.

Sfingolipidy: Cer, dhCer, HexCer, dhHexCer, SM, dhSM i SulfW sumie oznaczono 43 gatunki sfingolipidów wnerkowykora mózgowa i rdzeń w celu oceny wpływu leczenia cisplatyną i cylastatyną na ich poziomy, jak pokazano na rycinie 4. W odniesieniu do gatunków Cer (ryc. 4A), dhCer (ryc. 4B), HexCer (ryc. 4C) i dhHexCer (ryc. 4D), jak widać, że leczenie cisplatyną spowodowało znaczny wzrost 19 gatunków z tych czterech klas wnerkowykora i rdzeń. Ponownie, jednoczesne leczenie cisplatyną i cylastatyną wykazuje tendencję do osłabiania działania cisplatyny, z ogólnym spadkiem poziomów lipidów zmienionych cisplatyną w korze i rdzeniu. W rzeczywistości, dla gatunków dhCer (Figura 4B) i dhHexCer (Figura 4D), nie zaobserwowano różnicy między grupami traktowanymi cisplatyną plus cylastatyną a grupami kontrolnymi dla tych gatunków zmienionych cisplatyną, co wskazuje na pełne wyzdrowienie. W przypadku Cer (ryc. 4A) i HexCer (ryc. 4C) ta rezerwa była również w przypadku niektórych zmienionych gatunków, takich jak HexCer 34:1 (kora i rdzeń) oraz HexCer 38:1 i HexCer 42:1 (rdzeń ); Cer 36:1, Cer 38:1, Cer 40:1, Cer 42:1 i Cer 42:2 w korze; oraz Cer 34:1 i Cer 42:2 w rdzeniu, całkowicie lub częściowo odzyskane. Odwrotnie, leczenie cisplatyną i cylastatyną nadal wykazywało znaczące różnice w porównaniu z grupami kontrolnymi dla Cer 36:1, Cer 38:1, Cer 40:1, Cer 42:1 i HexCer 36:1 w rdzeniu, bez wyzdrowienia, wskazując znacznie lepszy efekt regeneracyjny wywierany przez cylastatynę w korze niż w rdzeniu dla Cer i HexCer.
W przypadku gatunków SM (ryc. 4E) i dhSMt (ryc. 4F), cisplatyna prowadziła do zmniejszenia kory i rdzenia dla gatunków o najkrótszym i najdłuższym łańcuchu, co było statystycznie istotne dla SM 34:1, dhSM 34:{{ 5}}, SM 42:2, SM 42:1 i dhSM 42:1. W przeciwieństwie do tego, efekt obserwowany dla leczenia cisplatyną na pośrednie łańcuchy SM i gatunki dhSM w korze i rdzeniu był wzrostem, który był statystycznie istotny dla dhSM 36:0 (zarówno w korze, jak i rdzeniu) i dhSM 4{{ 15}}:0, SM 36:1, SM 38:1 i SM 40:1 w rdzeniu. Jednoczesne podawanie cisplatyny i cylastatyny w wielu przypadkach powodowało normalizację poziomów gatunków SM i dhSM, przy czym SM 34:1, SM 36:1, SM 38:1, SM 40:1, SM 42:2, SM 42:1, dhSM 36:0, dhSM 40:0 i dhSM 42:1 nie wykazują żadnej różnicy w stosunku do grup kontrolnych w rdzeniu. Wreszcie, niektóre gatunki Sulf zostały również zmienione przez traktowanie cisplatyną wnerkowykora i rdzeń, jak pokazano na rycinie 4G. Podczas gdy stwierdzono, że Sulf 40:1 jest znacząco zwiększony zarówno w korze, jak i rdzeniu po leczeniu cisplatyną, inne gatunki, takie jak Sulf-OH 40:1 lub długołańcuchowy Sulf-OH 42:2, Sulf-OH 42:2 uległy zmniejszeniu w korze, przy czym Sulf 42:0 i Sulf-OH 42:1 również uległy zmniejszeniu zarówno w korze, jak i rdzeniu. Cilastatyna podawana razem z cisplatyną ponownie doprowadziła do łagodnego efektu powrotu do zdrowia, szczególnie dla Sulf 40:1 (kora i rdzeń) oraz Sulf 40:2 i Sulf-OH 42:1 (rdzeń), nie wykazując różnicy w porównaniu z grupami kontrolnymi.

Fosfolipidy: PC, PE i LPCOznaczenie ilościowe 60 rodzajów fosfolipidów (28 PC, 20 PE i 12 LPC) przeprowadzono wnerkowykora mózgowa i rdzeń do oceny potencjalnych zmian wywołanych cisplatyną i renoprotekcyjnego działania cylastatyny. Wyniki dla gatunków PC przedstawiono odpowiednio na Rysunku 5A, B. Jak widać, cisplatyna znacząco zmieniła do 19 gatunków PC w korze lub rdzeniu. Większość z tych gatunków PC została zmniejszona przez cisplatynę, z wyjątkiem PC 40:2, PC 40:4 i PC 34:2, które zostały zwiększone w korze. Frakcja wysoce nienasyconych form PC była znacząco zmniejszona zarówno w rdzeniu, jak i korze, podczas gdy frakcja form zawierających dwa wiązania podwójne była znacząco zwiększona, jak widać na Figurze 5C,D. Leczenie zarówno cisplatyną, jak i cylastatyną wykazywało podobne efekty do tych obserwowanych wcześniej, z pewnym obserwowanym efektem osłabiającym, w niektórych przypadkach prowadzącym do pełnej poprawy poziomów PC, bez znaczących różnic w porównaniu z grupą kontrolną lub do częściowej poprawy. Regenerację tę zaobserwowano głównie w Wyniki dla oznaczania gatunków PE w korze i rdzeniu przedstawiono odpowiednio na Ryc. 6A, B. W sumie 16 gatunków PE zostało znacząco zmienionych przez cisplatynę w korze lub rdzeniu, przy czym największą liczbę zmienionych gatunków znaleziono w rdzeniu. W większości przypadków ilość gatunków PE została zmniejszona przez leczenie cisplatyną, z wyjątkiem PE 38:2, PE 40:6 i PE 40:4, które były zwiększone albo w korze, rdzeniu, albo zarówno w korze jak i rdzeniu, odpowiednio. W związku z tym, biorąc pod uwagę całkowitą długość łańcuchów kwasów tłuszczowych w rodzajach PE w rdzeniu, całkowita ilość PE o 34, 36 i 38 C była znacząco zmniejszona w przypadku cisplatyny, podczas gdy gatunki o 40 C wzrosły, jak przedstawiono na Rysunku 6C . Jednoczesne leczenie cisplatyną i cisplatyną osłabiło większość wywołanych cisplatyną zmian w poszczególnych gatunkach PE stwierdzonych w rdzeniu, oferując poziomy bez istotnych różnic w porównaniu z grupami kontrolnymi w 11 z 15 gatunków zmienionych cisplatyną w rdzeniu, z 2 innymi gatunkami PE częściowo odzyskany. Jednak w korze tylko 2 z 11 gatunków zmienionych cisplatyną odzyskano z cylastatyną do poziomów kontrolnych, przy czym częściowo odzyskano 2 dodatkowe gatunki PE. Podobnie do obserwacji dla gatunków PC, frakcja wysoce nienasyconych gatunków PE była znacznie zmniejszona w rdzeniu, podczas gdy frakcja gatunków zawierających wiązania podwójne 1-3 była znacząco zwiększona, jak pokazano na Figurze 6D.


Jeśli chodzi o analizę gatunków LPC, większość zaobserwowanych zmian wywołanych cisplatyną stwierdzono wnerkowykory, gdzie LPC 16:1, LPC 16:0, LPC 18:1, LPC 18:0 , LPC 20:3, LPC 22:6 i LPC 22:5 uległy znacznemu zmniejszeniu wraz z w odniesieniu do próbek kontrolnych, jak widać na Rysunku 7A. Z drugiej strony stwierdzono wzrost LPC 17:1 i LPC 18:2 w rdzeniu podczas leczenia cisplatyną (Figura 7B). Jednoczesne leczenie cisplatyną i cylastatyną nie miało wpływu na regenerację gatunków korowych LPC. Odwrotnie, LPC 17:1 i LPC 18:2 odzyskano w rdzeniu, bez znaczących różnic w porównaniu z próbkami kontrolnymi.

Lipidy nerkowe jako zmienne klasyfikacyjne dlaUszkodzenie nereki Ochrona
Przeprowadzono analizę wielowymiarową przy użyciu wszystkich zmiennych lipidowych zmierzonych w korze i rdzeniu, aby ocenić, czy gatunki te mogą służyć do klasyfikacji grupowej i rozpoznawania indukowanego cisplatynąuszkodzenie nerekoraznefroprotekcjaprzez cylastatynę. Analizę głównych składowych (PCA) i analizę rzutów ortogonalnych na utajone struktury (OPLS-DA) przeprowadzono przy użyciu oddzielnie lipidów kory lub rdzenia, jak pokazano na rycinie 8. Analiza PCA kory (ryc. 8A) i rdzenia (ryc. 8B) Lipidy umożliwiły modelom wyraźne oddzielenie grupy cisplatyny od grupy kontrolnej i cylastatyny, przy czym te dwie ostatnie grupują się ściśle. Z drugiej strony, grupa leczona cisplatyną i cisplatyną miała tendencję do oddzielania się od grupy cisplatyny i znajdowała się pomiędzy grupą kontrolną i cisplatyną, co sugeruje różnice między grupami. Wszystkie modele PCA prezentowały R2 wyższe niż 0.7 i wartości Q2 wyższe niż 0.5.
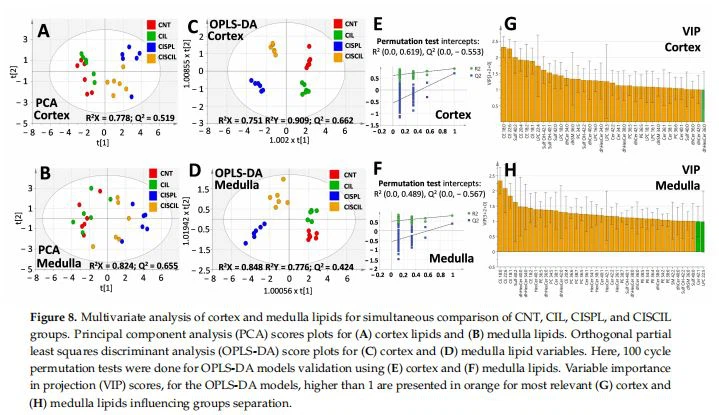
Wielogrupowa analiza OPLS-DA wykazała również wyraźnie oddzielone grupowanie różnych grup, zarówno przy użyciu zmiennych lipidowych kory (Figura 8C), jak i rdzenia (Figura 8D). Modele OPLS-DA prezentowały akceptowalne wartości Q2 i R2 wyższe niż 0.7 i okazały się słuszne podczas testowania permutacji dla 100 iteracji, jak pokazano na rysunku 8E, F. Cechy o zmiennym znaczeniu w projekcji (VIP) wyższe niż 1 można znaleźć na rycinie 8G,H, wskazując odpowiednio lipidy kory lub rdzenia, które mają większy wpływ na rozdział grup. Obejmowały one różne gatunki lipidów z klas CE, sfingolipidów i fosfolipidów. Aby określić specyficzne różnice lipidów między poszczególnymi grupami związane z leczeniem cisplatyną inefroprotekcja, dalszą analizę OPLS-DA przeprowadzono oddzielnie z lipidami kory i rdzenia, jak widać odpowiednio na Figurach 9 i 10. Modele OPLS-DA zbudowano dla cisplatyny w porównaniu z grupą kontrolną, cisplatyny z cylastatyną w porównaniu z cisplatyną oraz dla cisplatyny z cylastatyną w porównaniu z grupą kontrolną. Najbardziej wyróżniającymi się modelami OPLS-DA były te między grupą kontrolną a grupą leczoną cisplatyną lub cisplatyną z cylastatyną, biorąc pod uwagę ich najwyższe wartości R2 i Q2, z odpowiednią walidacją opartą na wynikach testu permutacji z 100 cyklami (ryc. 9A, B, D, E i Rysunek 10A,B,D,E).

Z drugiej strony modele OPLS-DA dla grup cisplatyny plus cylastatyny i cisplatyny, zarówno z wykorzystaniem lipidów kory (ryc. 9C), jak i rdzenia (ryc. 10C), również umożliwiły rozróżnienie grup, z rozsądnymi wartościami R2 i Q2 oraz odpowiednie wyniki walidacji z 100-testów permutacji cykli (Figury 9F i 10F), przy czym lipidy rdzenia są tymi, które wykazują lepszą przewidywalność. Wykresy S dla różnych modeli OPLS-DA przedstawiono na rycinie 9G,H,I i rycinie 10G,H,I, dla cech lipidowych kory lub rdzenia. Gatunki z |p(corr)| wyższe niż 0,5 i wyniki VIP wyższe niż 1 zostały oznaczone na wykresach S jako cechy najbardziej istotne dla dyskryminacji grup. Pełne dane, w tym wartości p(corr) i VIP z modeli OPLS-DA, wraz z jednowymiarowymi statystykami dla każdego gatunku lipidów, można znaleźć w tabelach uzupełniających S2 (lipidy kory mózgowej) i S3 (lipidy rdzenia). Wydaje się jasne, żenerkowylipidy kory mózgowej i rdzenia mogą służyć jako kryteria rozróżniające dla wywołanych cisplatynąuszkodzenie nereki dla cylastatynynefroprotekcjapodczas leczenia cisplatyną.

Lipidy nerkowe jako potencjalne biomarkery uszkodzenia nerek wywołanego cisplatyną W celu wyselekcjonowania potencjalnych biomarkerów lipidowych uszkodzenia nerek
wywołanych przez cisplatynę, zastosowano kombinację wielu kryteriów statystycznie istotnych wartości p z jednoczynnikowej analizy cisplatyny w porównaniu z grupami kontrolnymi, a także wartości p(corr) i VIP stwierdzonych w odpowiednim modelu OPLS-DA. Wybrane lipidy o wartościach p < 0.05;="" fdr="">< 0.1;="" |p(korekta)|=""> 0,5 i VIP > 1 można znaleźć w Tabeli 2 (lipidy kory mózgowej) i Tabeli 3 (lipidy rdzenia), gdzie uwzględniono również krotność zmiany (FC) i pola powierzchni pod krzywą (AUC) dla krzywych charakterystyki operacyjnej odbiornika (ROC).

Jak można zauważyć, odpowiednio w Tabelach 2 i 3 wybrano do 40 lipidów z rdzenia i 27 lipidów z kory, obejmujących CE, sfingolipidy i rodzaje fosfolipidów. Wartości AUC dla krzywych ROC uzyskanych dla każdego lipidu były wyższe niż 0.85 i, w większości przypadków, bliskie 1, co wskazuje na dobrą zdolność odróżniania gatunków między grupami cisplatyny i kontrolnymi. Co godne uwagi, gatunki CE o zwiększonej zawartości cisplatyny (CE 18:1, CE 18:2, CE 18:0, CE 20:4 i CE 22:6) wydają się być najbardziej dyskryminujące cechy zarówno w rdzeniu, jak i korze, wykazując najwyższe wartości FC, VIP, p(corr) i AUC. dhHexCer 34:0 to kolejny podwyższony poziom lipidów w korze z wysokim FC i odpowiednimi wynikami. Z drugiej strony, sulfatydy, takie jak Sulf 42:0, Sulf-OH 40:1 lub Sulf-OH 42:1 są również dość istotne w korze, podczas gdy PE 36:5, PE 38:6, PE 38:5 PC 36:5 lub PC 36:6 są również bardzo ważne w rdzeniu, wszystkie z nich ulegają zmniejszeniu podczas leczenia cisplatyną.

Lipidy nerkowe jako potencjalne biomarkery nefroprotekcji cylastatyny
W celu wyselekcjonowania potencjalnych biomarkerów lipidowych ochrony cylastatyny przed cisplatyną nefrotoksycznym działaniem cisplatyny zastosowano to samo podejście oparte na wielu kryteriach, co w rozdziale 2.5, stosując jednowymiarową analizę cisplatyny z cylastatyną w porównaniu z grupami cisplatyny oraz wartości p(corr) i VIP w odpowiednich Model DA. Wybrane lipidy o wartościach p < 0.05;="" fdr="">< 0.1;="" |p(korekta)|=""> 0,5 i VIP > 1 można znaleźć w Tabeli 4 (lipidy kory mózgowej) i Tabeli 5 (lipidy rdzenia), gdzie obliczono również FC i AUC dla krzywych ROC.

Jak widać w Tabeli 4, wszystkie gatunki CE (CE 18:1, CE 18:2, CE 18:0, CE 20:4 i CE 22:6) w korę mózgową można uznać za najsilniejsze wskaźniki ochrony wywieranej przez cylastatynę, zmniejszając jednocześnie znacząco zmiany wywoływane przez cisplatynę. PE 36:5 i dhHexCer 34:0 w korze są również ważnymi potencjalnymi biomarkerami ochrony cylastatyny, zwłaszcza tej ostatniej, która dzięki cylastatynie ulega całkowitej regeneracji w kierunku poziomów kontrolnych. W odniesieniu do lipidów rdzenia, jak pokazano w Tabeli 5, stwierdzono większą ilość potencjalnych biomarkerów ochrony cylastatyną niż w korze mózgowej. Warto zauważyć, że Sulf 40:2 wydaje się być najbardziej dyskryminującym gatunkiem w rdzeniu, biorąc pod uwagę jego najwyższe wyniki FC i VIP. Stwierdzono również różne gatunki PC i PE, w tym PE 36:5, PE 38:5, PE 38:6, PE 36:4, PE 34:3 i PC 36:6, żeby wymienić tylko kilka, oprócz Cer 42:2, dhHexCer 36:0 i HexCer 34:1, jako znaczące biomarkery ochrony cylastatyny w rdzeniu. We wszystkich przypadkach te lipidy były związane z częściowym lub całkowitym odzyskiwaniem poziomów kontrolnych wywołanym przez cylastatynę w porównaniu z ich poziomami zmienionymi przez cisplatynę. Dla wszystkich gatunków wartości AUC dla uzyskanych krzywych ROC były wyższe niż 0,85, co świadczy o ich dobrych zdolnościach do rozróżniania
DyskusjaW tej pracy określiliśmy ilościowo w sumie 108 rodzajów lipidów zawierających ważne lipidy strukturalne, takie jak fosfolipidy, sfingolipidy i cholesterol wraz z jego formami zestryfikowanymi nanerkakora i rdzeń szczurów leczonych cisplatyną i/lub cylastatyną. Przeprowadzono je w celu lepszego zrozumienia nefrotoksycznego działania cisplatyny i ochronnego działania cylastatyny. Stwierdzono, że do 63 gatunków lipidów uległo znacznej zmianie w rdzeniu przez leczenie cisplatyną, podczas gdy 56 gatunków lipidów zostało zmienionych w korze, co odzwierciedlauszkodzenie nerekw obu regionach. Chociaż tradycyjnie większość badań nad AKI indukowanym cisplatyną koncentruje się na komórkach kanalika proksymalnego inerkowyuszkodzenia kory, gdzie skupia się głównie akumulacja leku, ostatnie badania wskazują, że uszkodzenie w rdzeniu może być nawet tak poważne jak w korze, na podstawie testów apoptozy TUNEL [5]. Może to być związane z akumulacją cisplatyny w odcinku S3 kanalików proksymalnych [3,5], schodzącym w kierunku rdzenia zewnętrznego, poza potencjalnym bezpośrednim i wtórnym uszkodzeniem pętli Henlego [4]. Ponadto, rdzeń został wskazany jako najbardziej wrażliwynerkowyobszar do obserwacji globalnych zmian metabolitów związanych z cisplatyną w porównaniu z korą [5]. Nasze wcześniejsze wyniki wskazywały również na bezpośrednie uszkodzenie komórek rdzenia (poza uszkodzeniem wtórnym) przez cisplatynę, odzwierciedlone w różnych zmianach fosfolipidowych i kardiolipinowych [4]. Te nowe wyniki poszerzają te obserwacje o dodatkowe rodzaje i klasy lipidów zmienione przez cisplatynę i wzmacniają znaczenie uszkodzenia rdzenia kręgowego w AKI wywołanym cisplatyną.
Chociaż FC wnerkanie był znacząco zmieniony przez leczenie cisplatyną, zarówno całkowite CE, jak i wszystkie mierzone poszczególne gatunki CE były znacząco zwiększone zarówno w korze (ośmiokrotny wzrost dla całkowitego CE) i rdzeniu (czterokrotny wzrost dla całkowitego CE) w związku z indukowanym cisplatynąuszkodzenie nerek.Cholesterol jest kluczowym składnikiem błon plazmatycznych, lokując się między fosfolipidami i wpływając na płynność, ładunek powierzchniowy i interakcje polarnych grup głowy [35,36]. Jej obecność ma również fundamentalne znaczenie w raftach lipidowych, ustanawiając oddziaływania hydrofobowe z SM oraz jest niezbędna do segregacji cząsteczek i kontrolowania ich oddziaływania z innymi składnikami błony [37]. Komórki utrzymują równowagę cholesterolu między syntezą de novo w retikulum endoplazmatycznym (ER) a wychwytem za pośrednictwem LDL. Większość cholesterolu znajduje się w błonie plazmatycznej, ale może również powrócić do ER, gdzie FC może zostać przekształcony (poprzez estryfikację za pośrednictwem ACAT) w CE, który jest uważany za formę cholesterolu do przechowywania w cytozolu [36]. CE może również ulegać hydrolizie z powrotem do FC, tworząc cykl estru cholesterolu [36]. Fakt, że FC pozostała niezmieniona podczas leczenia cisplatyną, ale CE była zwiększona zarówno w korze, jak i rdzeniu, sugeruje zmianęnerkowymetabolizm cholesterolu związany z AKI indukowanym cisplatyną. Wcześniejsze badania wykazały dość podobne obserwacje zarówno w ludzkich komórkach kanalika proksymalnego HK-2, jak iw korze nerkowej myszy podczas ostrego niedokrwieniauszkodzenie nerek, z niezmienionym FC i podwyższonym poziomem CE [36]. W tym przypadku uszkodzenie błony plazmatycznej, powodujące zwiększony ruch FC z błony do ER, wydawało się najbardziej prawdopodobnym wyjaśnieniem, skutkującym eskalacją generacji CE. Pod tym względem uszkodzenie bogatych w cholesterol tratw lipidowych, a nie błony plazmatycznej, okazało się bardziej skuteczne w zwiększonym przenoszeniu cholesterolu do ER [36]. W poprzednich badaniach sugerowano również cytoprotekcyjną rolę CE. Wzrost poziomu CE odnotowano również u szczuranerkowykora mózgowa we wczesnym stadium nefropatii cukrzycowej [29]. Wyniki są również zgodne z globalnym wzrostem lipidów neutralnych wnerkowykanaliki proksymalne zgłaszane podczas leczenia cisplatyną [32]. Nasze wyniki wskazują po raz pierwszy na globalny wzrost całkowitego CE oprócz poszczególnych gatunków CE, zarówno wnerkowykora i rdzeń, podczas AKI wywołanej cisplatyną. Z drugiej strony, sam cylastatyna wydawał się nieznacznie zwiększać CE 18:0 i CE 22:6 tylko w korze, chociaż całkowite poziomy FC lub CE pozostały niezmienione. Ten niewielki efekt może wynikać z faktu, że jego cel, DHP-I, znajduje się w tratwach lipidowych w kanaliku proksymalnym (głównie w korze), a podczas jego interakcji mogą sugerować niewielkie zakłócenia błony. Z drugiej strony, jednoczesne podawanie cisplatyny i cylastatyny doprowadziło do zmniejszenia wszystkich rodzajów CE o podwyższonym stężeniu cisplatyny w korze, podczas gdy w rdzeniu prawie nie zaobserwowano efektu regeneracji, z jedynie częściową regeneracją CE18:2. . Wskazuje to na specyficzne działanie cylastatyny w komórkach kanalika bliższego, wywierając znaczącą ochronę przed ekspansją śmierci komórkowej, związaną z bezpośrednim uszkodzeniem cisplatyny na błonie plazmatycznej i raftach lipidowych w korze, podczas gdy uszkodzenia komórek związane z zaburzeniami równowagi cholesterolu w całym rdzeniu wydają się pozostawać w dużej mierze bez ochrony.
Sfingolipidy są aktywnymi lipidami znajdującymi się głównie w błonach komórkowych i są dość bogate w rafty lipidowe [37]. Ceramidy są głównymi metabolitami metabolizmu sfingolipidów, angażującymi różne cząsteczki i enzymy odgrywające ważną rolę w procesach komórkowych, w tym wzroście komórek, apoptozie, różnicowaniu, lekooporności i starzeniu się [38, 39]. Dodatkowo sfingolipidy uczestniczą w szlakach związanych z śmiercią komórek raka cisplatyny i AKI [33]. Ceramidy mogą być generowane przez kilka szlaków, w tym syntezę de novo, hydrolizę sfingomieliny lub recykling złożonych sfingolipidów [38]. Synteza de novo jest główną drogą i zachodzi w ER, od palmitoilo-CoA i seryny, poprzez szereg szlaków enzymatycznych do produkcji sfinganiny, która prowadzi do dihydroceramidów poprzez syntazę dihydroceramidową (CerS). Wreszcie desaturacja dhCer generuje Cer [40]. SM może być również hydrolizowany przez sfingomielinazy, wytwarzając Cer. Cer może zostać przekształcona w bardziej złożone sfingolipidy w aparacie Golgiego: ufosforylowana w celu wytworzenia Cer-1-P, cząsteczki sygnałowej; przekształcone w SM przez działanie syntazy SM; lub glikozylowane z wytworzeniem hezoksyloceramidów (glukozylo- lub galaktozyloceramidów), prekursorów sulfatydów [38]. Cer może również ulec degradacji do sfingozyny, prekursora sfingozyny-1-fosforanu (S1P), odgrywając ważną rolę w przeżywaniu i proliferacji komórek, stanach zapalnych i lekooporności [39]. Wreszcie degradacja S1P do etanoloaminy i heksadecenalu jest drogą wyjścia tej drogi [38].

Podczas oznaczania ilościowego gatunków sfingolipidów podczas leczenia cisplatyną zaobserwowano globalny wzrost całkowitych poziomów Cer, dhCer, HexCer i dhHexCer, co było szczególnie istotne w przypadku Cer. Różnice w zakresie kontrolinerkabyły bardziej widoczne, gdy określono ilościowo poszczególne podgatunki, przy czym 19 z 22 gatunków uległo zwiększeniu w korze (11 gatunków) i/lub rdzeniu (18 gatunków) po leczeniu cisplatyną. Jest to zgodne z wcześniejszymi obserwacjami wskazującymi na wzrost Cer i HexCer u myszynerkowykora mózgowa związana z leczeniem cisplatyną [33], ale tutaj stwierdziliśmy, że rdzeń jest również dotknięty tym efektem.
Obserwacje te mogą odzwierciedlać zwiększoną metaboliczną produkcję Cer/dhCer i HexCer/dhHexCer. Z jednej strony mogłoby się to odbywać poprzez zwiększoną aktywność CerS, w świetle wcześniejszych obserwacji wnerkowykora mózgowa, w której mierzono aktywność długołańcuchowego CerS podczas leczenia cisplatyną, a hamowanie CerS prowadziło do zmniejszenia obserwowanej akumulacji Cer/HexCer [33]. Co więcej, indukowane cisplatyną obniżenie poziomów SM/dhSM w korze i rdzeniu sugeruje dodatkowo zwiększoną produkcję Cer/dhCer poprzez hydrolizę SM/dhSM poprzez szlak sfingomielinazy (SMazy) [38], ze szczególnym wpływem na długołańcuchowe Cer/dhCer, wszystkie szkodliwe w modelach AKI [40]. Byłoby to również zgodne z faktem, że długołańcuchowe gatunki Cer wydają się być istotne podczas AKI [40] oraz z wcześniejszymi obserwacjami zwiększonej aktywności SMazy wnerkowykora mózgowa podczas leczenia cisplatyną [33]. Cer bierze udział w apoptozie indukowanej cisplatyną poprzez sygnalizację zarówno w szlakach wewnętrznych, jak i zewnętrznych [39]. W wewnętrznym szlaku mitochondrialnym cisplatyna powoduje permeabilizację mitochondrialnej błony zewnętrznej. Wzrost Cer, wraz z jego dalszymi metabolitami, może przyczyniać się do tej permeabilizacji, a tworzenie kanałów przez Cer ułatwia apoptozę w błonie mitochondrialnej, umożliwiając wnikanie Baxu do zewnętrznej błony mitochondrialnej, jak również odpływ cytochrom C [39]. Co więcej, apoptoza zewnętrzna, w której pośredniczy Fas, wykorzystuje receptor Fas zlokalizowany w raftach lipidowych, a w jego skupieniu pośredniczy aktywacja SMazy wywołana cisplatyną i podwyższenie poziomu Cer [39]. Cer determinuje zatem apoptozę w AKI indukowanej cisplatyną, podczas gdy ich poziomowanie poprzez transformację do HexCer wydaje się działać ochronnie [33] i wiąże się z opornością na cisplatynę [39]. Cer wytwarzany w dużych ilościach może również wpływać na właściwości fizyczne błon oraz może wypierać cholesterol i napędzać jego estryfikację [35]. Z drugiej strony SM występuje głównie w błonach komórkowych i ma bezpośredni związek z cząsteczkami cholesterolu, co jest szczególnie ważne w raftach lipidowych [41]. Brak regeneracji SM może być negatywny dla prawidłowego funkcjonowania błony [41].
Siarka jest obfita wnerka,zwłaszcza w błonie wierzchołkowej kanalików dystalnych [42]. Chociaż nie są niezbędne do normalnościfunkcja nerkiStwierdzono, że niedobór siarki jest kompensowany przez zwiększone wytwarzanie siarczanowanych glikolipidów i cholesterolu [42]. Sulfatyd jest kluczowym ligandem selektyny L wnerka,odgrywający istotną rolę w infiltracji monocytów donerkaśródmiąższowe [42]. Z drugiej strony białko mieliny i limfocytów (MAL) związane z tratwami lipidowymi tworzy kompleksy z sulfatydami i glikosfingolipidami wnerkowybłon, przyczyniając się do stabilizacji i sortowania mikrodomen wzbogaconych w glikosfingolipidy [42]. Nasze wyniki dotyczące zmian siarczanowych w korze i rdzeniu potwierdzają wcześniejsze badania, w których uważano, że różne gatunki sulfatydów są również zmieniane przez cisplatynę w nerkach [34].
Wszystkie gatunki Cer, dhCer, HexCer i dhHexCer zmienione w korze przez cisplatynę zostały częściowo lub całkowicie odzyskane przez jednoczesne podawanie cylastatyny, podczas gdy w rdzeniu nie odzyskano dużej ilości gatunków Cer, z prawie całkowitym odzyskaniem dhCer , HexCer i dhHexCer. Biorąc pod uwagę udział gatunków Cer w apoptozie zewnętrznej za pośrednictwem Fas i jej zablokowanie przez wiązanie cylastatyny z DHP-I w tratwach lipidowych w kanaliku proksymalnym, może to wyjaśniać efekt ochronny i odzyskiwanie Cer zachodzące głównie w komórkach kory. Jeśli chodzi o SM, dhSM i Sulf, regeneracja cylastatyny wydaje się być bardziej istotna w rdzeniu niż w korze, co sugeruje, że wtórne uszkodzenie jest osłabione przez działanie cylastatyny w proksymalnych kanalikach sięgających do rdzenia zewnętrznego, gdzie większośćuszkodzenie nerekjest skoncentrowany [4].
Fosfolipidy są najliczniejszymi gatunkami w błonach komórkowych, gdzie dominują PC i, w mniejszym stopniu, PE, z większą obecnością PC po stronie światła, a PE jest liczniejsze w cytozolowej ulotce liściowej [35, 43]. Lizofosfolipidy są natomiast gatunkami sygnalizacyjnymi, które mogą powstawać w wyniku hydrolizy glicerofosfolipidów, w tym LPC [35]. Stwierdzono, że większość z 60 zbadanych gatunków PC, PE i LPC została zmieniona przez leczenie cisplatyną, zarówno w korze, jak i rdzeniu, przy czym PC i LPC wykazywały większą liczbę zmian w korze, podczas gdy zmiany związane z PE były liczniejsze. i widoczny w rdzeniu. Zmianynerkowygatunki PC, PE lub LPC w wyniku leczenia cisplatyną są zgodne z wcześniejszymi zgłoszonymi obserwacjami w:nerkapodczas AKI [4,5,26,34,44]. Nasze wyniki wskazują, że większość zmienionych gatunków PE, PC i LPC została zmniejszona przez cisplatynę zarówno w korze, jak i rdzeniu. W odniesieniu do działania nefroprotekcyjnego cylastatyny, uderzająco, wyższy stopień częściowego lub całkowitego efektu wyzdrowienia zaobserwowano w rdzeniu dla lipidów zmienionych cisplatyną niż w korze. Innym interesującym faktem jest to, że wszystkie te gatunki PC, PE i LPC o zwiększonym poziomie cisplatyny w korze i rdzeniu zostały odzyskane przez cylastatynę, podczas gdy większość gatunków w korze o zmniejszonej zawartości cisplatyny była nadal zmieniona podczas jednoczesnego leczenia z cylastatyną. Może to wskazywać na wyższy stopień bezpośredniego uszkodzenia spowodowanego przez nagromadzenie cisplatyny w korze, pozostawanie bez ochrony przez cylastatynę i prowadzące do śmierci komórki i związanego z nią PC, PE (głównych składników błony komórkowej) i uwalniania LPC w ciałach apoptotycznych oraz, w związku z tym zmniejszenie ich poziomów. W przeciwieństwie do tego, wtórne uszkodzenia związane z apoptozą zewnętrzną i wynikającą z tego akumulacją białka w kanalikach proksymalnych mogą być chronione przez cylastatynę. Sugerowałoby to, że gatunki PC, PE i LPC zmniejszyły się w rdzeniu i są bardziej związane z wtórnym uszkodzeniem komórek wywołanym cisplatyną. Z drugiej strony, zwiększona liczba gatunków PC, PE i LPC może być związana albo z regeneracją błony komórkowej, albo z procesami sygnalizacji, co zgodnie z tymi wynikami może być bardziej związane z wtórną apoptozą zewnątrzpochodną, wywołaną przez cisplatynę, chronioną przez cylastatynę.
Ponadto zaobserwowano również indukowany cisplatyną spadek odsetka rodzajów PC i PE z wysoce nienasyconymi łańcuchami tłuszczowymi, co może być związane z procesami peroksydacji lipidów, a zmniejszałoby się pod wpływem cylastatyny [4,10,11].
Ogólnie rzecz biorąc, w obrębie gatunków lipidów tutaj oznaczonych ilościowo, efekt regeneracyjny cylastatyny zaobserwowano w 26 z 56 lipidów o zmienionej cisplatynie w korze oraz w 50 z 63 lipidów o zmienionej cisplatynie w rdzeniu. Być może odzwierciedla to wysoki stopień zmian lipidowych związanych z niezabezpieczonym bezpośrednim uszkodzeniem mitochondriów, wywołanym przez cisplatynę głównie w korze w porównaniu z rdzeniem, przy czym w całym rdzeniu wykryto więcej zmian lipidowych związanych z wtórną ochroną przed uszkodzeniami. Ponadto analiza wieloczynnikowa umożliwiła identyfikację potencjalnych nowych biomarkerów lipidowych zarówno dla AKI indukowanej cisplatyną, jak i cylastatynynefroprotekcja, w tym gatunki CE, Sulf, PE, PC, Cer lub HexCer, jak opisano w sekcjach 2.5 i 2.6. Z naszych ustaleń wynika, że CE 18:2 i PE 36:5 są potencjalnymi kandydatami na biomarkery zdolne do jednoczesnego rozróżniania uszkodzeń cisplatyny i cylastatynynefroprotekcjazarówno w korze, jak i rdzeniu. Jednakże, ponieważ odzyskiwanie tych dwóch gatunków za pomocą cylastatyny jest częściowe, bardziej odpowiednimi gatunkami jako biomarkerami byłby dhHexCer 34:0 w korze i Sulf 42:0 w rdzeniu, umożliwiając rozróżnienie obuuszkodzenie nerekoraz ochronę, przy czym cylastatyna w pełni odzyskuje zmieniony poziom cisplatyny do poziomu z grupy kontrolnej. Można to ekstrapolować na każde uszkodzenie nerek, w którym pośredniczy ligand Fas/Fas, ale powinno to zostać potwierdzone w przyszłych badaniach. W ostatnich latach zaproponowano kilka nowych biomarkerów AKI, głównie białek (np. KIM-1 [45] lub NGAL [46]). Fakt, że znaleźliśmy potencjalne nowe biomarkery AKI indukowanej cisplatyną i związanej z nią ochrony cylastatyną, o charakterze lipidowym wnerkatkanki, poszerza istniejącą wiedzę i zapewnia uzupełniające opcje dla lepszej diagnozy, rokowania i obserwacji. W rzeczywistości kombinacja wykrywania biomarkerów może być nawet potencjalnie wykorzystana jako wskazanie konkretnego AKI spowodowanego przez konkretny środek nefrotoksyczny (taki jak cisplatyna) lub inną przyczynę, a nawet rozróżnienie stanu/progresji choroby. Kolejnym krokiem byłoby ustalenie, czy nasze wyniki na zmienionychnerkowywzorce lipidowe znajdują również odzwierciedlenie w krążących lipidach we krwi lub w moczu. Umożliwiłoby to wykrywanie biomarkerów dla AKI i cylastatyny indukowanej cisplatynąnefroprotekcjabardziej wykonalne u pacjentów.
Indukowane przez cisplatynę zmiany poziomu lipidów związane z AKI są liczne i zróżnicowane, obejmując ważne lipidy strukturalne w całościnerkowystruktura: kora i rdzeń. Tłumienie wielu z tych zmian przez cylastatynę pokazuje jej ogromny potencjał poprawyczynność nereki zmniejszenie zmian strukturalnych związanych z lipidami, w korelacji ze znormalizowanymnerkowymorfologia. Ponownie, cylastatyna okazała się przydatna w wykrywaniu niechronionych bezpośrednich uszkodzeń komórek spowodowanych przez cisplatynę i wtórnych zmian związanych z uszkodzeniem pierwotnym, które mogą być upośledzone w kanalikach proksymalnych przez zablokowanie przez cylastatynę szlaku apoptotycznego, w którym pośredniczy Fas.
Materiały i metody
OdczynnikiZastosowano cilastatynę (dostarczoną dzięki uprzejmości Merck Sharp and Dohme SA, Madryt, Hiszpania) i cisplatynę (Pharmacia Nostrum (Madryt, Hiszpania). A {{0}}.9-procentowy roztwór NaCl (Braun Medical SA, Barcelona, Hiszpania) do przygotowania roztworów leków do podawania N-dodekanoilo-D-erytro-sfingozylofosforylocholina [SM 30:1 (d18:1/12:0)], D-glukozylo- ß-1,10-N-dodekanoilo-D-erytro-sfingozyna [HexCer 30:1 (d18:1/12:0)], N-dodekanoil D -erytro sfinganylofosforylcholina [dhSM 3{{50}}:0 (d18:0/12:0)], 1,2-dimyristoleoilo-sn glicero-3- fosfocholina [PC 28:2 (14:1/14:1)], 1-heptadekanoilo-2-hydroksy-sn-glicero-3-fosfocholina [LPC (17:0)] i 1, 2- dipalmitooleoil-sn-glicero-3-fosfoetanoloamina [PE 32:2 (16:1/16:1)] zakupiono od Avanti Polar Lipids (Alabaster, Alabama, USA). D-erytro-sfingozyna [Cer 42:1-d7 (d18:1/24:0)], N-stearoilo-D-erytro-dihydrosfingozyna [dhCer (36:0-d3)] oraz C16-30-sulfogalaktozyloceramid [Sulf 34:1(d18:1/16:0)] nabyto od Matreya LLC (State College, PA, USA). Cholesterol-d7 (FC-d7) i palmitynian cholesterolu d7 [CE (16:0-d7)] pochodziły z Sigma-Aldrich.
Stosowano wyłącznie rozpuszczalniki i odczynniki klasy HPLC lub LC-MS, w tym metanol (MeOH), acetonitryl (ACN) i izopropanol (iPrOH) (VWR International Eurolab, Barcelona, Hiszpania), a także chloroform, dichlorometan i mącz amonu (NH4COOH) (Sigma-Aldrich, Merck Life Science SL, Madryt, Hiszpania). Ultraczystą wodę otrzymano z systemu oczyszczania Milli-Q (Millipore, Merck Life Science SL, Madryt, Hiszpania).
Model zwierzęcyDorosłe samce szczurów Wistar (WKY, Criffa, Barcelona, Hiszpania) wyhodowano w Instituto de Investigación Sanitaria Gregorio Maraón (IiSGM, Madryt, Hiszpania). Przechowywano je w warunkach kontrolowanej temperatury, światła i wilgotności, ze swobodnym dostępem do pożywienia i wody. Leczenie podawano dootrzewnowo, jak opisano wcześniej [4,11] czterem grupom szczurów (n=6 zwierząt na grupę): Grupa 1: Kontrolna (CNT) — 0,9 procent NaCl wstrzyknięto do szczury w taki sam sposób jak leczenie dla grup 3 i 4; Grupa 2: Cilastatin (CIL) wstrzykiwany (150 mg kg 1 masy ciała (mc) dziennie); Grupa 3: Cisplatyna (CISPL) po wstrzyknięciu (unikalna dawka 5 mg kg 1 mc w dniu 0); oraz Grupa 4: Cisplatyna z cylastatyną (CISCIL) wstrzykiwana 5 mg kg 1 mc w dniu 0 i wstrzykiwana cylastatyna (150 mg kg 1 mc dziennie). Zwierzęta uśmiercono pięć dni po rozpoczęciu leczenia. Wcześniej od każdego szczura zbierano 24-godzinny mocz w klatkach metabolicznych. Surowicę krwi wyizolowano również przez odwirowanie. Nerki usunięto po perfuzji 0,9% roztworem soli fizjologicznej w 4°C, po czym przeprowadzono dekapsulację. Kora i rdzeń lewej stronynerkai poprzecznie przecięta połowa prawejnerkawycięto, szybko zamrożono w ciekłym N2 i ostatecznie przechowywano w temperaturze t 80 C. Druga połowa prawejnerkazostał utrwalony w 4% paraformaldehydzie i zatopiony w parafinie do badań histologicznych.
Badania histologiczneBarwienie hematoksyliną/eozyną (Sigma-Aldrich, Steinhem, Niemcy) przeprowadzono na 5 µm szczurze strzałkowymnerkaSekcje. Do wykonania mikrofotografii przy powiększeniu 20× i 60× do badania histologicznego wykorzystano mikroskop odwrócony IX70 (Olympus, Hamburg, Niemcy).
Wskaźniki funkcji nerekDo oznaczania BUN, kreatyniny, sodu i potasu w próbkach surowicy zastosowano AutoAnalyzer Cobas 711 (Roche, Bazylea, Szwajcaria). Do obliczenia GFR zastosowano wskaźnik klirensu kreatyniny. Białko całkowite oznaczono w moczu metodą kwasu sulfosalicylowego [47].
Homogenizacja tkanek Nerkatkanki kory i rdzenia (około 50 mg każda) dodano do 1,5 ml plastikowych probówek z zakrętką zawierających 800 µl roztworu buforu do lizy: 50 mM Tris–HCl pH 7,5, 125 mM NaCl, 5 mM NaF, 1,4 mM Na4O7P2, 1 mM Na3VO4, i inhibitor proteazy (Pierce Biotechnology, Inc., Rockford, IL, USA) oraz 1,5 mm kulki cyrkonowe. Tkanki poddano dezagregacji na homogenizatorze BeadBug-6 (Benchmark D1036-E, Bechmark Scientifific, Sayreville, NY, USA) przy 4500 obr./min, w trzech cyklach po 90 sekund. Homogenat dalej sonikowano przez 40 s przy 10 procentach amplitudy i odwirowywano przy 600 x g przez 1 min w 4°C. Porcję powstałego supernatantu rozcieńczono 1:10 w celu oznaczenia całkowitego białka w teście białkowym kwasu bicynchoninowego (BCA) (Pierce Biotechnology Inc., Rockford, IL, USA). Resztę ekstraktu białkowego przechowywano w t 80◦C do czasu analizy lipidomicznej.

Analiza lipidowa metodą LC-MS/MSLipidy wyekstrahowano z tkanek (co odpowiada 250 µg całkowitego białka) metodą Folcha [48]. Dziesięć mikrolitrów mieszaniny wzorców wewnętrznych (IS) dodano przed ekstrakcją lipidów w celu uzyskania względnej ilościowej oceny ilościowej lipidów, jak opisano wcześniej [49]. Mieszanina IS składała się z następujących elementów: CE (16:0-d7), FC-d7, Cer (42:{{10}} d7), HexCer (30 :1), LPC (17:0), PC (28:2), PE (32:2), SM (30:1), dhSM (30:0), dhCer (35:0) i Sulf (34 :1) w stężeniach podanych w Tabeli S4. Ekstrakty lipidowe wysuszono w strumieniu azotu i rozpuszczono w 250 µl acetonitrylu/izopropanolu (1:1, obj.:obj.), sonikowano przez 10 min, a następnie przeniesiono do fiolki do wstrzykiwań.
Pięć mikrolitrów ekstraktu lipidowego wstrzyknięto do systemu LC Eksigent UltraLC{{0}} (AB-Sciex LLP, Framingham, MA, USA). Gatunki rozdzielono na kolumnie Kinetex C18 (100 × 2,1 mm, 1,7 µm; Phenomenex, Macclesfifield, Wielka Brytania) pracującej w 55°C. Elucję przeprowadzono za pomocą dwuskładnikowej mieszaniny rozpuszczalnika A (60 procent acetonitrylu w wodzie, 10 mM NH4COOH) i rozpuszczalnika B (90 procent alkoholu izopropylowego w acetonitrylu, 10 mM NH4COOH) i gradientu liniowego od 60 procent A do 100 procent B w 12 min i 100 procent B do 60 procent A w ciągu 8 minut, przy natężeniu przepływu 0,4 ml min悆 1 . Do wykrywania lipidów użyto aparatu QTrap 4000 (AB-Sciex LLP, Framingham, MA, USA) z oprogramowaniem Analyst 1.6.2. Azot zastosowano zarówno jako gaz suszący (T: 500◦C, ciśnienie: 30 psi) jak i jako gaz do nebulizacji (50 psi). Detekcję ustawiono w dodatnim trybie elektrorozpylania (ESI) dla wszystkich klas lipidów z wyjątkiem Sulf, który analizowano w trybie ujemnym ESI. CE i FC analizowano przy użyciu źródła jonizacji chemicznej pod ciśnieniem atmosferycznym (APCI) w trybie jonów dodatnich. Zastosowano ukierunkowane podejście do wykrywania lipidów, ustawiając wielokrotne monitorowanie reakcji (MRM) przejścia dla każdego rodzaju lipidów w czasie ich retencji (Tabela S5). Chromatogramy pików LC-MS/MS przetwarzano za pomocą oprogramowania Skyline w wersji 4.1 (MacCoss Lab, Seattle, WA, USA) [50]. Gatunki lipidów oznaczono ilościowo przez bezpośrednie porównanie powierzchni każdego gatunku z powierzchnią IS dla ich klasy lipidów, jak opisano wcześniej [49]. Wyniki wyrażono jako nmol/mg białka. Całkowite poziomy klas lipidów określono jako sumę ilościowo zliczonych gatunków poszczególnych klas lipidów. Gatunki lipidowe oznaczono zgodnie z zalecaną notacją [51].
Analiza statystycznaWartości wyrażono jako średnią ± odchylenie standardowe. SPSS 11.5 (SPSS, Chicago, IL, USA) wykorzystano do statystyki opisowej i oceny różnic statystycznych w zmiennych między grupami poprzez analizę wariancji. W celu porównania zmiennych lipidowych w dwóch niesparowanych grupach, po testach normalności (Shapiro-Wilk) przeprowadzono testy parametryczne (dwustronny niesparowany t-Studenta) lub nieparametryczne (Mann-Whitney). Do korekcji współczynnika fałszywego odkrycia (FDR) wartości p przy porównywaniu wielu poszczególnych gatunków lipidów zastosowano metodę Benjamini-Hochberg. Dwustronna wartość p < 0.05="" i="" fdr="">< 0,1="" były="" brane="" pod="" uwagę="" w="" celu="" identyfikacji="" statystycznie="" istotnych="" różnic,="" aby="" uniknąć="" pominięcia="" potencjalnych="" kandydatów="" na="" biomarkery.="" krotność="" zmiany="" grupy="" x="" względem="" grupy="" y="" obliczono="" jako="" stosunek="" wartości="" średnich="" dla="" zmiennych="" odpowiednich="" grup="">
Wielowymiarową analizę danych (MVDA) przeprowadzono przy użyciu SIMCA w wersji 14.1 (MKS Umetrics, Uppsala, Szwecja) i MetaboAnalyst 5.0 (https://www.metaboanalyst.ca (dostęp 30 2 września) {{20}21)) [52], w tym nienadzorowanej PCA i nadzorowanej OPLSDA. Brakujące wartości zostały zastąpione metodą k-najbliższych sąsiadów. Zmienne były przekształcane logarytmicznie i skalowane w skali Pareto przed MVDA. Modele oceniano według ich wartości R2 i Q2. OPLS-DA został zwalidowany przez test permutacji (100 cykli). Wyniki VIP i wykresy S z modeli OPLS-DA zostały użyte do zidentyfikowania odpowiednich zmiennych w dyskryminacji grup CISPL versus CNT, CISCIL versus CNT i CISCIL versus CISPL. Jednoczesna zgodność z VIP > 1, ładunki przeskalowane jako współczynnik korelacji |p(corr)| > 0,5 i dwustronna wartość p < 0,05="" i="" fdr="">< 0,1="" dla="" porównania="" dwóch="" grup="" były="" kryteriami="" zastosowanymi="" do="" wyboru="" potencjalnego="" biomarkera.="" wartości="" auc="" uzyskano="" z="" wykresów="" krzywej="">
PatentyNastępujące patenty są częściowo związane z pracą przedstawioną w tym manuskrypcie: „Zastosowanie cylastatyny w celu zmniejszenia nefrotoksyczności różnych związków” (numery patentowe EP 2 143 429 B1; US 9 216 185 B2; US 9 522 128 B2 i US 9 757 349 B2). Są one przypisane do Fundación para la Investigación Biomédica Hospital Gregorio Marañón (FIBHGM) i licencjonowane przez FIBHGM na rzecz Telara Pharma SL Telara Pharma SL zawarła obecnie umowę licencyjną z Arch Biopartners.
